Clear Sky Science · nl
Computationeel ontwerp van generalistische cyclopropanases met stereodivergente selectiviteit
Waarom kleine drieledige ringen belangrijk zijn voor geneesmiddelen
Cyclopropanen—drieledige koolstofringen—zijn kleine, gespannen bouwstenen die drastisch kunnen veranderen hoe een geneesmiddel zich in het lichaam gedraagt. De exacte 3D‑rangschikking van atomen (de stereochemie) kan bepalen of een molecuul een bruikbaar medicijn wordt of een inactieve of zelfs schadelijke look‑alike. Dit artikel beschrijft een computationele strategie om enzymen te ontwerpen die betrouwbaar alle vier mogelijke 3D‑vormen van deze ringen uit dezelfde uitgangsmaterialen kunnen maken, waarmee de deur wordt geopend naar snellere en schonere verkenning van kandidaat‑geneesmiddelen.
Van één recept naar vier verschillende uitkomsten
Wanneer een eenvoudige dubbele binding (een olefine) reageert met een carbene‑donor zoals een diazoverbinding, kan het resultaat een cyclopropaanring zijn. Die ring kan echter vier verschillende stereoisomere vormen aannemen, elk met dezelfde atomen maar anders gerangschikt in de ruimte. Chemici willen toegang tot al deze vormen omdat ze heel verschillend met biologische doelen kunnen interageren en belangrijke geneesmiddel‑eigenschappen zoals absorptie, metabolisme en veiligheid kunnen beïnvloeden. Traditionele klein‑molecuulkatalysatoren behalen soms deze controle, maar dat met enzymen—de katalysatoren van de natuur—bereiken is moeilijk geweest, vooral wanneer zowel hoge selectiviteit als tolerantie voor veel verschillende substraten vereist is.
Enzymen ontwerpen op een computerscherm
De auteurs ontwikkelden een mechanismegebaseerde, meer‑toestand computationele workflow om dit probleem op te lossen. Ze gebruikten eerst kwantumchemische berekeningen om de vluchtige overgangstoestanden—de hoogenergetische structuren langs het reactiepad—te modelleren voor de vorming van elk van de vier cyclopropaan‑stereoisomeren. Deze modellen werden vervolgens geplaatst in de actieve centra van verschillende heme‑bevattende eiwitten, en de Rosetta‑eiwitontwerpsoftware werd gebruikt om te evalueren hoe goed elk eiwit elke overgangstoestand stabiliseerde of destabiliseerde. Cruciaal was dat de ontwerpscore mutaties beloonden die zowel de gewenste overgangstoestand bevoordeelden (positief ontwerp) als de concurrerende toestanden benadeelden (negatief ontwerp), waardoor het enzym in feite leerde één 3D‑product boven de anderen te ‘verkiezen’.
Een complete gereedschapskist van enzymen opbouwen
Met deze aanpak creëerde het team een familie van “generalistische” cyclopropanase‑enzymen. Beginnend vanaf myoglobine herontworpen ze het actieve centrum om varianten te verkrijgen die het trans‑(1R,2R)‑cyclopropaan met zeer hoge selectiviteit en goede activiteit produceren voor meer dan 20 verschillende olefinen, waaronder veeleisende niet‑geactiveerde en elektronarme substraten. Een eerder ontworpen myoglobine leverde al het complementaire trans‑(1S,2S)‑product. Om de twee cis‑producten te bereiken, wendden de auteurs zich tot andere heme‑eiwitten. Ze hermodelleerden het bacteriële enzym P450cam om varianten te verkrijgen die selectief het cis‑(1S,2R)‑product geven, en ze herbestemden human indoleamine 2,3‑dioxygenase‑1 (IDO1)—dat voorheen niet voor carbene‑chemie was gebruikt—om het cis‑(1R,2S)‑product te bevoordelen. Gezamenlijk kunnen deze vier biokatalysatoren elk stereoisomeer van dezelfde cyclopropaan‑producten leveren, vaak met tot 99% controle over zowel diastereomeer als enantiomeer.
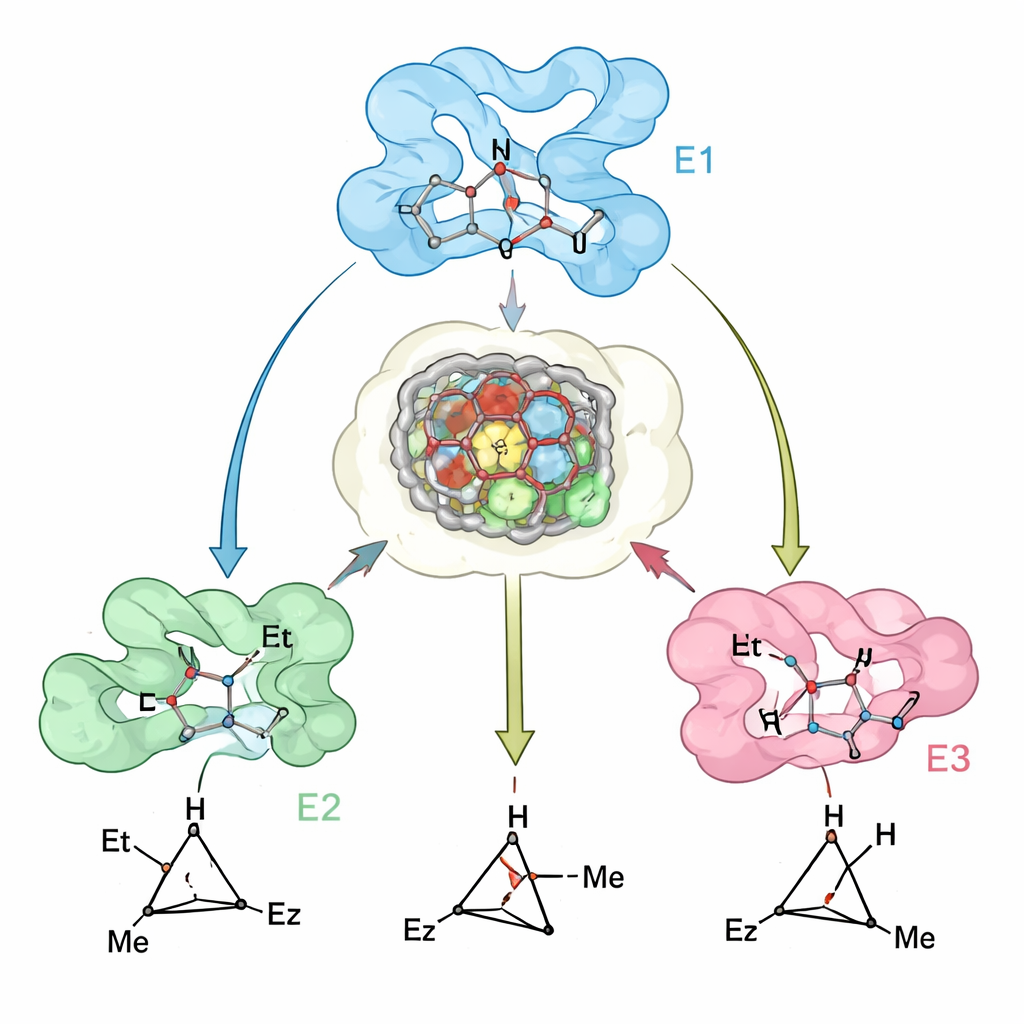
Inzicht in hoe ontwerp overeenkomt met realiteit
Om te testen hoe goed hun computationele modellen echte enzymen weerspiegelen, losten de onderzoekers kristalstructuren op van een belangrijke myoglobinevariant en vergeleken die met de voorspelde structuren. De overeenstemming was groot, en de experimentele gegevens benadrukten een subtiel maar belangrijk kenmerk: het actieve centrum van het eiwit is vooraf georganiseerd om de geprefereerde overgangstoestand te verwelkomen, terwijl kleine verschuivingen in nabijgelegen lussen en helices de binding van de “verkeerde” overgangstoestand energetisch ongunstig maken. Waar de voorspellingen minder nauwkeurig waren—zoals bij enkele volumineuze substraten—waren de verschillen terug te voeren op ruggegraatbewegingen die niet volledig in de modellering waren vastgelegd, wat duidelijke aanknopingspunten geeft voor verbetering van toekomstige ontwerpmethoden.
Wat dit betekent voor toekomstige geneesmiddelen en katalysatoren
Door fysica‑gebaseerde overgangstoestandsmodellering te combineren met slim eiwitherontwerp, laat dit werk zien dat stereochemische uitkomsten van enzymgeëscaleerde reacties vooraf geprogrammeerd kunnen worden in plaats van alleen via trial‑and‑error‑evolutie ontdekt te worden. De resulterende reeks cyclopropanases biedt chemici een praktische manier om volledige sets cyclopropaan‑stereoisomeren te maken uit een breed scala aan uitgangs‑olefinen, wat structuur‑activiteitsstudies in geneesmiddelenontdekking en natuurlijke productensynthese sterk vereenvoudigt. Dezelfde strategie zou aanpasbaar moeten zijn aan andere enzymtypes en reactiecategorieën, waardoor de creatie van biokatalysatoren die precieze 3D‑controle over complexe moleculen bieden, versneld wordt.
Bronvermelding: Shen, Z., Siriboe, M.G., Ren, X. et al. Computational design of generalist cyclopropanases with stereodivergent selectivity. Nat Commun 17, 1620 (2026). https://doi.org/10.1038/s41467-026-68327-1
Trefwoorden: biokatalyse, cyclopropanatie, enzymontwerp, stereochemie, heme-eiwitten