Clear Sky Science · nl
Glycerol-3-fosfaat-acyltransferase verergert α-synucleïne-geïnduceerde toxiciteit door lipideperoxidatie te verhogen
Waarom vetten in de hersenen ertoe doen bij Parkinson
De ziekte van Parkinson wordt doorgaans beschreven als een probleem met een eiwit dat alpha‑synucleïne heet en samenklontert en daarmee hersencellen die beweging regelen beschadigt. Deze studie laat zien dat hersenlipiden—vooral de manier waarop ze worden aangemaakt en beschadigd raken—een verrassend sterke rol spelen in hoe toxisch alpha‑synucleïne wordt. Door een vetvormend enzym te onthullen dat zenuwcelbeschadiging verergert, wijst het werk op een nieuw, geneesmiddelbaar pad dat bestaande pogingen om Parkinson bij de bron aan te pakken kan aanvullen.
Een eiwit dat zich misdraagt bij Parkinson
Mensen met Parkinson verliezen geleidelijk dopamine-producerende zenuwcellen in een diepgelegen hersengebied dat beweging coördineert. In deze stervende cellen vinden wetenschappers vaak dichte afzettingen, Lewy-lichaampjes genoemd, vol met het eiwit alpha‑synucleïne. In zeldzame families veroorzaken mutaties of extra kopieën van het alpha‑synucleïne-gen direct Parkinson, maar veelvoorkomende genetische varianten in dat gen verhogen het risico slechts licht. Dat suggereert dat andere genen en routes beïnvloeden hoe schadelijk alpha‑synucleïne wordt. Steeds meer bewijs wijst op lipiden—vetten en vetachtige moleculen die celmembranen en energieopslag vormen—als sleutelpartners bij zowel alpha‑synucleïne-aggregatie als zenuwcelsterfte.
Een krachtig lipide-enzym gevonden in fruitvliegmodellen
De onderzoekers gebruikten fruitvliegen die zo zijn gemodificeerd dat ze menselijk alpha‑synucleïne in hun zenuwstelsel produceren als een levende proefopstelling. Deze vliegen ontwikkelen Parkinson-achtige problemen: verlies van dopamine-producerende neuronen, moeite met klimmen en verstoorde dag-nachtactiviteitsritmes. Het team veranderde systematisch de vliegversies van menselijke Parkinson-risicogenen om te zien welke de impact van alpha‑synucleïne beïnvloedden. Eén gen stak eruit: een gen genaamd mino, dat een mitochondriale vorm van het enzym glycerol‑3‑fosfaat‑acyltransferase (GPAT) produceert. GPAT bevindt zich bij het beginpunt van de synthese van fosfolipiden en triglyceriden—de lipiden die membranen en vetdruppels vormen. Wanneer het team de activiteit van mino in neuronen verminderde, behielden alpha‑synucleïne-vliegen meer van hun dopaminerge neuronen en bewogen ze langer beter; het verhogen van mino had het tegenovergestelde, schadelijke effect.
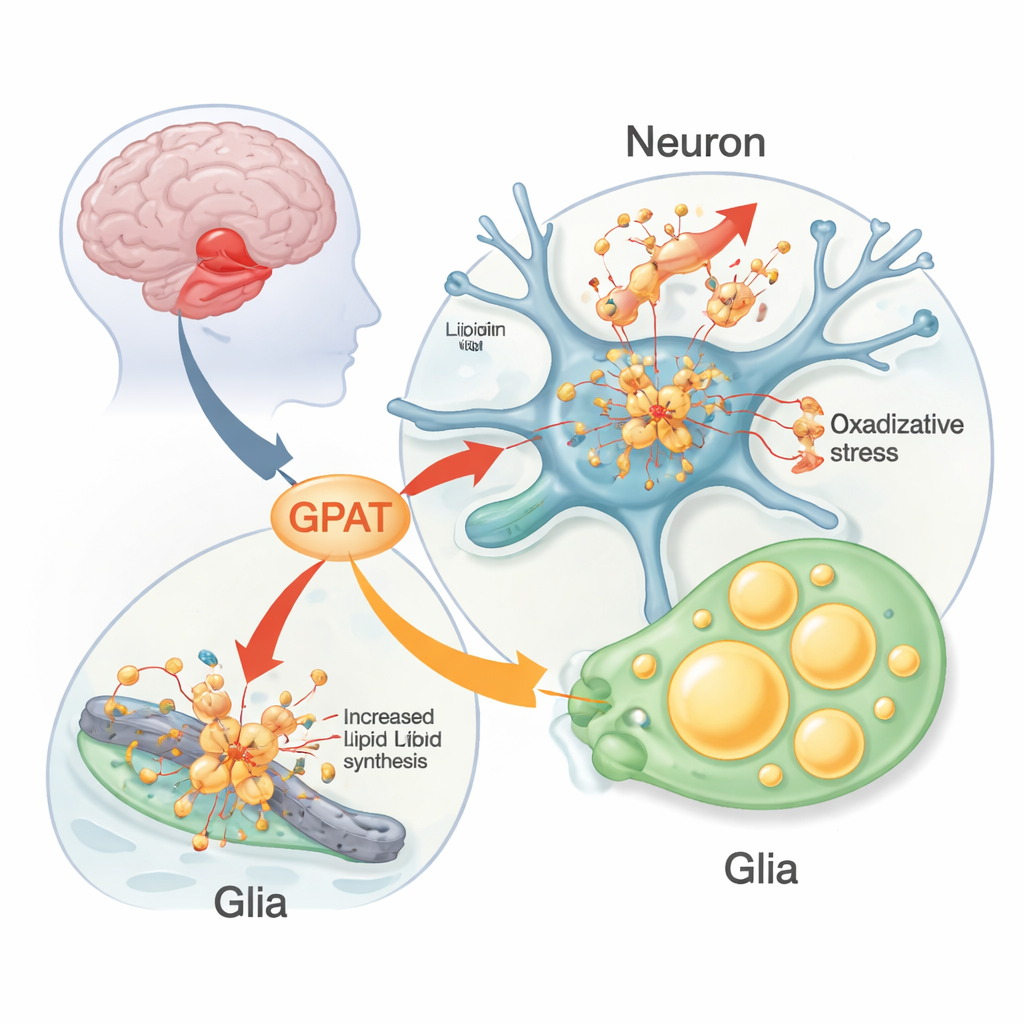
Beschadigde vetten, gestreste mitochondriën en gliale vetdruppels
Dieper onderzoek toonde aan dat GPAT beïnvloedde hoeveel oxiderende schade zich ophoopte in hersenlipiden. Bij alpha‑synucleïne-vliegen die bij hogere temperatuur werden gehouden (wat ziektekenmerken verergert), nam lipideperoxidatie—chemische “roest” van vetten—toe in hersenmembranen. Het verlagen van mino verminderde deze schade, terwijl overexpressie deze verhoogde; zonder alpha‑synucleïne had het veranderen van mino weinig effect. Markers van celdood in het visuele hersengebied weerspiegelden dit patroon. Het team observeerde ook een opvallende ophoping van lipidedruppels—kleine vetopslagsferen—niet in de neuronen zelf maar in naburige gliale cellen. Deze druppels werden groter met de leeftijd in alpha‑synucleïne-vliegen en werden beïnvloed door enzymen die triglyceriden opbouwen of afbreken, wat een actieve metabole samenwerking tussen neuronen en glia onder stress benadrukt.
Metabole herprogrammering en alpha‑synucleïne-aggregatie
Metabolietmetingen van vliegbrains lieten zien dat expressie van alpha‑synucleïne verband hield met een knelpunt in de energieleverende cyclus van de cel: citraat en isocitraat, twee tussenproducten van de tricarbonzuurcyclus (TCA), stapelden zich sterk op, terwijl downstream-stappen minder sterk veranderden. Lactaatniveaus stegen ook, wat consistent is met verhoogde glycolyse. Tegelijkertijd toonde gedetailleerde lipideprofilering verschuivingen in de balans van membraanfosfolipiden en hun vetzuursamenstelling, in de richting van soorten die vatbaarder zijn voor oxidatieve schade. Wanneer het team meerdere GPAT-enzymen verminderde—mino in mitochondriën en aanverwante enzymen op het endoplasmatisch reticulum—hoopte alpha‑synucleïne nog steeds op, maar nam de neiging om hogere-orde oligomeren (meerdere eiwittenbundels) te vormen af, en vertoonden mitochondriën minder tekenen van reactieve zuurstofstress en “veroudering.”
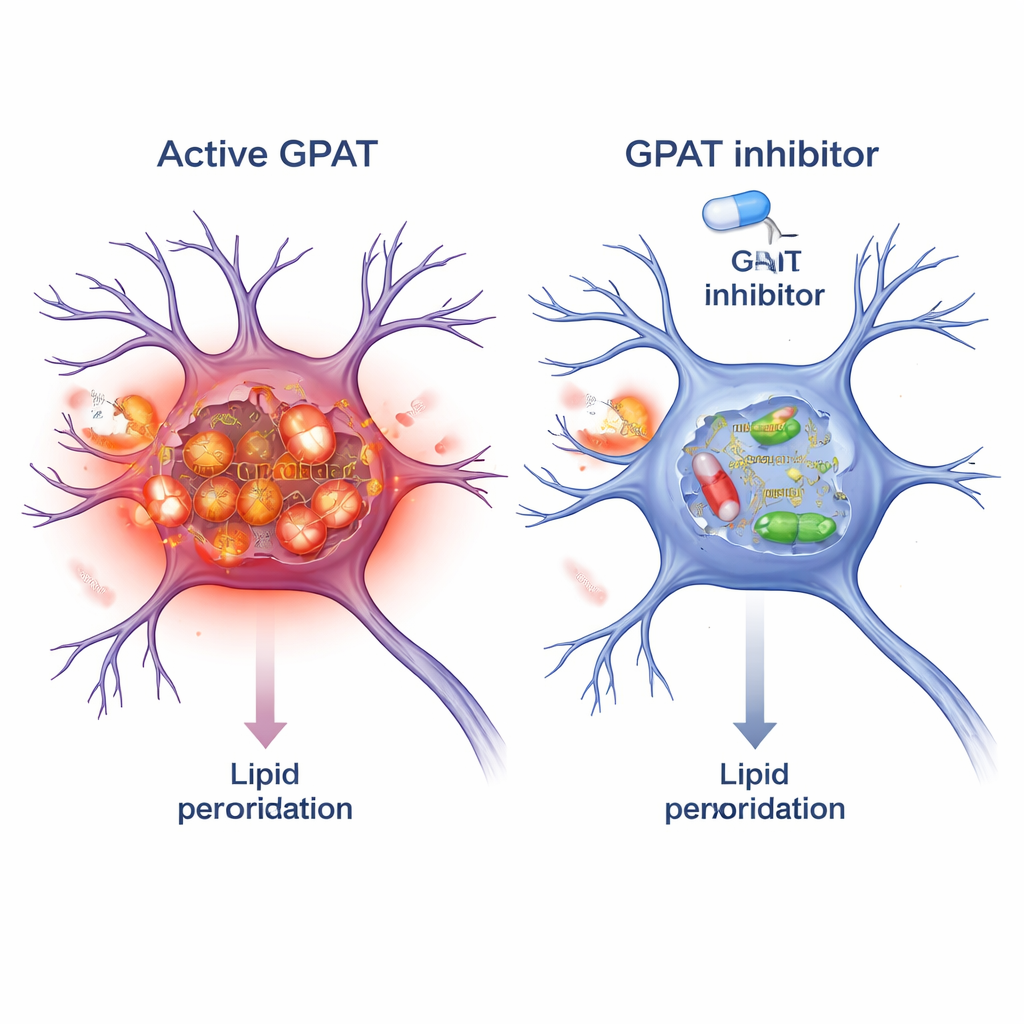
GPAT blokkeren als beschermende strategie
Aangezien GPAT een enzym is, kan het worden gericht met kleine molecule-remmers. De onderzoekers testten FSG67, een bestaande GPAT-remmer oorspronkelijk ontwikkeld voor obesitas en diabetes. Bij alpha‑synucleïne-vliegen reproduceerde het toevoegen van FSG67 aan het voer de voordelen van genetische GPAT-knockdown: verbeterde beweging, beter behoud van dopaminerge neuronen, minder schadelijke alpha‑synucleïne-oligomeren en verminderde mitochondriale oxidatieve stress. Om te onderzoeken of dit concept zich uitstrekt tot zoogdieren, behandelden ze muishersenneuronen in kweek met vooraf gevormde alpha‑synucleïne-fibrillen, die toxische aggregaten zaaien. Gelijktijdige behandeling met FSG67 verminderde de ophoping van gefosforyleerd alpha‑synucleïne en verlaagde meerdere onafhankelijke markers van lipideperoxidatie binnen deze neuronen.
Wat dit betekent voor mensen met Parkinson
In eenvoudige bewoordingen laat dit werk zien dat de manier waarop de hersenen met vetten omgaan alpha‑synucleïne‑toxiciteit kan versterken of verminderen. Wanneer GPAT zeer actief is, worden vatbaardere lipiden ingebouwd in membranen en opslagdruppels, waardoor ze gemakkelijker oxideren; deze beschadigde vetomgeving lijkt schadelijke vormen van alpha‑synucleïne te bevorderen en mitochondriën, de energiecentrales van de cel, te belasten. Het terugschakelen van GPAT—zowel genetisch als met een geneesmiddel—verschuift de balans naar minder lipide “roest”, minder toxische eiwitassemblages en gezondere neuronen. Hoewel deze bevindingen voorlopig zijn en afkomstig uit vliegen en gekweekte muiscellen, zetten ze lipidemetabolisme, en GPAT in het bijzonder, in de schijnwerpers als een veelbelovende nieuwe invalshoek voor Parkinson‑therapieën die strategieën die zich direct op alpha‑synucleïne richten, zouden kunnen aanvullen.
Bronvermelding: Ren, M., Lim, G.G.Y., Tang, W. et al. Glycerol 3-phosphate acyltransferase exacerbates α-synuclein-induced toxicity by increasing lipid peroxidation. Nat Commun 17, 1618 (2026). https://doi.org/10.1038/s41467-026-68325-3
Trefwoorden: Ziekte van Parkinson, alpha-synucleïne, lipideperoxidatie, GPAT-remmer, neurodegeneratie