Clear Sky Science · nl
Structuur van het SHOC2-KRAS-PP1C-complex onthult RAS-isoform-specifieke bepalende factoren en inzichten in het richten op complexassemblage door RAS-remmers
Hoe cellen beslissen wanneer ze groeien
Onze cellen vertrouwen op een intern bedradingsysteem om te bepalen wanneer ze moeten groeien, delen of stil blijven. Centraal in dit systeem staan RAS-eiwitten, kleine moleculaire schakelaars die in kanker vaak defect raken. Deze studie onderzoekt diepgaand hoe een specifieke groep eiwitten—SHOC2, RAS en PP1C—samenkomen om een sleutelschakel voor groei om te zetten, en hoe moderne kankermedicijnen mogelijk kunnen worden afgestemd om dat proces effectiever te blokkeren en te voorkomen dat tumoren behandeling weten te omzeilen.
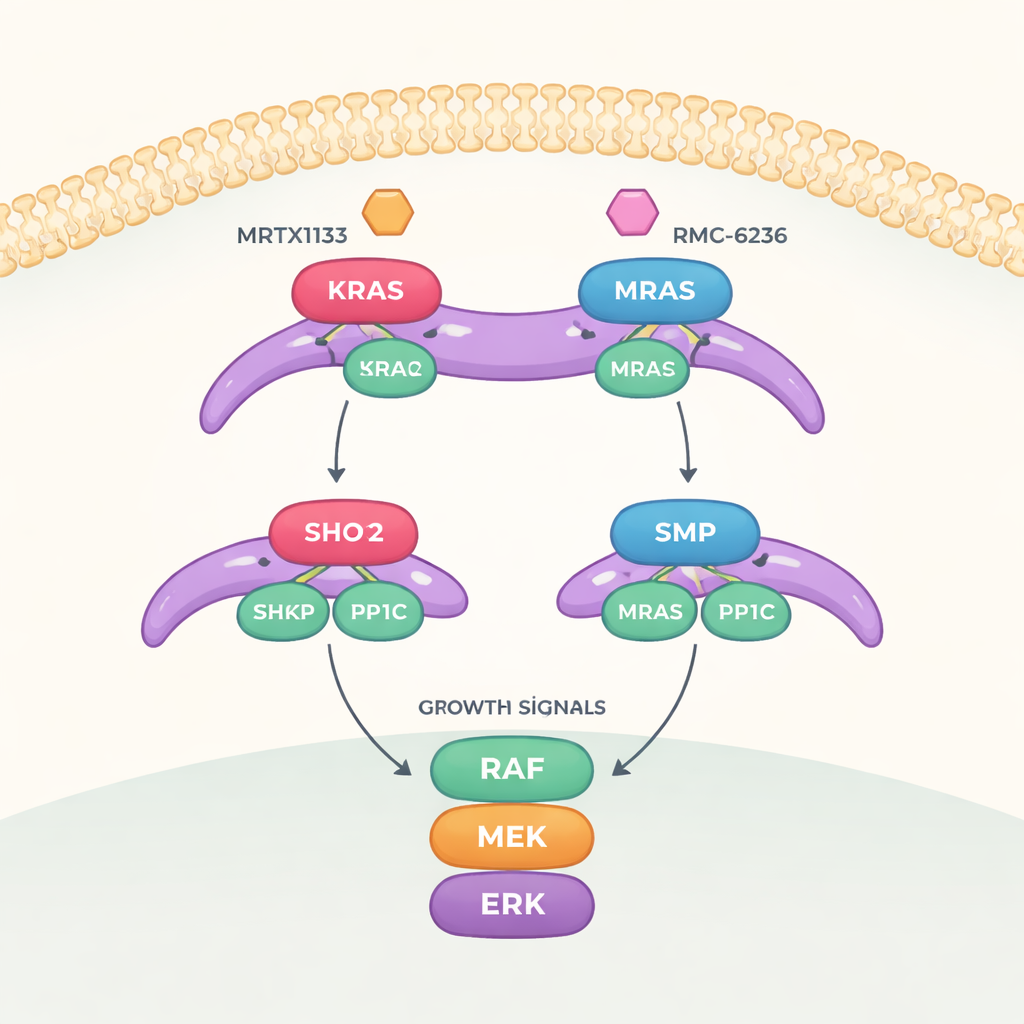
Een groeischakelaar met drie cruciale delen
Het werk richt zich op een signaleringsroute die de MAPK-route heet, die groeiberichten van het celoppervlak naar de kern brengt. Om deze route volledig aan te zetten, moet een ander eiwit, RAF, van een „uit”- naar een „aan”-toestand worden geschakeld. Die schakel wordt gecontroleerd door een drievoudig complex bestaande uit SHOC2 (een steiger die onderdelen bij elkaar houdt), PP1C (een enzym dat een fosfaatgroep verwijdert) en een actieve RAS-eiwit. Wanneer dit trio assembleert, verwijdert het een specifieke fosfaatmarkering van RAF, waardoor RAF de onderliggende groeicascade kan activeren.
Waarom een partner met lagere affiniteit toch belangrijk is bij kanker
Er bestaan verschillende soorten RAS-eiwitten. MRAS vormt een zeer strak complex met SHOC2 en PP1C, terwijl de bekender geworden kankergeneesheer KRAS—en ook HRAS en NRAS—zwakkere varianten van hetzelfde complex vormen. Verrassend genoeg blijken kankercellen gedreven door gemuteerd KRAS, HRAS of NRAS sterk afhankelijk te zijn van SHOC2, ook al zijn hun complexen minder stabiel. Grote genetische screeningsdatasets laten zien dat veel tumoren met bepaalde RAS-mutaties—vooral die mutaties op sleutelposities zoals Q61 en G13—zeer gevoelig zijn voor verlies van SHOC2, wat betekent dat deze assemblage essentieel is voor hun overleving.
De vorm van het KRAS-complex onthuld
Tot nu toe hadden wetenschappers alleen een hoge-resolutiestructuur gezien van het sterke MRAS-gebaseerde complex. De zwakkere KRAS-variant viel te gemakkelijk uit elkaar om vast te leggen. In deze studie gebruikten de auteurs ziektegerelateerde mutaties die de contacten tussen de componenten subtiel versterkten om het SHOC2–KRAS–PP1C-complex lang genoeg te stabiliseren om het te imageren met cryo-elektronenmicroscopie. Ze vonden dat de algemene architectuur sterk overeenkomt met het MRAS-complex, maar dat KRAS enkele kleine structurele kenmerken mist die MRAS gebruikt om SHOC2 en PP1C steviger vast te grijpen. Daardoor begrenst het KRAS-complex een kleinere contactoppervlakte en vormt het minder bindingen, wat verklaart waarom het van nature minder stabiel is, ook al blijft het zeer belangrijk in tumoren waarin KRAS overactief is.
Hoe RAS-medicijnen de complexassemblage blokkeren
Het team onderzocht vervolgens hoe twee klassen RAS-gerichte medicijnen dit drievoudige complex beïnvloeden. MRTX1133, ontworpen om te binden aan een pocket nabij een flexibele regio van KRAS bekend als Switch‑II, vergrendelt deze regio in een vorm die botst met het SHOC2-oppervlak. Dit voorkomt sterk dat nieuwe SHOC2–KRAS–PP1C-complexen vormen, hoewel het minder effectief is in het uiteenhalen van reeds bestaande complexen. Een tweede geneesmiddel, RMC‑6236, werkt samen met een hulpeiwit (cyclophiline A) en blokkeert eveneens dezelfde KRAS-oppervlakken die nodig zijn voor SHOC2-binding. Geen van beide middelen bindt van nature MRAS, zodat het hoge‑affiniteits MRAS-complex intact blijft en kan helpen de groeiroute opnieuw te activeren wanneer KRAS wordt geremd.
Op weg naar dubbele targeting om resistentie te voorkomen
Om te testen of dubbele targeting mogelijk is, ontwierpen de onderzoekers een versie van MRAS waarvan de Switch‑II-pocket zo was aangepast dat MRTX1133 nu kon binden. Deze mutant vormde nog steeds een sterk complex met SHOC2 en PP1C, maar het medicijn blokkeerde nu de assemblage en verminderde zijn vermogen om RAF in buisproefassays aan te zetten. Gecombineerd met gegevens over SHOC2-bindende verbindingen tonen deze resultaten aan dat het realistisch is medicijnen te ontwerpen die zowel het KRAS‑gebaseerde als het MRAS‑gebaseerde complex uitschakelen. Voor een niet‑specialist is de kernboodschap dat kankercellen meerdere, nauw verwante schakelaars gebruiken om groeisignalen te laten doorstromen, vooral wanneer één schakelaar wordt bestreken door een geneesmiddel. Door de precieze vormen en contacten binnen deze eiwitassemblages te begrijpen, kunnen onderzoekers nu therapieën plannen die beide reserve‑routes tegelijk raken, waardoor het voor RAS‑gedreven kankers moeilijker wordt zich aan te passen en resistentie te ontwikkelen.
Bronvermelding: Bonsor, D.A., Finci, L.I., Potter, J.R. et al. Structure of SHOC2-KRAS-PP1C complex reveals RAS isoform-specific determinants and insights into targeting complex assembly by RAS inhibitors. Nat Commun 17, 1614 (2026). https://doi.org/10.1038/s41467-026-68319-1
Trefwoorden: RAS-signaaloverdracht, KRAS-remmers, MAPK-route, proteïnecomplexen, medicatie-resistentie