Clear Sky Science · nl
Injecteerbare hydrogels voor behandeling van osteomyelitis veroorzaken metabole herprogrammering ter bescherming tegen herinfectie
Het lichaam tot zijn eigen infectiebestrijder maken
Botinfecties, vooral die veroorzaakt door antibiotica‑resistente bacteriën, zijn berucht lastig te genezen en keren vaak terug, zelfs na langdurige kuursen met geneesmiddelen en operaties. Deze studie beschrijft een injecteerbare gel die direct in geïnfecteerd bot wordt ingebracht, waar hij niet alleen kiemen doodt maar ook de aangeboren verdediging van het lichaam traint en het bot helpt zichzelf te herstellen. Het werk wijst op een toekomst waarin materialen meer doen dan alleen antibiotica afleveren—ze coachen ook ons immuunsysteem om terugval te voorkomen.
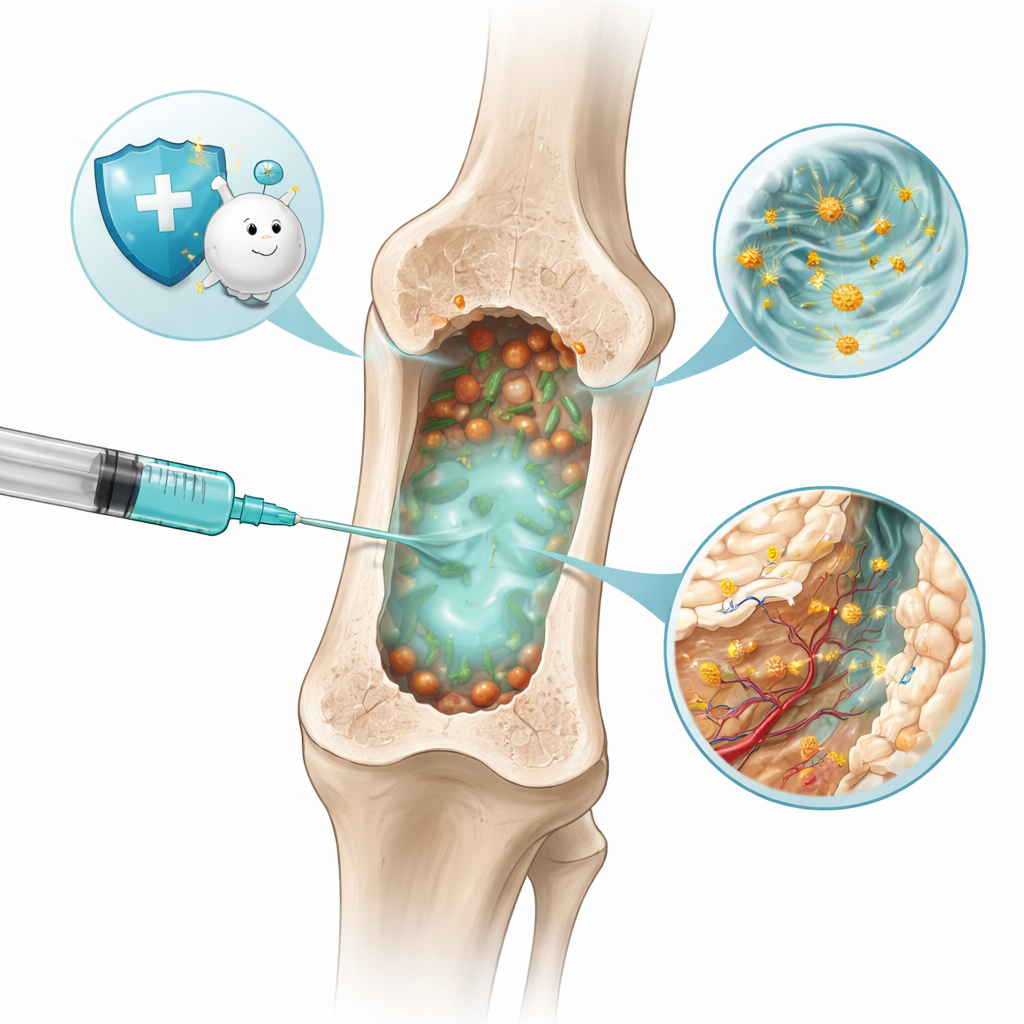
Een kleverige gel die in het bot vormt
De onderzoekers ontwikkelden een zacht materiaal, een hydrogel, dat als vloeistof geïnjecteerd kan worden en vervolgens snel uithardt in de botmergholte, het sponsachtige centrum van botten waar veel immuuncellen ontstaan. Hun gel, GaCuVan&HACHO‑BSA genoemd, bestaat uit twee in elkaar grijpende netwerken. Het ene netwerk combineert een natuurlijk plantaardig molecuul uit zoethout (glycyrrhizinezuur), koperionen en het antibioticum vancomycine. Het andere gebruikt een aangepaste vorm van hyaluronzuur—een suiker die in onze gewrichten voorkomt—gekoppeld aan een veelvoorkeiend bloedproteïne. Samen vormen deze componenten een poreus, flexibel steigersysteem dat door een naald stroomt, onregelmatige ruimten vult en geleidelijk afbreekt over ongeveer een maand.
Bacteriën en toxines bij de bron vangen
Eens in het geïnfecteerde bot gedraagt de hydrogel zich als een slimme spons. Zijn kleine poriën en chemische groepen maken het mogelijk bacteriën te vangen, zoals methicilline‑resistente Staphylococcus aureus (MRSA), samen met fragmenten van bacteriële celwanden en ontstekingsmoleculen die door het geïnfecteerde weefsel drijven. Vancomycine aan het oppervlak van de gel helpt de gevangen bacteriën te grijpen en te doden, terwijl andere chemische bindingen zich vasthechten aan bacteriële toxines en signaalproteïnen. Laboratoriumtests toonden aan dat deze gel de meeste bacteriën en schadelijke factoren uit de omgeving veel beter kon verwijderen dan simpelere gels, en dat hij voldoende sterk bleef om botdefecten te ondersteunen en te vullen terwijl dat gebeurde.
Aangeboren immuniteit herprogrammeren
Buiten het functioneren als een lokaal medicijnreservoir verandert de hydrogel het geïnfecteerde merg in een oefenterrein voor frontlijn‑immuuncellen. Omdat de gel bacteriële fragmenten en ontstekingssignalen vasthoudt, worden deze signalen continu aan nabijgelegen macrofagen en andere aangeboren cellen gepresenteerd in plaats van snel weggespoeld te worden. In ratexperimenten leidde dit tot een golf van kortdurende ontsteking: meer witte bloedcellen arriveerden en bot‑resident immuuncellen schakelden over naar een geactiveerde, bacteriebestrijdende toestand. Diepgaande genetische en metabole analyses van het beenmerg toonden aan dat sleutelroutes voor gevaarherkenning werden aangezet en dat cellen hun energiegebruik herbedenkten richting snel, suikerverbrandend metabolisme—kenmerken van zogenaamde “getrainde immuniteit,” een vorm van aangeboren geheugen die cellen voorbereidt om sterker te reageren bij een volgende confrontatie met indringers.
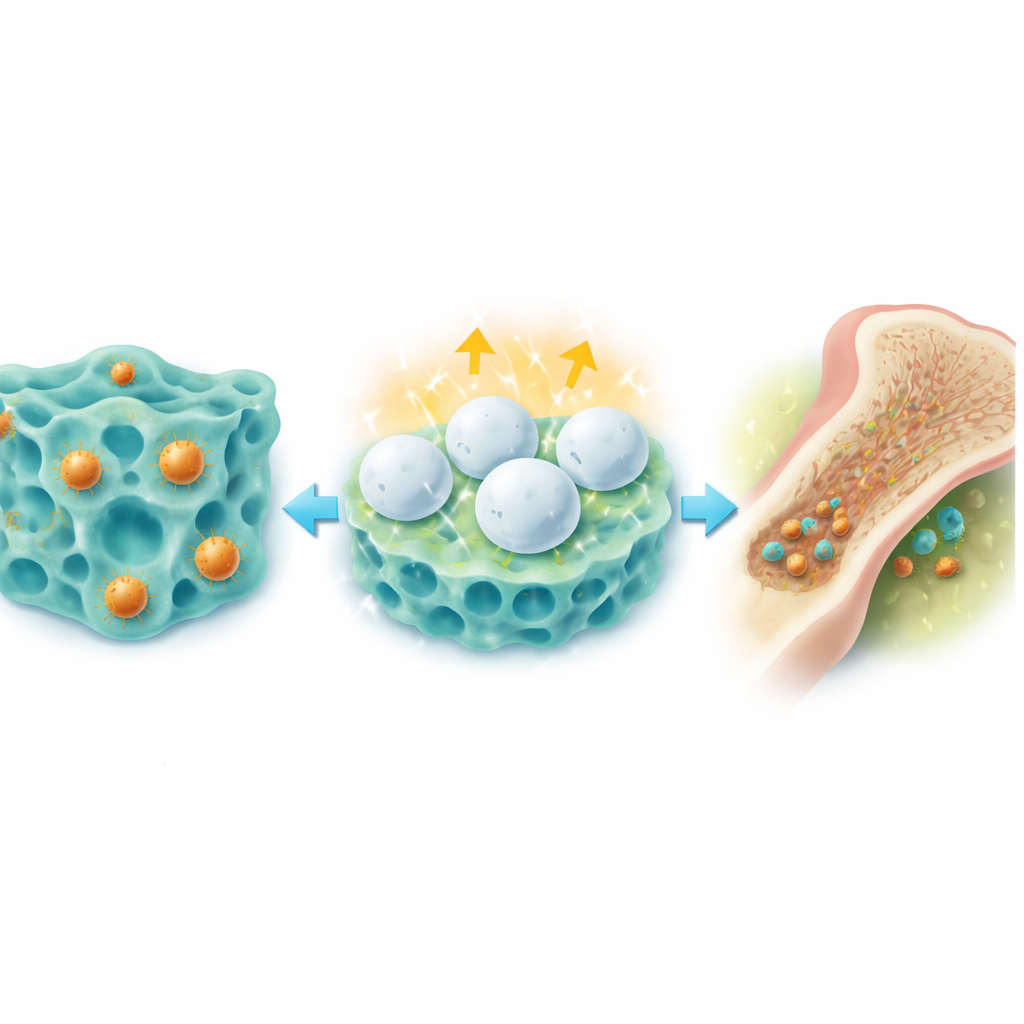
Infectie opruimen en botgenezing stimuleren
Bij ratten met ernstige MRSA‑botinfecties reduceerde een enkele in‑bot injectie van de hydrogel de bacteriële aantallen in het merg snel tot bijna nul, terwijl dieren behandeld met standaard vancomycine of eenvoudigere gels vaak zwaar geïnfecteerd bleven. De gel stimuleerde ook de aanmaak van nieuw bot. Koper en de zoethoutafgeleide component zetten stamcellen beide in de richting van botvormende cellen, wat markers van botgroei verhoogde en de botdichtheid en -sterkte in beschadigde scheenbenen vergrootte. Beeldvorming en weefselkleuring over meerdere weken toonden dat defecten in geïnfecteerde botten van behandelde dieren bijna sloten, waarbij georganiseerd, gezond nieuw bot de beschadigde gebieden verving.
Bescherming tegen toekomstige infecties
Een opvallende vondst was dat botten die vooraf met de hydrogel waren behandeld later beter bestand waren tegen aanvallen. Toen ratten die hun eerste infectie hadden uitgevocht opnieuw werden uitgedaagd—of met dezelfde MRSA‑stam of met verschillende stammen en verwante bacteriën—mobiliseerden hun botten snel sterke ontstekingsreacties, beperkten bacteriële groei en voorkwamen vaak helemaal herinfectie. Het blokkeren van het veranderde suikermetabolisme van de cellen deed deze bescherming verdwijnen, wat bevestigde dat metabole “herprogrammering” van aangeboren immuuncellen essentieel was. Het effect trad op bij zowel jonge als oudere ratten, maar was zwakker bij diabetische dieren, waarvan het immuunsysteem al metabool verstoord is.
Wat dit voor patiënten zou kunnen betekenen
Voor iemand met een chronische of medicijnresistente botinfectie zou dit type injecteerbare gel mogelijk meer kunnen bieden dan een tijdelijke antibiotische impuls. Door de mergholte te voorzien van een materiaal dat kiemen opvangt, antibiotica en botopbouwende ionen afgeeft en aangeboren immuuncellen traint om sneller en krachtiger op toekomstige dreigingen te reageren, zouden artsen zowel de huidige ziekte kunnen genezen als het risico op terugval kunnen verlagen. Hoewel meer onderzoek nodig is—vooral in grotere dieren en bij mensen met complexe aandoeningen—introduceert de studie een nieuwe manier van denken over de behandeling van botinfecties: gebruik maken van slimme materialen niet alleen om geneesmiddelen af te leveren, maar om de lokale immuun‑ en herstelomgeving te hervormen voor langdurige bescherming.
Bronvermelding: Chen, H., Wei, L., Yu, Q. et al. Injectable hydrogels for osteomyelitis treatment induce metabolic reprogramming for protection against reinfection. Nat Commun 17, 1613 (2026). https://doi.org/10.1038/s41467-026-68318-2
Trefwoorden: osteomyelitis, hydrogeltherapie, getrainde immuniteit, botregeneratie, antibioticaresistentie