Clear Sky Science · nl
Omkeerbare lipide-gemedieerde pH‑schakeling van connexine-46/50 door cryo-EM
Waarom kleine cellulaire kanalen belangrijk zijn voor gezondheid en ziekte
Elke seconde wisselen onze cellen elektrische signalen en kleine moleculen uit via microscopische tunnels die gap junctions worden genoemd. Deze kanalen helpen het hart synchroon te laten kloppen, het brein toxische bijproducten te verwijderen en de ooglens transparant te houden. Wanneer de omstandigheden in cellen zuur worden, zoals bij beroerte, hartaanval of de ontwikkeling van staar, sluiten veel van deze kanalen — maar hoe ze zuurtegraad waarnemen en daarop reageren is lange tijd een raadsel geweest. Deze studie gebruikt hoogresolutie cryo-elektronenmicroscopie om, bijna atoom voor atoom, te onthullen hoe specifieke kanalen in de ooglens reageren op zuur en hoe dit proces volledig omkeerbaar kan zijn.
Cellulaire tunnels die weefsels in sync houden
Gap junctions zijn opgebouwd uit eiwitten genaamd connexines, die zich samenvoegen tot ringvormige kanalen die de membranen van twee naburige cellen overspannen. Dit werk richt zich op een paar nauw verwante connexines, connexine‑46 en connexine‑50, die kanalen vormen in de lens van het oog. Deze kanalen laten ionen en kleine moleculen direct tussen cellen stromen en helpen zo de helderheid van de lens en de algemene gezondheid van het weefsel te behouden. Wanneer cellen echter onder stress staan, kunnen dezelfde kanalen paden worden voor schadelijke signalen. Om weefsels te beschermen sluiten gap junctions wanneer het celinterieur zuurder wordt. Het begrijpen van het fijnmazige mechanisme van deze “pH‑schakeling” is belangrijk om te verklaren hoe weefsels stress overleven en waarom bepaalde mutaties leiden tot ziekten zoals staar.
Kanalen zien bewegen met cryo‑EM
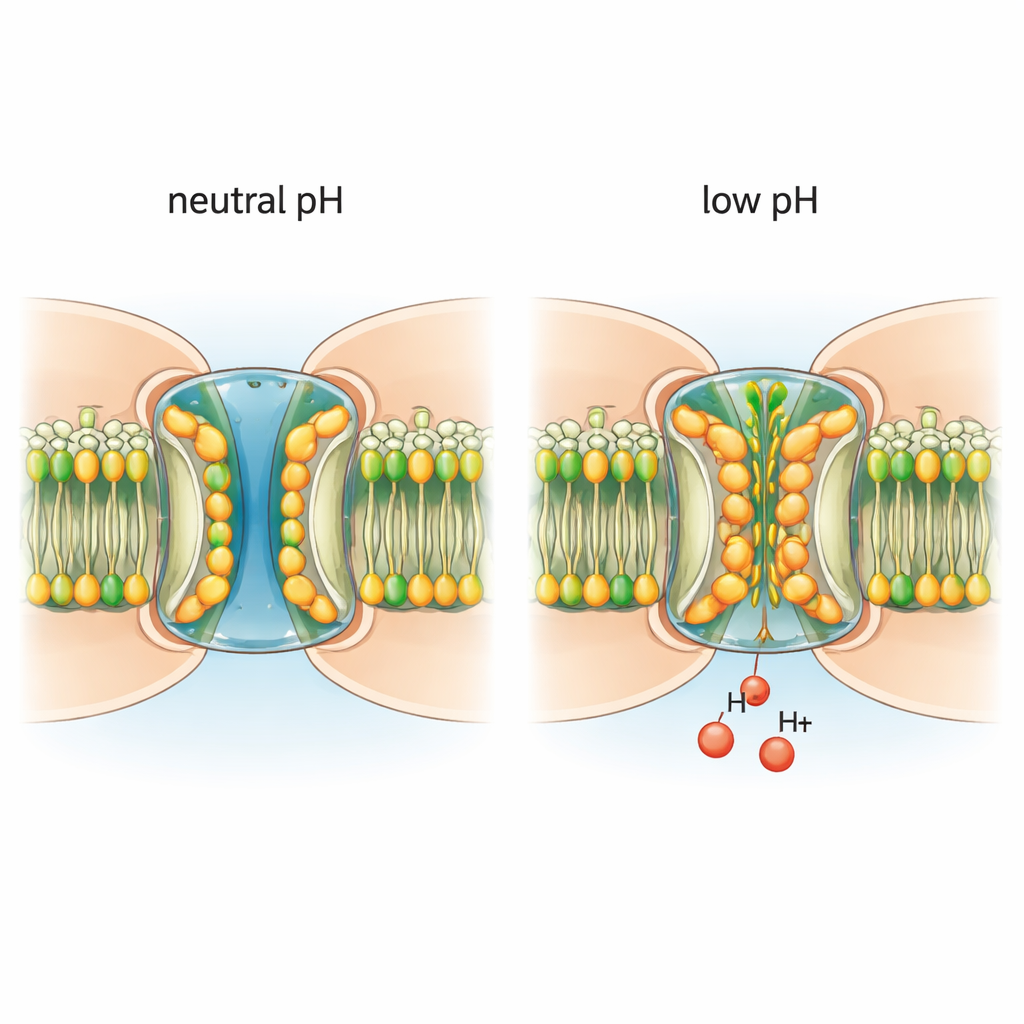
De onderzoekers zuiverden native connexine‑46/50‑kanalen uit oudere schapenlensen en plaatsten ze in een modelmembraan. Met cryo‑elektronenmicroscopie maakten ze beelden van de kanalen op bijna atomische resolutie onder neutrale omstandigheden, die een open porie bevorderen, en onder licht zure omstandigheden die schakeling veroorzaken. Bij neutrale pH nemen de kanalen grotendeels een stabiele open toestand aan, met een centrale tunnel breed genoeg voor ionen en kleine moleculen en met een flexibel segment, het N‑terminaal domein, dat de porie-ingang bekleedt. Onder deze omstandigheden is de porie schoon: geen extra moleculen blokkeren de doorgang en de omringende membraanlipiden blijven georganiseerd in regelmatige lagen.
Zuur trekt lipiden de porie in
Wanneer de omgeving licht zuur werd gemaakt, veranderde de architectuur van het kanaal op opvallende wijze. Lipidemoleculen uit het omringende membraan werden de porie ingetrokken en gleden tussen en onder de N‑terminale segmenten. Deze binnengedrongen lipiden vormen een tweeledig gelaagde hydrofobe “pakking” die de N‑terminale domeinen naar binnen duwt, waardoor het kanaal vernauwt en het transport deels geblokkeerd wordt. Extra lipiden klemmen zich tussen naburige eiwitsubunits bij hun interfaces en dienen blijkbaar als toegangswegen van het membraan naar de porie. Belangrijk is dat wanneer de kanalen in een detergentomgeving werden geplaatst die een echt lipidemembraan mist, lage pH deze structurele veranderingen niet langer induceerde. Dit toont aan dat echte lipiden geen passieve toeschouwers zijn: ze zijn vereiste partners in het pH‑schakelingsproces.
Een omkeerbare en fijn afgestemde veiligheidschakelaar
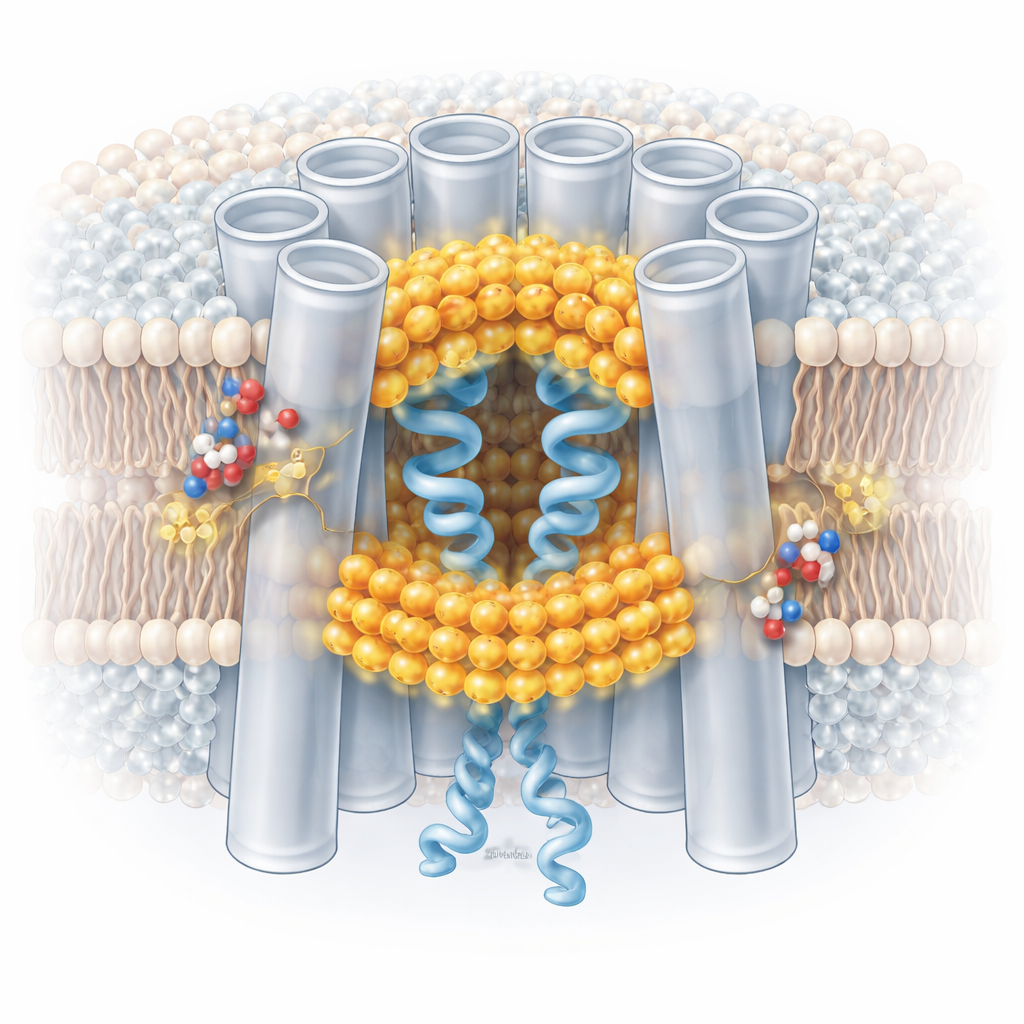
Door miljoenen individuele kanaaldeeltjes te volgen, vonden de auteurs dat lage pH niet simpelweg kanalen van volledig open naar volledig gesloten schakelt. In plaats daarvan verschuift het de populatie naar een mengeling van toestanden: sommige subunits binnen een kanaal tonen lipide‑gestabiliseerde, gesloten conformaties terwijl andere meer open blijven. Het schakelen is grotendeels niet‑coöperatief — elk bouwblok van het kanaal kan enigszins onafhankelijk reageren. Zure omstandigheden bevorderen deze gesloten conformaties, maar wanneer de pH weer neutraal wordt, trekken de porielipiden terug in het membraan en keren de kanalen terug naar de open toestand. Geconserveerde aminozuren genaamd histidines, die bij lage pH positieve lading krijgen, lijken te helpen bij het aantrekken en stabiliseren van de interfasciale lipiden die dit proces initiëren, wat een aannemelijke moleculaire pH‑sensor oplevert.
Implicaties voor staar en weefselbescherming
Deze resultaten ondersteunen een model waarbij lipiden fungeren als beweegbare pluggen die omkeerbaar de stroming door gap junctions regelen in reactie op zuurtegraad. In de ooglens kan zo’n mechanisme helpen beschadigde cellen te isoleren en voorkomen dat toxische signalen zich verspreiden, maar chronische of verkeerd geregelde schakeling kan ook bijdragen aan leeftijdsgebonden staarvorming. Omdat soortgelijke lipideintrusies zijn waargenomen in verwante kanaalfamilies, suggereert het werk een algemener principe: onder stress kunnen celmembranen zelf dynamische componenten leveren die vitale kanalen aan of uit zetten, wat nieuwe ideeën biedt voor medicijnen die de open of gesloten toestanden in ziekte stabiliseren.
Bronvermelding: Jarodsky, J.M., Myers, J.B. & Reichow, S.L. Reversible lipid-mediated pH-gating of connexin-46/50 by cryo-EM. Nat Commun 17, 1606 (2026). https://doi.org/10.1038/s41467-026-68311-9
Trefwoorden: gap junctions, connexine 46/50, pH‑schakeling, staar, cryo-EM