Clear Sky Science · nl
Dynamische single-cell-transcriptomics onthult lsamp-geleide neurale netwerkvorming in mannelijke S. japonicum die vrouwelijke reproductie aanstuurt
Waarom het liefdesleven van een parasiet ertoe doet
Schistosomiasis is een parasitaire ziekte die meer dan 250 miljoen mensen ziek maakt, vooral in armere regio’s met beperkte medische zorg. De ziekte wordt niet veroorzaakt door beten of toxines van de wormen, maar door de enorme aantallen eieren die vrouwelijke parasieten in het lichaam leggen. Verrassend genoeg kunnen vrouwelijke wormen alleen rijpen en beginnen met het leggen van eieren nadat ze gekoppeld zijn met een mannetje. Deze studie stelt een eenvoudige maar cruciale vraag: wat doet het mannetje precies om de vruchtbaarheid van het vrouwtje aan te zetten — en zou die schakel uitgeschakeld kunnen worden om de ziekte te stoppen?
Een verborgen wereld cel voor cel in kaart brengen
Om dit te onderzoeken, bouwden de onderzoekers een gedetailleerde “cellenatlas” van de bloedzuiger Schistosoma japonicum tijdens het sleutelvenster waarin mannetjes en vrouwtjes koppelen en seksueel volwassen worden. Met single-cell RNA-sequencing, een techniek die leest welke genen actief zijn in individuele cellen, analyseerden ze meer dan 100.000 cellen van wormen die op vier tijdstippen na infectie bij muizen waren verzameld. Ze identificeerden 76 verschillende celtypen, waaronder vele soorten zenuwcellen, stamcellen en voortplantingscellen. Dit stelde hen in staat te volgen hoe specifieke celpopulaties uitbreiden, krimpen of van identiteit veranderen terwijl de wormen groeien en beginnen te reproduceren.
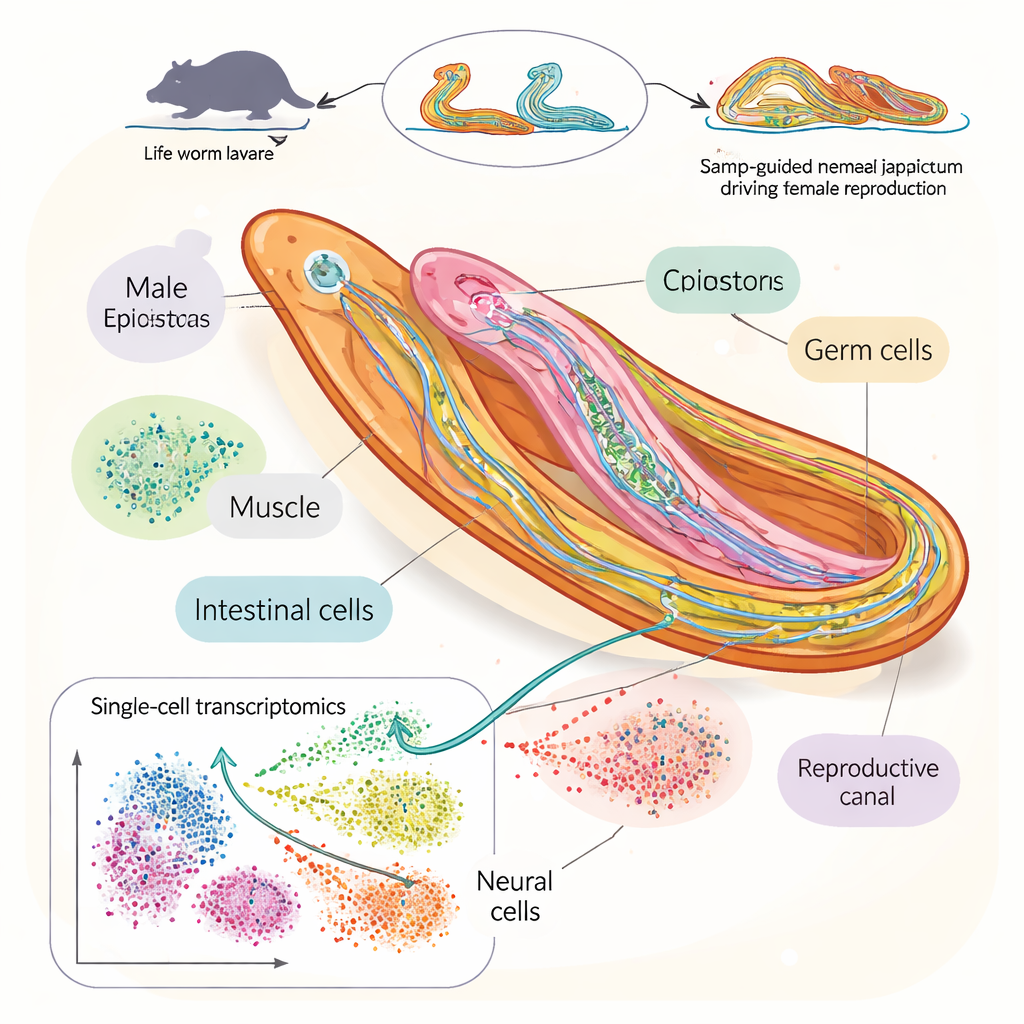
De opkomst van eieren en sperma volgen
Door in te zoomen op cellen uit de testes, ovaria en gerelateerde weefsels reconstrueerde het team de stapsgewijze ontwikkeling van sperma en eieren. Ze toonden aan hoe kiemlijn-stamcellen uitmonden in laatstadium sperma- en eicellen via onderscheiden genactiviteitsprogramma’s bij mannetjes en vrouwtjes. Bij vrouwtjes leggen de genen die eiergroei ondersteunen de nadruk op eiwitproductie en -verpakking, terwijl bij mannetjes de nadruk meer ligt op structuren zoals cilia en microtubuli die sperma helpen bewegen. De studie bracht ook in kaart hoe het omvangrijke eierondersteunende orgaan bij vrouwtjes, de vitellaria, zich ontwikkelt via tussenstadia, en identificeerde nieuwe genetische markers die laten zien hoe volwassen elk voortplantingsweefsel is.
Een alleen-mannelijk zenuwcircuit in een klemkanaal
Een van de meest opvallende ontdekkingen kwam uit het zenuwstelsel. In plaats van een losse verzameling zenuwcellen onthulde de atlas vijf duidelijke neuronale lijnen, waaronder meerdere die verschilden tussen mannetjes en vrouwtjes. Drie type neuronen — genoemd N2.2, N3.2 en N4.3 — waren sterk verrijkt in mannetjes en clusteren binnen het gynecophorale kanaal, een gespecialiseerde groef die het mannetje gebruikt om het vrouwtje te ‘klemmen’. Onder deze cellen vielen de N4.3-neuronen op omdat ze een gen tot expressie brachten dat nrps heet, dat het enzym produceert dat BATT maakt, een klein peptide-feromoon dat eerder is aangetoond vrouwelijke seksuele ontwikkeling te stimuleren. Met andere woorden: deze N4.3-cellen fungeren als de ‘signaalstations’ van het mannetje om de vruchtbaarheid van het vrouwtje aan te zetten.
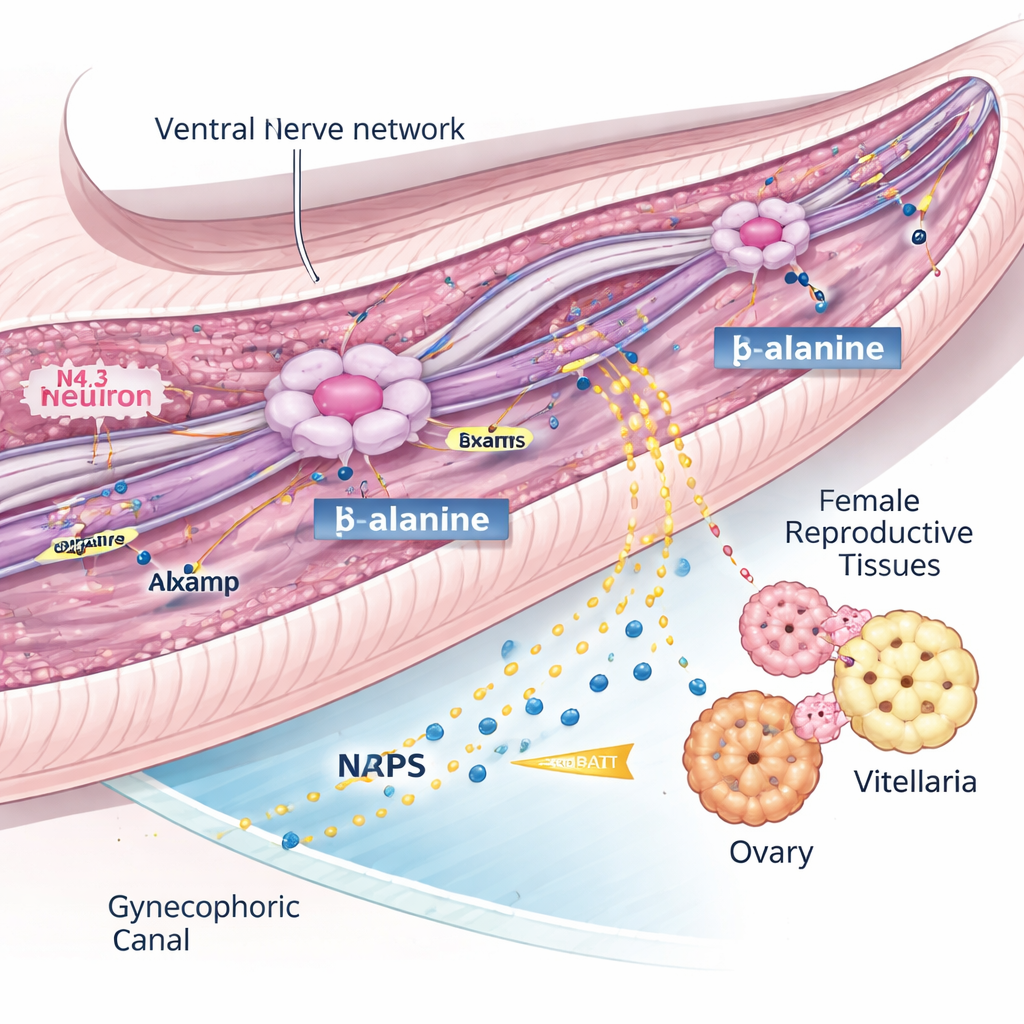
Een geleidemolecuul dat het signaal in stand houdt
Om te begrijpen hoe deze N4.3-neuronen werken, zochten de onderzoekers naar genen die hun ontwikkeling en functie lijken te sturen. Ze richtten zich op lsamp, een gen dat bij andere dieren bekendstaat om zenuwcellen te helpen verbinden en axonen te onderhouden. In mannelijke schistosomen stond lsamp aan in dezelfde N4.3-neuronen die het BATT-enzym maken, en de activiteit nam sterk toe naarmate de wormen volwassen werden. Door RNA-interferentie te gebruiken om lsamp bij mannetjes te verminderen, vonden ze dat gekoppelde vrouwtjes hun ovaria en vitellaria niet volledig ontwikkelden en vrijwel geen eieren legden. Toch waren de N4.3-neuronen nog aanwezig, het nrps-gen bleef actief en de ruwe chemische bouwstenen voor BATT waren onveranderd. In plaats daarvan vertoonden lsamp-deficiënte mannetjes beschadigde zenuwvezels en verstoord transport van vesikels langs gestabiliseerde microtubuli, en produceerden ze veel minder BATT binnen hun lichaam en in het omringende medium. Dit suggereert dat lsamp cruciaal is voor het behouden van een ventraal zenuwnetwerk dat een belangrijk voorloper levert, waarschijnlijk β-alanine, aan N4.3-neuronen zodat zij genoeg feromoon kunnen synthetiseren om het vrouwtje te activeren.
De reproductieschakelaar dimmen
Voor niet-specialisten is de kernboodschap dat het vermogen van deze parasiet om ziekte te veroorzaken afhangt van een intiem ‘gesprek’ tussen mannelijke en vrouwelijke wormen, gevoerd via een gespecialiseerd zenuwnetwerk en een klein feromoon. De studie toont dat een enkel geleidemolecuul, lsamp, helpt bij het bouwen en onderhouden van de ventrale zenuwbebouwing van het mannetje; wanneer die bedrading faalt, kan het mannetje geen sterk genoeg chemisch signaal meer uitzenden om de voortplantingsorganen van het vrouwtje volledig te laten rijpen, en daalt de eiproductie scherp. Door de cellen van de parasiet op hoge resolutie in kaart te brengen en dit alleen-mannelijke neurale circuit te onthullen, wijst het werk op nieuwe manieren om eiproductie te blokkeren — wat een potentiële strategie biedt om schistosomiasis te beteugelen waar de huidige behandeling afhankelijk is van slechts één verouderend geneesmiddel.
Bronvermelding: You, Y., Cheng, S., Chen, X. et al. Dynamic single-cell transcriptomics reveals lsamp-guided neural network formation in male S. japonicum driving female reproduction. Nat Commun 17, 1602 (2026). https://doi.org/10.1038/s41467-026-68305-7
Trefwoorden: schistosomiasis, single-cell-transcriptomics, parasitaire voortplanting, neurale circuits, feromoonsignalisatie