Clear Sky Science · nl
Mechanisme van SARS‑CoV‑2‑resistentie tegen antivirale middelen op basis van nucleotideanalogen
Hoe het virus belangrijke antivirale middelen te slim af is
Het COVID‑19‑virus behoort tot een zeldzame groep RNA‑virussen die hun genetisch materiaal kunnen proeflezen, waardoor ze uitzonderlijk goed bestand zijn tegen sommige van onze beste antivirale middelen. Deze studie gaat in op de atomaire details van hoe SARS‑CoV‑2 een veelgebruikte klasse geneesmiddelen, nucleotideanalogen, detecteert en verwijdert, en verklaart waarom middelen die goed werken tegen andere virussen vaak minder effectief zijn bij coronavirusinfecties.
Een touwtrekwedstrijd rond het virale RNA
SARS‑CoV‑2 kopieert zijn ongeveer 30.000 letters tellende RNA‑genoom met een groot moleculair apparaat dat het replicatie‑transcriptiecomplex wordt genoemd. Centraal staat de RNA‑afhankelijke RNA‑polymerase (RdRp), die nieuwe RNA‑strengen bouwt, en een aparte eenheid, de exonuclease (ExoN), die fouten proefleest en wegsnijdt. Veel antivirale tabletten, waaronder middelen die oorspronkelijk voor hepatitis C zijn ontwikkeld, bootsen de natuurlijke RNA‑bouwstenen voldoende nauwkeurig na om door RdRp te worden ingebouwd, maar hebben subtiele aanpassingen die het kopiëren doen stokken of fouten introduceren. Helaas beschikken coronavirussen over ExoN, dat deze bedriegers kan herkennen zodra ze in de RNA‑keten zitten en ze eruit kan knippen, waardoor de virale replicatie gered wordt.
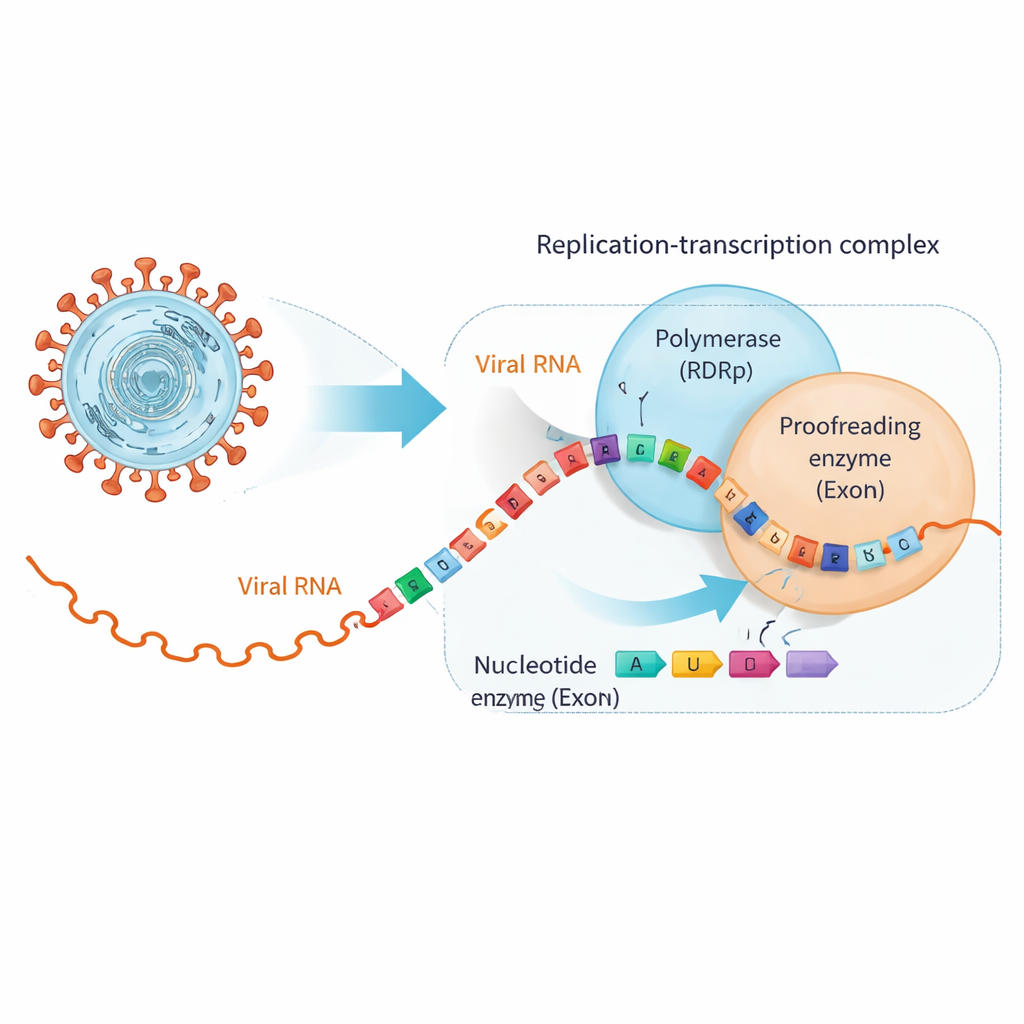
Als nuttige middelen het RNA van partner doen wisselen
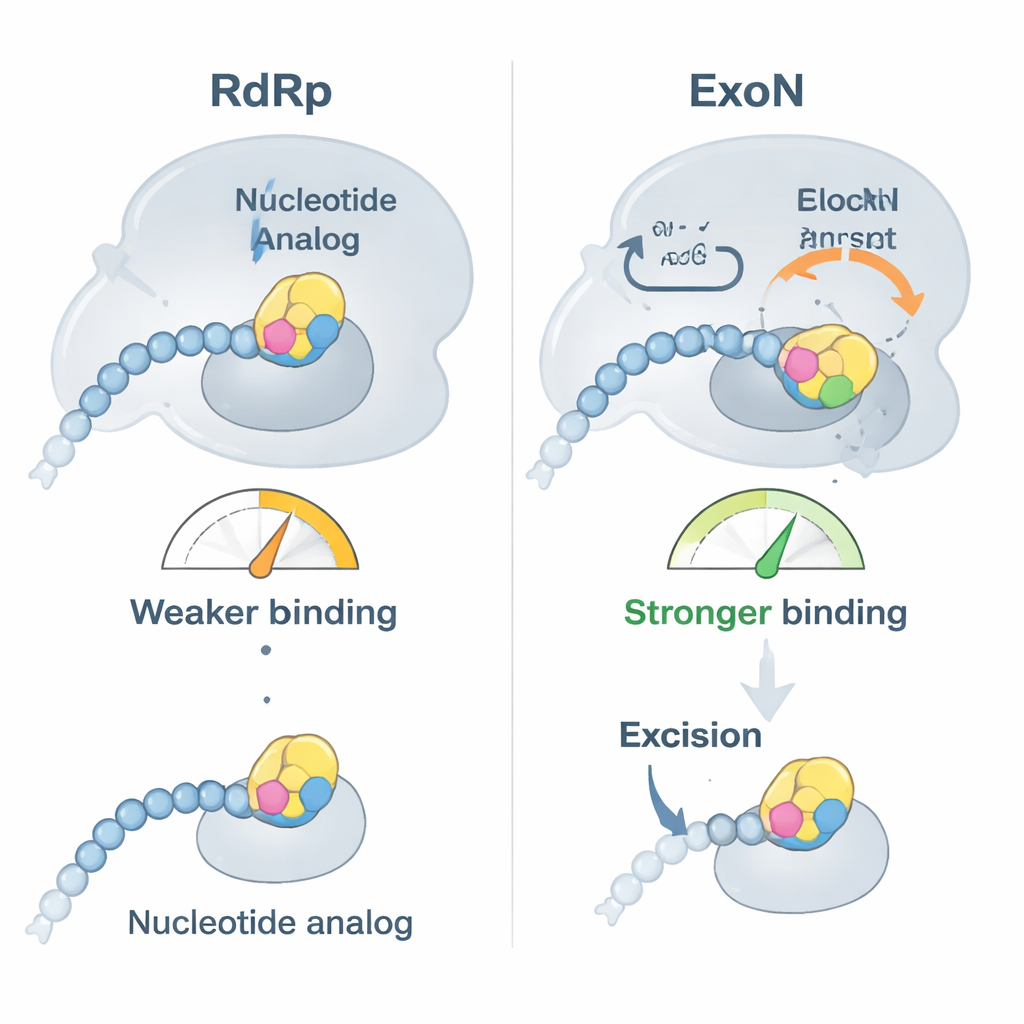
De onderzoekers richtten zich op twee klinisch belangrijke antivirale middelen, bemnifosbuvir en sofosbuvir, die beide zijn ontworpen om als gebrekkige RNA‑bouwstenen te fungeren. Eerst toonden ze aan dat de polymerase van SARS‑CoV‑2 deze analogen gemakkelijk aan het uiteinde van een RNA‑streng invoegt en daarna grotendeels stopt met het verlengen van de keten, zoals bedoeld. Bindingstests onthulden echter een onverwachte wending: zodra een analoog aan de punt van het RNA zit, hecht het RNA niet langer zo stevig aan de polymerase maar bindt het juist sterker aan ExoN. In feite wordt het door het medicijn gewijzigde RNA weggeduwd van de kopieermachine en overgedragen aan de proeflezer, die vervolgens de kans krijgt het problematische nucleotide af te knippen en de replicatie te laten doorgaan.
Proeflezen dat vertraagt maar niet stopt
Biochemische tijdsverloopexperimenten lieten zien dat ExoN bemnifosbuvir en sofosbuvir wel degelijk uit RNA verwijdert, maar langzamer dan normale nucleotiden. In celvrije reacties blokkeerden beide analogen de verdere RNA‑synthese sterk — toch werd, wanneer een actieve ExoN werd toegevoegd, een aanzienlijk deel van de vastgelopen RNA‑ketens gered en verlengd. Een uitgeschakelde ExoN‑mutant kon dit niet, wat bevestigt dat de proefleesactiviteit verantwoordelijk is voor het ongedaan maken van een groot deel van het effect van de geneesmiddelen. De aanwezigheid van polymerase samen met ExoN versnelde zelfs het verwijderen van de analogen, wat suggereert dat de twee virale enzymen samenwerken om obstakels op te ruimen en de replicatie gaande te houden.
De proeflezer bekijken op atomaire resolutie
Om te begrijpen hoe ExoN deze middelen herkent en erop reageert, gebruikte het team cryo‑elektronenmicroscopie met hoge resolutie om structuren van het ExoN‑complex op te lossen dat gebonden is aan RNA‑strengen die eindigen in ofwel bemnifosbuvir of sofosbuvir. Deze structuren, scherp genoeg om individuele chemische groepen te zien, onthulden dat de gewijzigde suikerring van elk medicijn in een hydrofobe pocket past die wordt gevormd door een korte lus van het ExoN‑eiwit. Deze extra strakke passing verklaart de sterkere binding van medicijnhoudend RNA aan ExoN. Maar het heeft ook een onverwacht neveneffect: door aan die lus te trekken, verstoren de middelen de precieze opstelling van een nabijgelegen katalytische lus die een sleutelhistidine op zijn plaats houdt. Wanneer deze histidine wegschuift van het knipgebied, wordt het actieve centrum van ExoN gedeeltelijk gedeactiveerd, waardoor het uitknippen van de analoog vertraagt maar niet volledig wordt voorkomen.
Een ingebouwde schakelaar die het virale proeflezen afstemt
Het muteren van individuele aminozuren in de gevoelige lus bevestigde het belang ervan. Veranderingen in vier geconserveerde residuen verminderden sterk het vermogen van ExoN om zowel standaard RNA‑einden als medicijn‑geëindigde einden te knippen, en veranderden ook welke laatste nucleotide ExoN het liefst verwijdert. Dit identificeert de lus als een allosterische regulator — een ingebouwde mechanische schakelaar die aangeeft welk type nucleotide aan de RNA‑punt zit en de activiteit van het enzym afstemt. De structuren laten verder zien dat ExoN verschillende basen (A, U, C of G) herkent via flexibele waterstofbindingen, maar het moeilijkst heeft met guanineachtige basen, wat relevant is omdat bemnifosbuvir guanosine nabootst.
Wat dit betekent voor toekomstige COVID‑19‑middelen
Voor niet‑specialisten is de kernboodschap dat SARS‑CoV‑2 een geraffineerde "spell‑checker" draagt die bepaalde middelen uit zijn genoom kan trekken nadat ze hun werk, het stilleggen van replicatie, hebben gedaan. Bemnifosbuvir en sofosbuvir verzwakken weliswaar de kopieermachine van het virus, maar sturen het RNA tegelijkertijd naar de proeflezer die een deel van hun effect kan ongedaan maken. Door precies te onthullen hoe de virale proeflezer deze middelen grijpt en hoe een kleine regelende lus het enzym schakelt tussen actieve en minder actieve toestanden, biedt dit werk een stappenplan voor het ontwerpen van nieuwe antivirale nucleotiden die ofwel slecht aan ExoN binden, het in een inactieve conformatie vergrendelen, of gebruikmaken van zijn moeilijkheid om met guanineachtige structuren om te gaan. Dergelijke volgende generatie moleculen zouden veel moeilijker voor het virus te "wissen" kunnen zijn en onze mogelijkheden om COVID‑19 en toekomstige coronavirusuitbraken te behandelen verbeteren.
Bronvermelding: Liu, C., Li, Y., Cao, X. et al. Mechanism of SARS-CoV-2 resistance to nucleotide analog-based antivirals. Nat Commun 17, 1601 (2026). https://doi.org/10.1038/s41467-026-68304-8
Trefwoorden: SARS‑CoV‑2, antivirale resistentie, nucleotideanalogen, RNA‑correctie, replicatie van coronavirussen