Clear Sky Science · nl
Geïntegreerde multi-omische atlas onthult de hiërarchie van ruimtelijk-temporele regulerende netwerken tijdens muis-gastrulatie
Hoe een embryo zijn lichaamsplan opbouwt
Elk zoogdier, inclusief de mens, begint het leven als een klein bolletje cellen dat zich snel moet organiseren tot een complex lichaam met een kop, staart, rug, buik en inwendige organen. Deze ingrijpende hervorming vindt plaats tijdens een korte periode die gastrulatie wordt genoemd. Het hier samengevatte artikel bouwt een gedetailleerde, meerlagige kaart van dit proces in muisembryo’s en laat zien hoe genen, DNA-schakelaars en chemische signalen samen in ruimte en tijd werken om cellen naar hun toekomstige bestemmingen te leiden.
Duizenden cellen zien hun keuzes maken
Om gastrulatie in actie te volgen, analyseerden de onderzoekers meer dan 35.000 afzonderlijke cellen uit muisembryo’s over vijf nauw opeenvolgende stadia, van vroege tot late gastrulatie. Voor elke cel bepaalden ze niet alleen welke genen actief waren, maar ook welke DNA-streken open en toegankelijk waren — een teken dat ze als regulerende schakelaars kunnen fungeren. Met deze gegevens identificeerden ze 31 verschillende celtypes en volgden hoe vroege, flexibele cellen zich stapsgewijs vertakken naar de drie hoofdkiemlagen — ectoderm, mesoderm en endoderm — die uiteindelijk alle weefsels en organen vormen. Ze ontwikkelden ook een nieuwe computationele methode, BioCRE, om genen nauwkeuriger te koppelen aan hun controlerende DNA-elementen, wat onthulde dat veel belangrijke schakelaars ver van de genen die ze reguleren kunnen liggen.
Een driedimensionale moleculaire atlas bouwen in echte embryoruimte
De meeste single-cell methoden verliezen de oorspronkelijke positie van elke cel in het embryo, terwijl locatie cruciaal is om patroonvorming te begrijpen. Het team loste dit op door hun single-cell gegevens uit te lijnen op een bestaande driedimensionale kaart van genactiviteit in muisembryo’s. Het resultaat is ST-MAGIC, een “digitaal embryo” waarin elke kleine locatie is geannoteerd met de waarschijnlijke celtypes, de genen die ze tot expressie brengen en de toegankelijkheid van het omringende DNA. Deze atlas toont bijvoorbeeld hoe verschillende mesoderm-subtypen — toekomstige hart-, spier- en ondersteunende weefsels — ontstaan in onderscheidende regio’s en hoe wijdverspreid uitgedrukte genen zoals Otx2 verschillende regulatoire elementen gebruiken aan de buitenzijde (epiblast) en binnenzijde (visceral endoderm) van het embryo.
Wanneer symmetrie breekt en links anders wordt dan rechts
Een opvallend kenmerk van lichaamsplannen is dat linker- en rechterzijde niet identiek zijn — denk aan het hart dat iets naar links zit. De auteurs gebruikten hun ruimtelijke atlas om in te zoomen op het laterale mesoderm, waar links-rechts verschillen eerst verschijnen. Ze vonden subtiele maar consistente asymmetrieën in welke celtypes aan elke kant verrijkt zijn en welke DNA-regio’s meer open zijn. Aan de rechterzijde waren regio’s gekoppeld aan een groeisignaalroute genaamd BMP toegankelijker; aan de linkerzijde waren regio’s geassocieerd met genen die nodig zijn voor segmentvorming en hartstructuren meer in het voordeel. Sommige van deze DNA-elementen, waaronder nieuw ontdekte elementen die het gen Lefty2 reguleren, worden geopend voordat zichtbare genexpressieverschillen ontstaan, wat suggereert dat vroege “primering” van het chromatine-landschap elke zijde van het embryo voorbereidt om signalen anders te interpreteren.
Een estafette van factoren stuurt de middellijn van het lichaam
De studie richt zich vervolgens op het axiale mesendoderm, een populatie cellen die de notochord zal vormen — een staafvormige structuur langs de middellijn die helpt de wervelkolom en het zenuwstelsel te organiseren. Met hun gecombineerde hulpmiddelen (ST-MAGIC en een uitgebreide versie genaamd ST-MAGIC (+)) volgden de auteurs hoe deze cellen ontstaan uit de anterior primitive streak en zich opsplitsen in twee takken: node-cellen, die een gecilieerde structuur opbouwen die belangrijk is voor links-rechts waarneming, en anterior mesendoderm, dat bijdraagt aan middellijnweefsels. Ze onthulden een hiërarchische estafette van transcriptiefactoren — eiwitten die genactiviteit regelen. Vroege factoren, zoals EOMES, en tussenliggende factoren, waaronder FOXA2 en LHX1, openen eerst sleutelregio’s van DNA en vestigen responsiviteit voor belangrijke signalen zoals WNT en NODAL. Later schakelen “terminerende” factoren zoals NOTO, SOX9 en een nieuw betrokken factor POU6F1 gespecialiseerde genprogramma’s aan, bijvoorbeeld die nodig zijn voor cilia of extracellulaire matrix.
Signalen, chromatine en laatwerkende specialisten
Door openbare datasets te integreren over waar WNT- en NODAL-signaaleffectoren aan DNA binden, toonden de auteurs aan dat de responsiviteit van het embryo op deze signalen ruimtelijk verschuift voordat de signaalbronnen zelf bewegen. In de regio die geprimed is om axiaal mesendoderm te worden, openen DNA-sites die gevoelig zijn voor NODAL en WNT vroeg, en velen bevatten motieven voor FOXA2, Zfp281 en andere regulatoren, wat wijst op gezamenlijke controle. Experimentele verwijdering van laatwerkende factoren NOTO en POU6F1 in muizen verstoorde de expressie van node-specifieke en cilia-gerelateerde genen en verkortte de node-cilia, terwijl het onderliggende open DNA-landschap grotendeels intact bleef. Dit duidt erop dat vroegere factoren het epigenetische fundament leggen, terwijl late factoren vooral de genexpressie verfijnen zonder het chromatine grootschalig te herstructureren.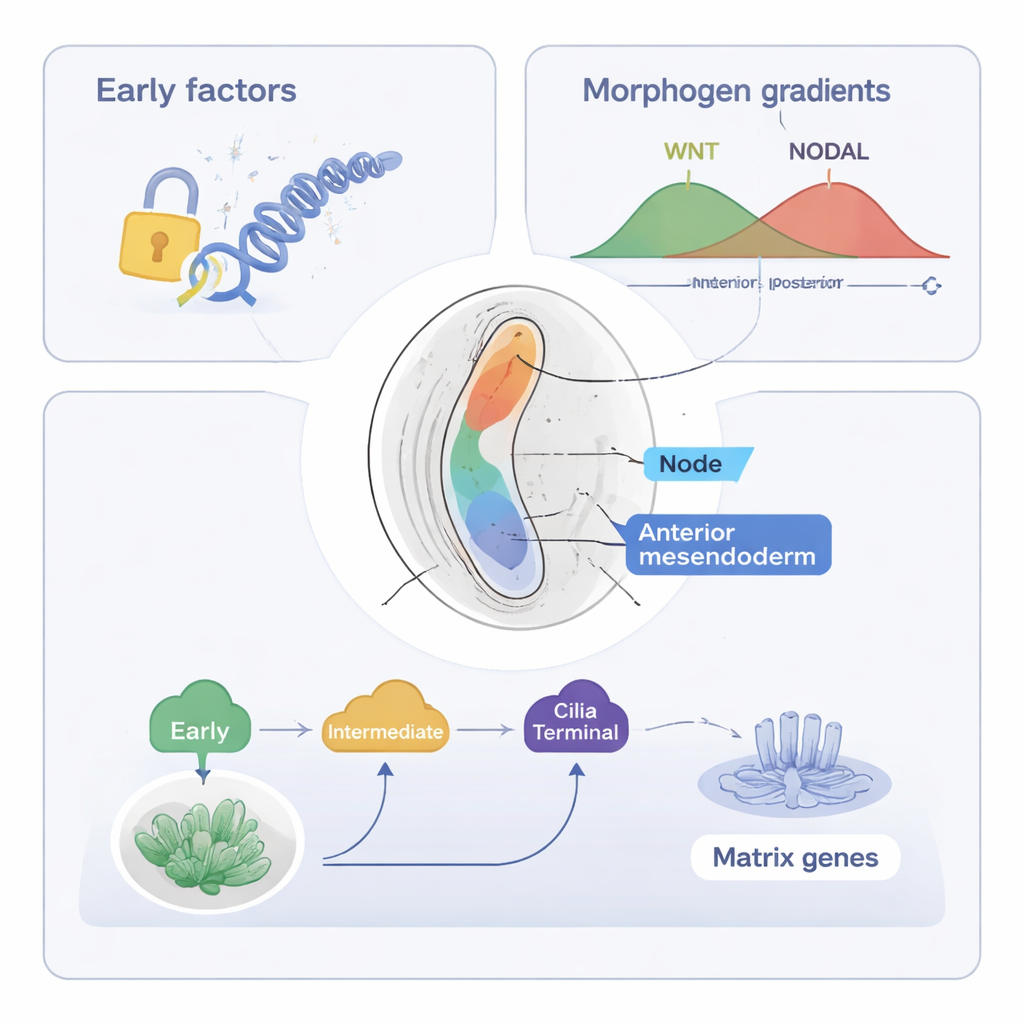
Waarom dit belangrijk is voor het begrip van ontwikkeling
Voor niet-specialisten kan dit werk worden gezien als het bouwen van een hoogresolutie “bedradingsschema” van hoe een embryo zijn lichaamsplan uitzet. De auteurs laten zien dat celbestemmingsbeslissingen tijdens gastrulatie niet alleen worden bepaald door welke signalen aanwezig zijn, maar ook door wanneer en waar DNA-schakelaars worden geopend en welke transcriptiefactoren in opvolging werken. Hun ST-MAGIC en ST-MAGIC (+) atlassen bieden een bron om deze relaties in ruimte en tijd te verkennen en vormen een kader dat studies naar aangeboren afwijkingen, stamcelgebaseerde embryo-modellen en uiteindelijk aspecten van menselijke ontwikkeling kan informeren.
Bronvermelding: Yang, X., Xie, B., Shen, P. et al. Integrated multi-omic atlas reveals the hierarchy of spatiotemporal regulatory networks of mouse gastrulation. Nat Commun 17, 1572 (2026). https://doi.org/10.1038/s41467-026-68291-w
Trefwoorden: gastrulatie, genregulatie-netwerken, single-cell multi-omics, embryonale patroonvorming, muisontwikkeling