Clear Sky Science · nl
De novo-varianten in het splicingfactor-gen SF3B1 zijn geassocieerd met neuro-ontwikkelingsstoornissen
Wanneer één gen het vroege bouwplan van de hersenen verstoort
Waarom ontwikkelen sommige kinderen leerproblemen, epilepsie of voedingsproblemen terwijl zwangerschap en geboorte normaal lijken te verlopen? Deze studie onderzoekt één gen, SF3B1 geheten, dat cellen helpt genetische boodschappen te verwerken. De onderzoekers tonen aan dat nieuwe, spontane veranderingen in dit gen subtiel kunnen verstoren hoe hersencellen DNA-instructies lezen, wat leidt tot een eerder niet-erkend neuro-ontwikkelingssyndroom.
Een meesterredacteur van genetische boodschappen
Elke cel in ons lichaam moet rauwe genetische tekst omzetten in heldere instructies voordat ze eiwitten kan maken. Deze bewerkingsstap, bekend als RNA-splicing, verwijdert niet-coderende segmenten en naait de bruikbare delen aan elkaar. SF3B1 is een centraal onderdeel van het cellulaire "splicingmachinaal." Tot nu toe stonden veranderingen in SF3B1 vooral bekend vanwege hun rol bij kanker, waar tumorcellen tijdens het leven mutaties in dit gen verwerven. Het nieuwe werk stelt een andere vraag: wat gebeurt er wanneer een schadelijke verandering in SF3B1 vanaf de conceptie in elke cel van het lichaam aanwezig is?
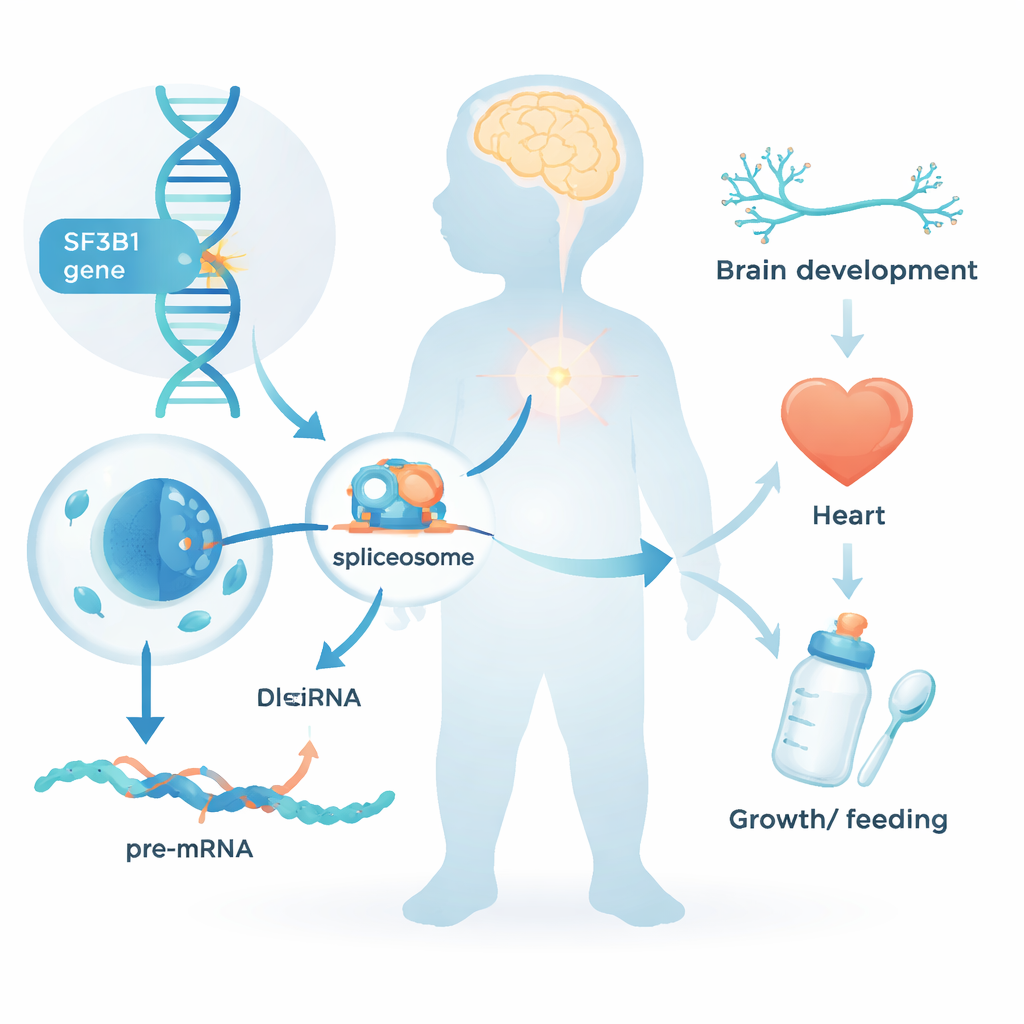
Een recent herkend kindersyndroom
Het team verzamelde gegevens van 26 kinderen en jongvolwassenen die allemaal zeldzame SF3B1-varianten droegen, meestal de novo ontstaan — dat wil zeggen niet geërfd van een van de ouders. Bij bijna allen deden zich neuro-ontwikkelingsproblemen voor: achterstanden bij het leren zitten, lopen of praten; een verstandelijke beperking die meestal mild tot matig was; en bij ongeveer de helft van de gevallen epileptische aanvallen. Velen hadden een lage spierspanning en hadden extra hulp bij voeden nodig, soms via een maagsonde. De gelaatskenmerken waren subtiel afwijkend maar niet identiek per kind; een opvallend vaak voorkomend kenmerk was een hoog gehemelte of gespleten gehemelte. Verschillende deelnemers hadden ook hartafwijkingen, groeibeperkingen of een kleine hoofdomvang, wat laat zien dat de impact van SF3B1-veranderingen verder reikt dan alleen de hersenen.
Twee klassen van genetische veranderingen, twee klinische patronen
De onderzoekers maakten onderscheid tussen twee brede types SF3B1-varianten. De ene groep omvatte "loss-of-function"-veranderingen, zoals voortijdige stopcodons, waarvan wordt verwacht dat ze de hoeveelheid functioneel SF3B1-eiwit verminderen. De tweede groep bevatte missense-varianten, waarbij één aminozuur in het eiwit is gewijzigd. Door de medische kenmerken van de kinderen te clusteren, zagen de onderzoekers dat degenen met missense-varianten doorgaans ernstiger en complexere problemen hadden, waaronder een hoger voorkomen van hart- en gastro-intestinale afwijkingen, korte lengte en microcefalie. Loss-of-function-varianten daarentegen werden soms geërfd van een licht aangedane of zelfs ogenschijnlijk gezonde ouder, wat suggereert dat minder SF3B1 hebben in sommige individuen samengaat met relatief milde symptomen.
Fijn-afstemmingsfouten in plaats van een volledige uitval
Om te begrijpen wat de missense-varianten in cellen doen, reconstrueerden de wetenschappers ze in laboratoriumcellijnen. Tot hun verrassing konden deze gewijzigde SF3B1-eiwitten nog steeds de basisfunctie van splicing voldoende uitvoeren om cellen te redden waarin normaal SF3B1 was uitgeschakeld. Dat sloot een eenvoudige loss-of-function-uitleg uit. Met diepe RNA-sequencing bekeek het team vervolgens het volledige repertoire aan cellulaire boodschappen. Ze vonden dat missense-varianten de splicing van honderden genen subtiel verschoven, vooral door te veranderen welke splice-sites aan de uiteinden van exons werden gekozen en door incidenteel exon-skippen te veroorzaken. De omvang van de verstoring was kleiner dan die gezien bij de klassieke kanker-geassocieerde SF3B1-mutatie K700E, maar nog steeds aanzienlijk: veel getroffen genen zijn betrokken bij hersenontwikkeling, zenuwbedrading en fundamentele processen zoals RNA-verwerking en eiwitsynthese.
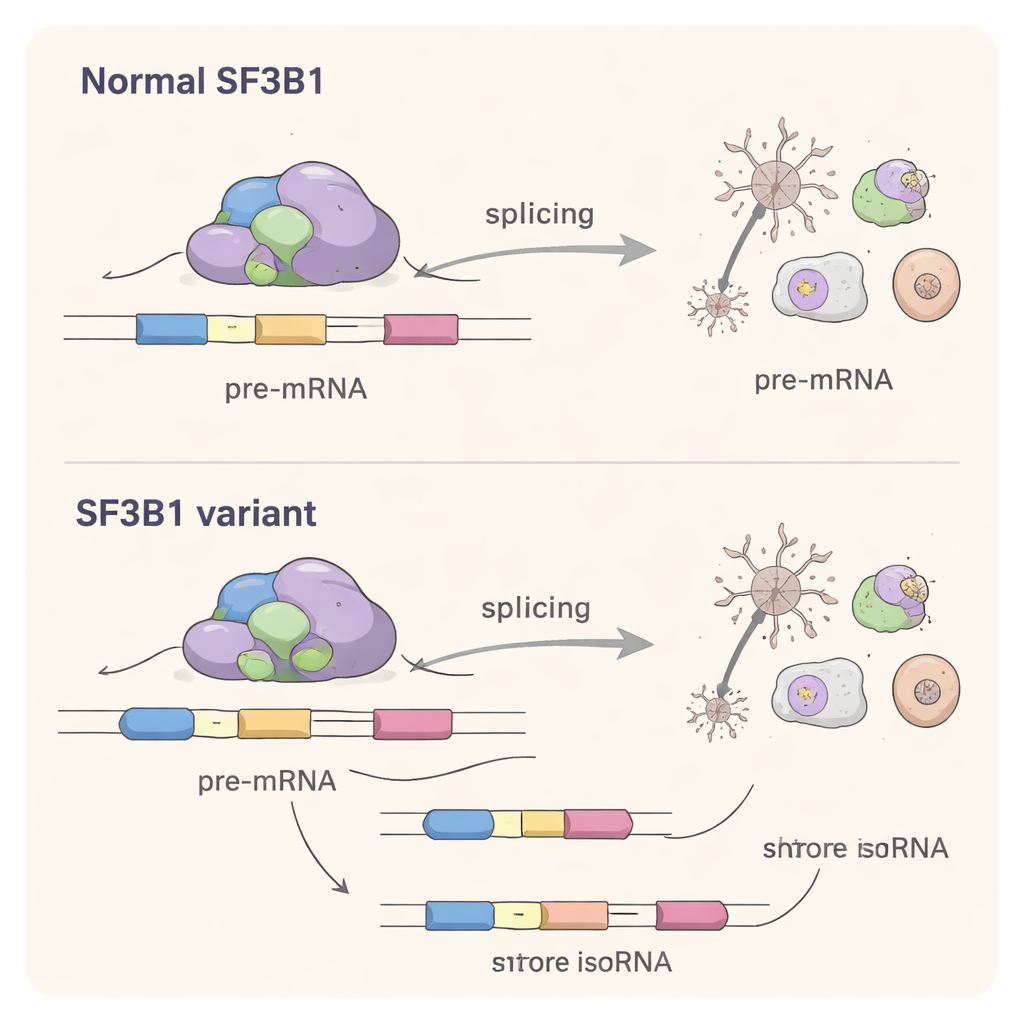
Een gedeeld mechanisme tussen kanker en hersenaandoeningen
Hoewel de meeste neuro-ontwikkelings-SF3B1-varianten op andere posities voorkomen dan de bekende kankermutaties, verstoren ze hetzelfde kernproces: de precieze herkenning van splice-sites in RNA. De studie toont aan dat deze ontwikkelingsvarianten hun eigen "splicingsignatuur" hebben, waarbij ze alternatieve splice-sites kiezen die vaak dichter bij de normale liggen dan die welke in kanker worden bevoordeeld. Dit wijst op een change-of-function-mechanisme, waarbij het gemuteerde eiwit concurreert met de normale kopie en het splicingmachinerie subtiel naar net verkeerde keuzes in veel genen tegelijk stuurt.
Wat dit betekent voor families en toekomstig onderzoek
Voor getroffen families identificeert het werk SF3B1 als een nieuwe oorzaak van neuro-ontwikkelingsstoornissen die nu in genetische klinieken getest kan worden, wat langdurige diagnostische zoektochten kan beëindigen. Breder gezien voegt het SF3B1 toe aan een kleine maar groeiende lijst van splicinggenen waarvan afwijkingen zowel kanker als kinderhersenaandoeningen kunnen aandrijven, afhankelijk van wanneer en hoe het gen verandert. Door in kaart te brengen hoe specifieke SF3B1-varianten RNA-splicing hervormen, legt de studie de basis voor toekomstige therapieën gericht op het herstellen van mis-splicing op gerichte wijze.
Bronvermelding: Uguen, K., Bergot, T., Scott-Boyer, MP. et al. De novo variants in the splicing factor gene SF3B1 are associated with neurodevelopmental disorders. Nat Commun 17, 1569 (2026). https://doi.org/10.1038/s41467-026-68284-9
Trefwoorden: RNA-splicing, SF3B1, neuro-ontwikkelingsstoornissen, de novo-varianten, spliceosomopathieën