Clear Sky Science · nl
Visco-elastische hydrogel voorbereide CAR-macrofagen voor de behandeling van longfibrose
De schoonmakers van het lichaam omscholen tot precisiereparatieteams
Longfibrose is een verwoestende longaandoening waarbij het normale, veerkrachtige longweefsel geleidelijk wordt vervangen door stijf littekenweefsel. Mensen krijgen moeite met ademen, en de huidige medicijnen vertragen meestal alleen het verval. Deze studie onderzoekt een nieuw idee: de eigen opruimcellen van het lichaam, macrofagen, omvormen tot geprogrammeerde “slimme schoonmakers” en hun kracht versterken met een speciaal ontworpen zachte gel. Samen helpen deze benaderingen de cellen de littekenvormende veroorzakers op te sporen en zelfs het verharde weefsel in beschadigde longen losser te maken.
Wanneer genezing schadelijk wordt
In gezonde longen helpen fibroblasten het fijne netwerk van collageen te onderhouden dat de luchtzakjes ondersteunt. Bij longfibrose worden deze cellen overactief en leggen ze dikke bundels collageen neer die de luchtwegen dichtknijpen. Bestaande medicijnen kunnen deze processen dempen maar keren ze zelden om. De auteurs richten zich op een celoppervlaktekenmerk genaamd fibroblast activatie-eiwit (FAP), dat overvloedig aanwezig is op overactieve fibroblasten maar schaars in normaal weefsel. Als immuuncellen kunnen worden getraind om FAP te herkennen, zouden ze selectief de “doorgeslagen” fibroblasten die littekenvorming aansturen kunnen verwijderen, terwijl gezonde buren gespaard blijven.
Macrofagen herprogrammeren om littekenbouwers aan te pakken
Macrofagen zijn rondzwervende immuuncellen die normaal gesproken dode cellen, microben en celresten opnemen. Het team voorzag ze van een chimere antigeenreceptor (CAR) die FAP herkent, waardoor CAR-macrofagen (CAR-Ms) ontstonden. In kweek schrokken deze CAR-Ms FAP-rijke fibroblasten efficiënt op en doodden ze, terwijl ze grotendeels cellen met verminderd FAP negeerden. Ze knaagden ook steviger door collageenrijke gels dan niet-gemodificeerde macrofagen, wat wijst op een dubbel voordeel: het verwijderen van de cellen die litteken vormen en het direct afbreken van de littekenmatrix zelf. Deze effecten traden zowel op in standaard cellijnen als in primaire muismacrofagen, die dichter bij de echte situatie in weefsels liggen. 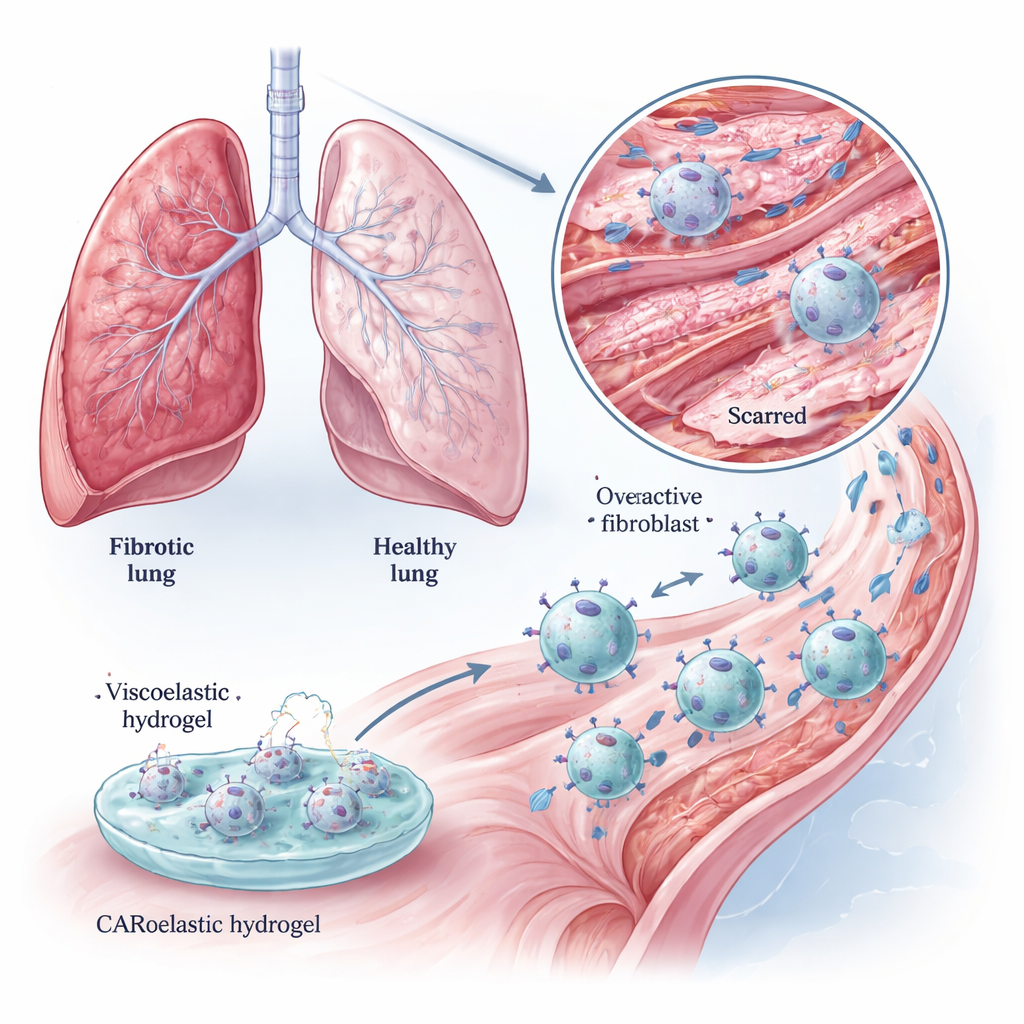
Immuuncellen voorbereiden met een zachte, visco-elastische gel
Genetisch ingrijpen in cellen is krachtig maar complex. De onderzoekers vroegen zich daarom af of een puur fysische prikkel — een zachte, visco-elastische hydrogel — het gedrag van CAR-Ms verder kon afstemmen. Ze ontwikkelden een gelatine–alginaat hydrogel waarvan de “loss modulus”, een maat voor hoe de gel onder spanning langzaam ontspant, fijn kon worden afgesteld zonder de algehele stijfheid te veranderen. Wanneer CAR-Ms kort op gels met de juiste visco-elasticiteit werden gekweekt, nam hun vermogen om doelgerichte fibroblasten te doden meer toe dan met gebruikelijke chemische stimulerende middelen, en de versterking bleef ten minste twee dagen aanhouden. Deze “Gel-CAR-Ms” zetten ook genen aan die verbonden zijn met immuunactivatie en weefselhermodellering, terwijl genen die met fibrose geassocieerd worden juist werden gedimd, wat suggereert dat de gelervaring een meer anti-litteken identiteit in de cellen indrukte.
Hoe een zachtere ondergrond celgedrag herbedraadt
Om te begrijpen waarom de gel belangrijk was, onderzocht het team de fysieke staat van de CAR-receptoren op het celoppervlak. Een fluorescente probe toonde aan dat hydrogel-geprimeerde CAR-Ms een lagere membraanspanning hadden — de buitenste huid van de cel was meer ontspannen. Onder deze omstandigheden spreidden CAR-moleculen zich uit van nauwe clusters naar meer geïsoleerde enkelvoudige eenheden en paren. Biochemische tests lieten zien dat deze verspreide receptoren de voorkeur gaven aan vormen die gemakkelijker interne signalering opwekten, vooral langs paden zoals ERK die activatie en dodecapaciteit regelen. Het nabootsen van de spanningsdaling met een klein molecuul reproduceerde dezelfde receptorverspreiding en verbeterde het doden van doelcellen, wat de gedachte ondersteunt dat mechanische ontspanning van het membraan genoeg is om de cellen te “voorbewapenen” voordat ze hun doelen ontmoeten. 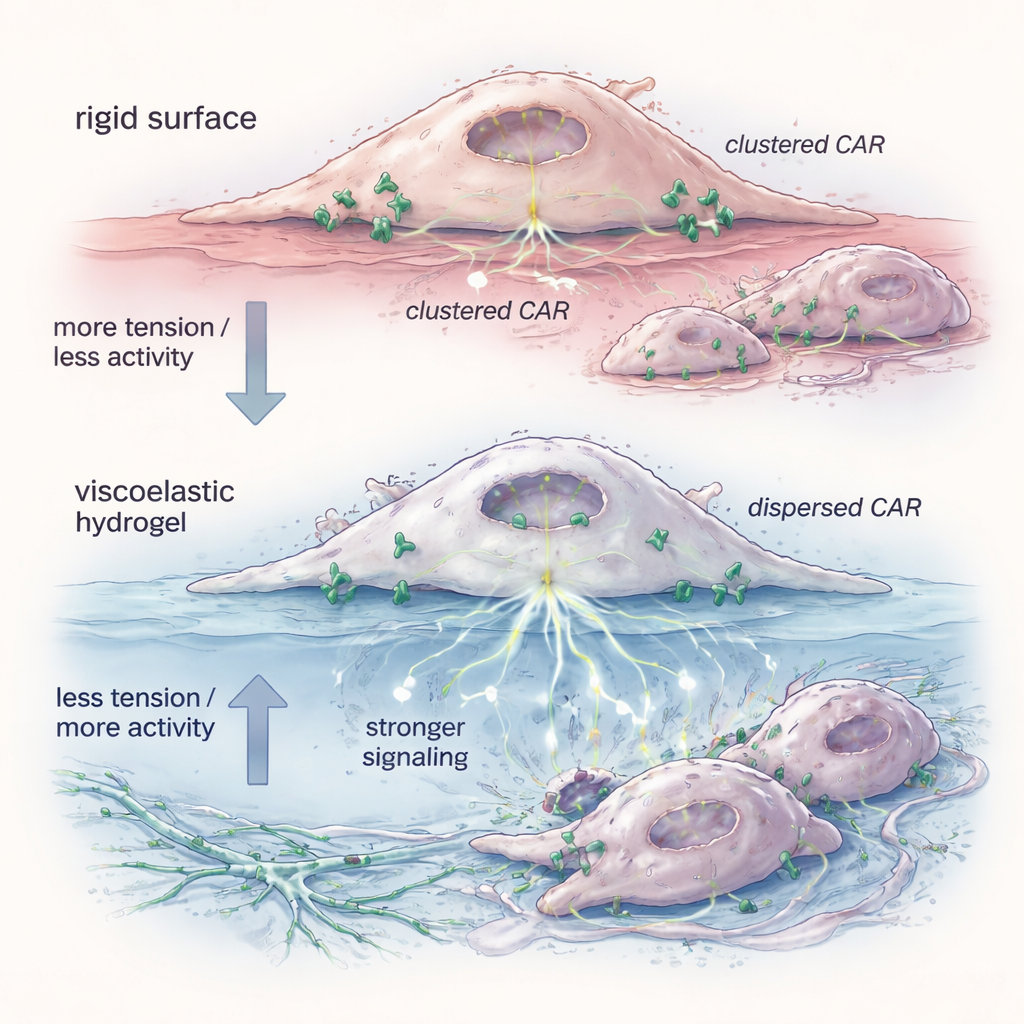
Genezende littekenlongen bij muizen
De ultieme test was een muismodel van medicijn-geïnduceerde longfibrose. Dieren kregen ofwel gewone macrofagen, standaard CAR-Ms of hydrogel-geprimeerde Gel-CAR-Ms. Alle behandelde muizen verbeterden in vergelijking met onbehandelde controles, maar Gel-CAR-Ms presteerden het beste: hun longen bevatten minder collageen, meer normale luchtzakjes en minder FAP-positieve fibroblasten. Genexpressiegegevens uit longweefsel toonden dat Gel-CAR-Ms ontstekingssignalen kalmeerden en de expressie van litteken-gerelateerde genen effectiever verminderden dan standaard CAR-Ms. Getraceerde cellen bleven ten minste een week in de long aanwezig en uitgebreide veiligheidsonderzoeken over 12 weken vonden geen belangrijke orgaanschade, bloedafwijkingen of tekenen van auto-immuniteit.
Een nieuwe richting voor celgebaseerde anti-fibrose therapieën
Voor niet-specialisten is de kernboodschap dat de combinatie van gerichte celengineering en slimme materialen aangeboren immuuncellen kan omvormen tot zeer effectieve, maar niet genetisch overdreven gecompliceerde, littekenbestrijdende middelen. Door korte tijd geprogrammeerde macrofagen op een zorgvuldig afgestemde zachte gel te laten rusten, “presetten” de onderzoekers mechanisch hun oppervlakte-receptoren in een meer responsieve modus. In muizen met longfibrose resulteerde dit in betere verwijdering van schadelijke fibroblasten, afbraak van overtollig collageen en gedeeltelijk herstel van een normaal longstructuur — zonder duidelijke veiligheidsproblemen. Hoewel er nog veel werk nodig is voordat menselijke proeven mogelijk zijn, suggereert deze aanpak dat het verfijnen van de fysieke omgeving van therapeutische cellen de behandeling van fibrotische longaandoeningen in de toekomst krachtiger en preciezer kan maken.
Bronvermelding: Zhang, Y., Liu, Z., Kong, W. et al. Viscoelastic hydrogel primed CAR-macrophage for pulmonary fibrosis treatment. Nat Commun 17, 1663 (2026). https://doi.org/10.1038/s41467-025-68033-4
Trefwoorden: longfibrose, CAR-macrofagen therapie, visco-elastische hydrogel, fibroblast activatie-eiwit, cel mechanobiologie