Clear Sky Science · nl
Moleculaire basis voor de remming van de novo DNA-methylering door TCL1A
Hoe cellen beslissen wat ze onthouden
Elke cel in je lichaam draagt in wezen hetzelfde DNA, maar zenuwcellen, bloedcellen en huidcellen gedragen zich heel verschillend. Een manier waarop cellen hun identiteit "onthouden", is via chemische labels die aan DNA worden toegevoegd — een proces dat DNA-methylering wordt genoemd. Deze studie onthult, tot op atomaire details, hoe een klein eiwit genaamd TCL1A de enzymen die deze methyleringsmerken aanbrengen kan uitschakelen. Omdat zowel DNA-methylering als TCL1A gekoppeld zijn aan kanker en voortplantingsstoornissen, kan inzicht in deze moleculaire touwtrekkerij uiteindelijk leiden tot nieuwe therapieën.
Het DNA-labelsysteem van de cel
DNA-methylering werkt als een potloodstreep in de marge van het genoom: het helpt bepaalde genen stil te leggen en stabiliseert het genoom tijdens ontwikkeling. Twee enzymen, DNMT3A en DNMT3B, zijn de belangrijkste "schrijvers" die nieuwe methylgroepen plaatsen tijdens vroege ontwikkeling en wanneer stamcellen zich specialiseren. Als deze enzymen gemuteerd of slecht gereguleerd zijn, raakt het patroon van DNA-labels verstoord, wat kan bijdragen aan ontwikkelingssyndromen en bloedkankers. TCL1A is een eiwit dat vooral bekend is vanwege zijn rol in kankers van immuuncellen, waar het vaak te veel wordt geproduceerd. Eerder werk suggereerde dat TCL1A kan binden aan DNMT3A en DNMT3B en hun activiteit kan temperen, maar niemand wist precies hoe dat blok tot stand komt.
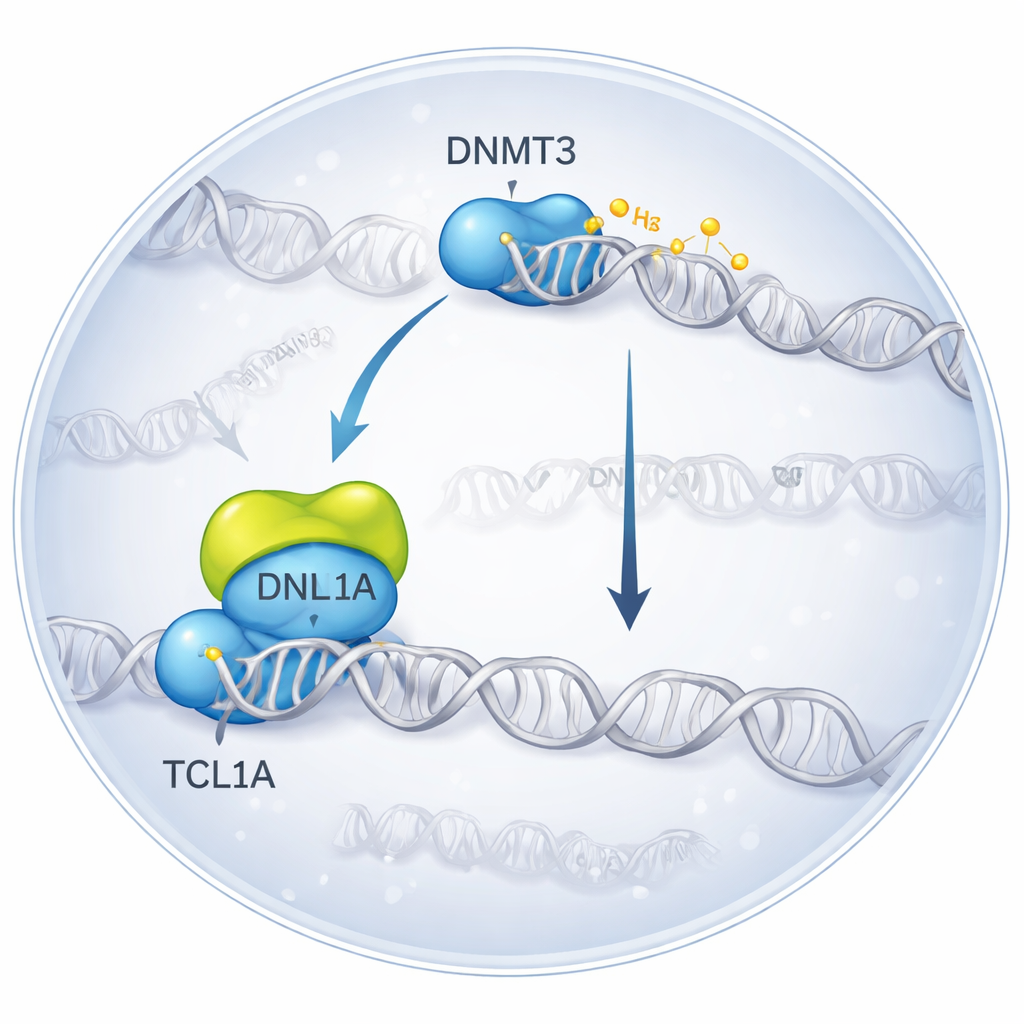
Een moleculair ontmoeting bevriezen in 3D
De onderzoekers gebruikten cryo-elektronenmicroscopie, een techniek die geflash‑vroren moleculen afbeeldt, om het complex te visualiseren dat ontstaat wanneer DNMT3A aan TCL1A bindt. Ze vonden dat twee DNMT3A-moleculen een paar vormen, en aan elke kant dockt een TCL1A-dimeer op het katalytische deel van DNMT3A — precies het gebied dat normaal gesproken met hulp-eiwitten en DNA interageert. Dit bindingsvlak overlapt met de plek waar een andere partner, DNMT3L, gewoonlijk aanhecht om DNMT3A’s activiteit te verhogen. In biochemische tests verminderde toevoeging van TCL1A sterk het vermogen van zowel DNMT3A als DNMT3B om DNA te methyleren, zelfs in aanwezigheid van DNMT3L, wat bevestigt dat het structurele complex overeenkomt met een sterk geremde toestand.
Een vormverandering die het enzym blokkeert
Bij nadere beschouwing zagen de onderzoekers dat TCL1A-binding niet eenvoudigweg bovenop het actieve centrum ligt als een deksel. In plaats daarvan veroorzaakt het een subtiele maar verstrekkende verandering in de vorm van DNMT3A. Twee flexibele regio’s van het enzym, bekend als de target‑recognition loop en de catalytic loop, zwaaien weg van de posities die ze innemen wanneer DNMT3A aan DNA gebonden is. In de actieve vorm nestelen deze lussen zich tegen DNA en vormen ze een pocket voor een klein brandstofmolecuul genaamd SAM, dat de methylgroep levert. Met TCL1A eraan vast, vouwt de catalytic loop zich in plaats daarvan in de SAM-pocket en blokkeert die, terwijl het ook moeilijker wordt voor DNA om het enzym te bereiken. Bindingsmetingen bevestigden dat DNMT3A geassocieerd met TCL1A DNA of SAM niet meer detecteerbaar kan vastgrijpen.
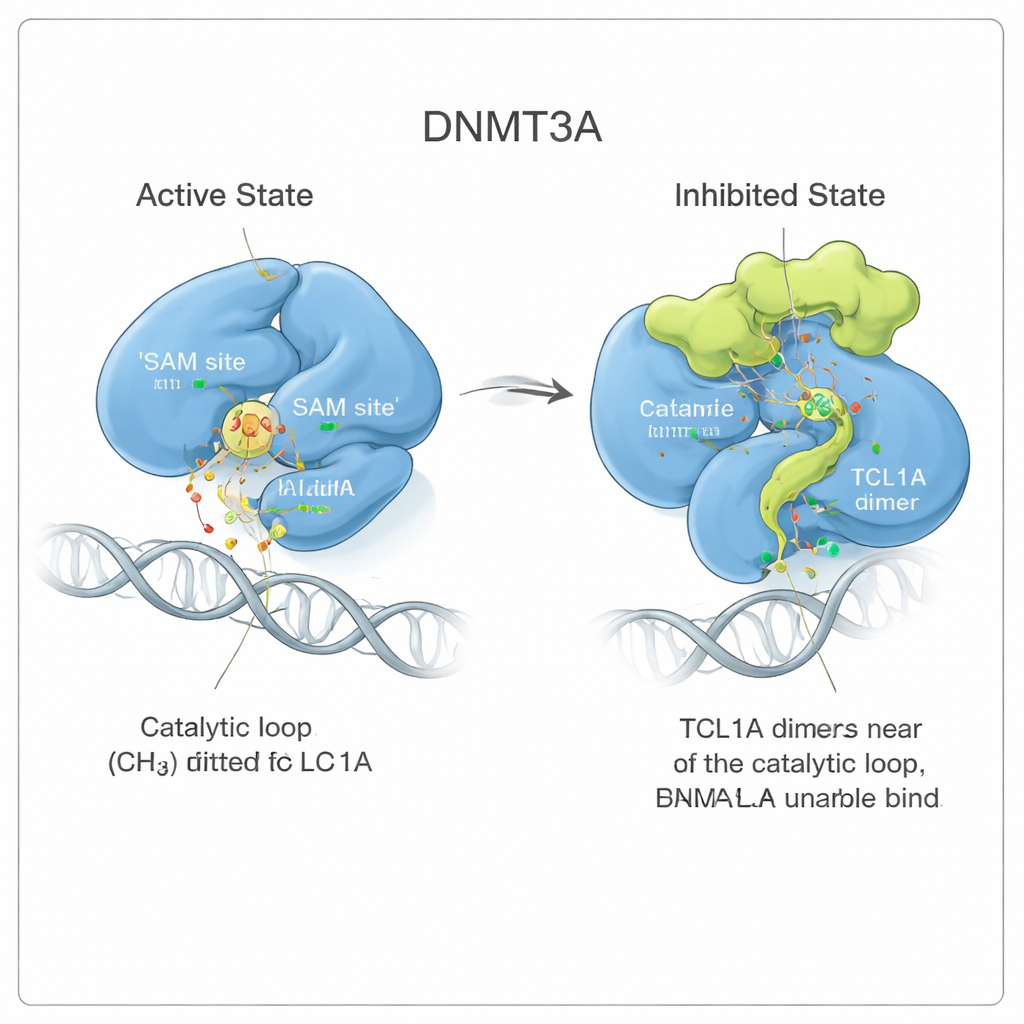
Een dynamisch blok in beweging bekijken
Om te begrijpen hoe stabiel deze geremde conformatie is, voerden de auteurs lange moleculaire dynamica-simulaties uit — in wezen natuurkundige films van de moleculen in oplossing. Wanneer DNMT3A aan zijn activator DNMT3L gebonden was, bleef de catalytic loop stevig in zijn actieve positie. In aanwezigheid van TCL1A werd die loop veel mobieler, flapperend rond maar herhaaldelijk de SAM-pocket bezettend als zeewier dat draait en toch een afvoer verstopt. Deze constante beweging verkleinde de beschikbare ruimte voor SAM meer dan tienvoudig, wat een model ondersteunt waarin TCL1A gebruikmaakt van de natuurlijke flexibiliteit van DNMT3A om een dynamische, in plaats van starre, vorm van remming op te leggen.
Gevolgen voor ontwikkelende cellen en ziekte
Het team vroeg vervolgens wat deze moleculaire blokkade betekent voor echte cellen. Ze manipuleerden muizembryonale stamcellen zodat ze menselijke TCL1A produceerden tijdens een fase waarin de cellen normaal gesproken hun DNA-methylering opvoeren zodra ze beginnen te differentiëren. Genoombrede methyleringskaarten toonden aan dat cellen die TCL1A overproduceren, er niet in slaagden het gebruikelijke hoge niveau van DNA-methylering te bereiken, wat sterk leek op cellen waarin zowel Dnmt3a als Dnmt3b waren uitgeschakeld. Een gemuteerde versie van TCL1A die slecht aan DNMT3-enzymen bindt had weinig effect, wat benadrukt dat de fysieke interactie cruciaal is. Deze bevindingen koppelen het structurele mechanisme aan brede epigenetische veranderingen in het hele genoom.
Wat dit betekent voor de gezondheid
Samengevat laat het werk zien hoe TCL1A kan fungeren als een krachtige rem op de enzymen die nieuwe DNA-methylgroepen plaatsen. Door te docken op een kritische interface herpositioneert TCL1A flexibele lussen in DNMT3A en DNMT3B zodat ze hun DNA-template of chemische brandstof niet meer kunnen binden, wat leidt tot een wereldwijde afname van methyleringsmerken in cellen. Tijdens normale ontwikkeling kan dit soort fijnmazige controle helpen bepalen wanneer en waar methylering wordt toegevoegd. Wanneer TCL1A verkeerd gepositioneerd of overgeproduceerd is, zoals bij bepaalde bloedkankers en zeldzame voortplantingsstoornissen, kan hetzelfde mechanisme het epigenetische programma van de cel ontregelen. Begrip van deze interactie op atomaire resolutie opent de deur naar het ontwerpen van moleculen die de effecten van TCL1A nabootsen of tegengaan, mogelijk met het doel gezonde DNA-methyleringspatronen te herstellen.
Bronvermelding: Liu, Q., Li, J., Wang, X. et al. Molecular basis for the inhibition of de novo DNA methylation by TCL1A. Nat Commun 17, 2159 (2026). https://doi.org/10.1038/s41467-025-67710-8
Trefwoorden: DNA-methylering, DNMT3A, TCL1A, epigenetica, kanker