Clear Sky Science · nl
Voorbeelden van aflevermethoden voor eiwit-X-raykristallografie met speciale aandacht voor staalverbruik
Moleculen in actie bekijken
X-raykristallografie stelt onderzoekers in staat de rangschikking van atomen in eiwitten te zien, de kleine machientjes die het leven aandrijven. Een nieuwere benadering, seriële kristallografie genoemd, gaat een stap verder: ze kan “moleculaire films” van eiwitten in actie vastleggen, bijvoorbeeld enzymen die een geneesmiddel verwerken of fotosynthetische eiwitten die water splitsen. Er zit echter een keerzijde aan. Veel belangrijke eiwitten zijn moeilijk te produceren en te kristalliseren, en huidige experimenten verbruiken gemakkelijk milligrammen tot grammen van dit kostbare materiaal. Dit overzichtsartikel stelt een ogenschijnlijk eenvoudige vraag: hoe kunnen we kristallen in krachtige X-raystralen afleveren terwijl we zo weinig mogelijk monster verspillen?
Waarom seriële kristallografie betere aflevermethoden nodig heeft
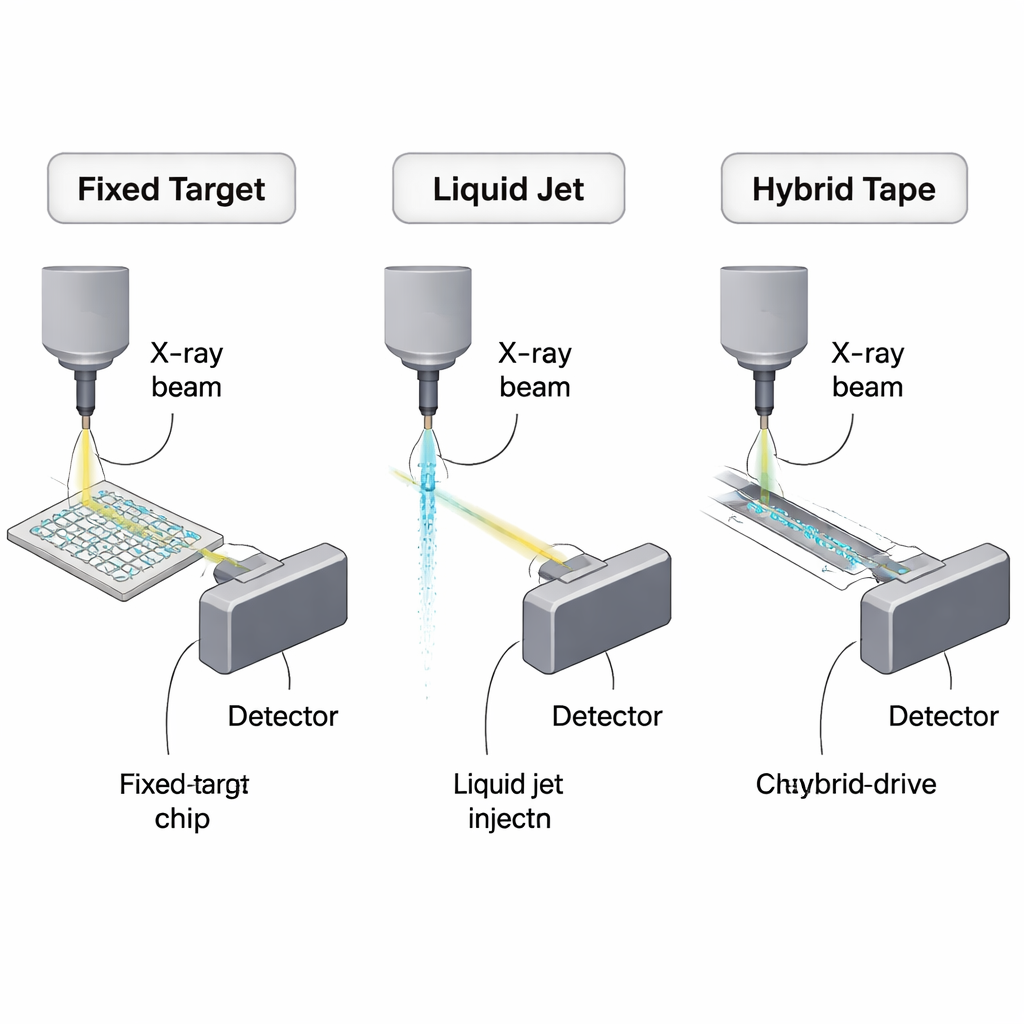
Traditionele kristallografie berustte op één grote kristal die in een X-raystraal werd geroteerd. Seriële kristallografie draait het om: in plaats van één grote kristal worden duizenden microkristallen, die elk maar één keer worden gebruikt, door ultrafelle X-raypulsen van synchrotrons of X-ray vrije-elektronenlasers (XFELs) geschoten of gescand. Dit maakt dataverzameling bij kamertemperatuur en snelle “momentopnamen” van chemische reacties mogelijk, maar het betekent ook dat voortdurend kristallen moeten worden aangevoerd met snelheden die passen bij X-raypulstreinen die tot miljoenen pulsen per seconde kunnen reiken. Veel van de kristaloplossing komt nooit in aanraking met de straal en wordt weggegooid, dus het terugdringen van monsterverbruik is een centraal technisch en economisch vraagstuk geworden in het veld.
Vaste doelwitten: kleine chipjes die elke druppel rekken
Een belangrijke strategie is het immobiliseren van microkristallen op kleine vaste dragers, vaste doelwitten genaamd. In plaats van kristallen langs de straal te sproeien, rangschikken onderzoekers ze in arrays op silicium- of polymeerchips en verplaatsen ze de chip zodat elk kristal eenmaal in het X-rayfocalepunt komt. In het beste denkbare geval zou circa 10.000 microkristallen van een model-eiwit in principe een volledige dataset kunnen opleveren met slechts ongeveer 450 nanogram eiwit. Eeuwige apparaten zijn nog niet zo zuinig, maar ze verminderen de benodigde hoeveelheid al tot tientallen microgrammen tot enkele tienden van een milligram—orde(en) van grootte beter dan de eerste seriële experimenten. Het overzicht vergelijkt siliciumgaasjes, ultradunne polymeerfolies en meerlaagse plasticchips en weegt hun sterke punten (lage achtergrondverstrooiing, groei van kristallen op de chip, compatibiliteit met studies bij kamertemperatuur) af tegen praktische problemen zoals uitdroging, ongewenste verstrooiing door het chipmateriaal en extra “dode volume” dat ontstaat bij handmatig pipetteren.
Vloeistofjets en viskeuze stromen: snel maar vraatzuchtig
Een andere groep methoden houdt kristallen in suspensie in vloeistof en levert ze continu door de straal. Gas-dynamische virtuele nozzles creëren haarfijne jets die gelijke tred kunnen houden met snelle XFEL-pulstreinen en zijn daardoor een werkpaard voor tijdsopgeloste studies en mix‑and‑inject-experimenten waarbij reacties worden geactiveerd door snelle menging net voor blootstelling. Omdat jets echter voortdurend lopen, komt het grootste deel van de stroom nooit een X-raypuls tegen. Zelfs met zorgvuldige afstemming verbruiken praktische experimenten veel meer eiwit dan het theoretische minimum—typisch tientallen tot honderden microliters geconcentreerde kristalpap. Om het verlies te beperken hebben onderzoekers efficiëntere ontwerpen ontwikkeld, zoals dubbelstroomdoppen die de kristalstroom omhullen met een offerende vloeistof, electrospun MESH-injectoren die bij lagere debieten werken, en hoogviskeuze extruders die kristallen ingebed in gels of lipidic cubic phases met microliters per minuut of langzamer duwen. Deze viskeuze methoden zijn vooral waardevol voor kwetsbare membraaneiwitten en voor studies bij kamertemperatuur aan synchrotrons, maar hun dikkere stromen verhogen de achtergrondverstrooiing en zijn minder geschikt voor de aller-snelste X-raybronnen.
Druppels, tapes en hybriden: pulsen één voor één matchen
Een derde, steeds creatievere klasse van “hybride” benaderingen combineert vaste dragers met gecontroleerde vloeistof- of druppelafgifte. Tape-drive-systemen bijvoorbeeld deponeerden druppels of dunne vloeistofstrepen op een bewegende polymeerfilm die door de straal loopt; door de beweging te timen kunnen reactiestappen of gasblootstelling op gedefinieerde vertragingen worden onderzocht. Drop-on-demand-systemen gaan verder en gebruiken akoestische of piezo-elektrische apparaten om nanoliter- of zelfs picoliterdruppels alleen uit te werpen wanneer een X-raypuls wordt verwacht, wat het afval drastisch vermindert. Sommige ontwerpen mengen een liganddruppel met een vooraf geplaatste kristalbevattende druppel op tape net vóór de straal, wat tijdsopgeloste enzymologie mogelijk maakt met nauwkeurig gedoseerde reagentia. Andere hybriden, zoals de LAMA-on-chip-methode, brengen piepkleine druppels substraat direct aan op kristallen die vooraf op vaste doelwitchips zijn gemonteerd. Over deze ontwerpen heen varieert het gerapporteerde eiwitgebruik sterk—van nabij milligramniveaus tot enkele milligrammen voor volledige tijdsopgeloste series—wat zowel de belofte als de huidige technische uitdagingen van het synchroniseren van druppels, kristallen en X-raypulsen illustreert.
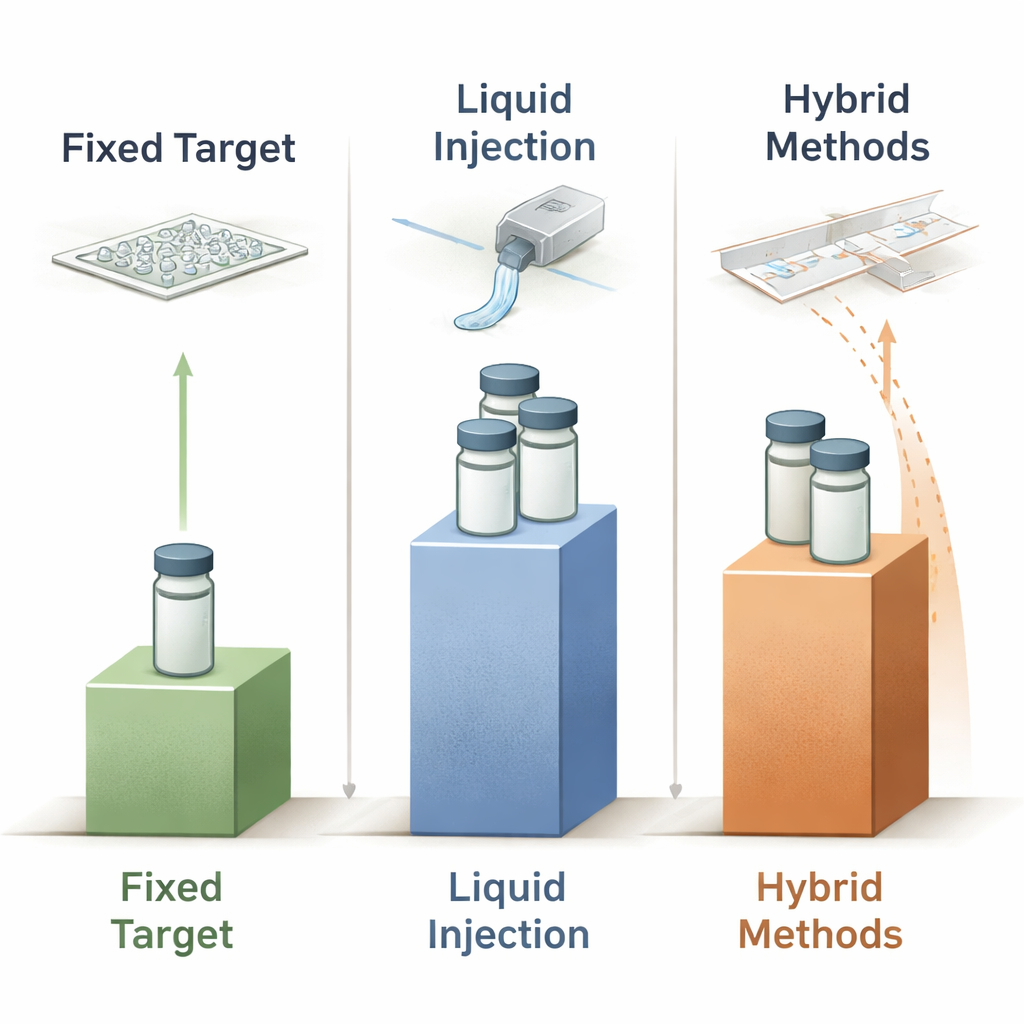
Hoe dicht zitten we bij het theoretische minimum?
Door tientallen gepubliceerde experimenten met vaste doelwitten, vloeistofinjectoren en hybride systemen te vergelijken laten de auteurs zien dat geen enkele bestaande methode in de buurt komt van de ideale 450‑nanogramnorm; zelfs de beste apparaten overschrijden dat nog met ongeveer twee orde van grootte. Toch tekenen zich duidelijke trends af. Vaste doelwitten gebruiken doorgaans het minste eiwit en zijn aantrekkelijk wanneer tijdsopgeloste menging niet essentieel is of op de chip kan worden gerealiseerd. Vloeistofjets domineren nog steeds de meest veeleisende tijdsopgeloste XFEL-studies maar blijven monsterintensief, vooral wanneer veel tijdspunten nodig zijn. Hybride druppel‑en‑tape‑schema’s bieden sommige van de grootste relatieve besparingen, vooral als de druppeltiming strak gesynchroniseerd is met de X-raybron. Vooruitkijkend stellen de auteurs dat verdere vooruitgang zal komen van betere microfluidische controle, automatisering om verspilling bij handelingen te elimineren, en het gebruik van compacte X-raybronnen en data‑gedreven optimalisatie om experimenten en afleveringssystemen samen te ontwerpen zodat het eiwitgebruik steeds dichter bij het theoretische maximum wordt gebracht.
Bronvermelding: Manna, A., Doppler, D., Sripati, M.P. et al. Sample delivery methods for protein X-ray crystallography with a special focus on sample consumption. Nat Commun 16, 9856 (2025). https://doi.org/10.1038/s41467-025-65173-5
Trefwoorden: seriële kristallografie, eiwit-X-raykristallografie, monsterafgifte, X-ray vrije-elektronenlaser, microfluidica