Clear Sky Science · nl
Vermindering van RAD23A verlengt de levensduur en vermindert pathologie in een muismodel van TDP-43-proteïnopathie
Waarom dit onderzoek belangrijk is voor gezinnen en patiënten
Veel vormen van dementie en motorneuronziekten, waaronder amyotrofische laterale sclerose (ALS) en frontotemporale dementie (FTD), houden verband met eiwitten in hersencellen die verkeerd vouwen, samenklonteren en neuronenen langzaam vergiftigen. Een van de belangrijkste boosdoeners is een eiwit genaamd TDP-43, dat normaal gesproken helpt bij het reguleren van RNA maar toxisch wordt wanneer het aggregateert. Deze studie stelt een hoopvolle vraag: kunnen we hersencellen veerkrachtiger maken door een ander eiwit, RAD23A, dat helpt bepalen hoe beschadigde eiwitten worden afgehandeld, te verlagen? De auteurs tonen in muizen aan dat verlaging van RAD23A de levensduur kan verlengen, de beweging kan verbeteren en hersenschade kan verminderen in een model van TDP-43–gedreven ziekte, wat wijst op een nieuw soort behandelstrategie.
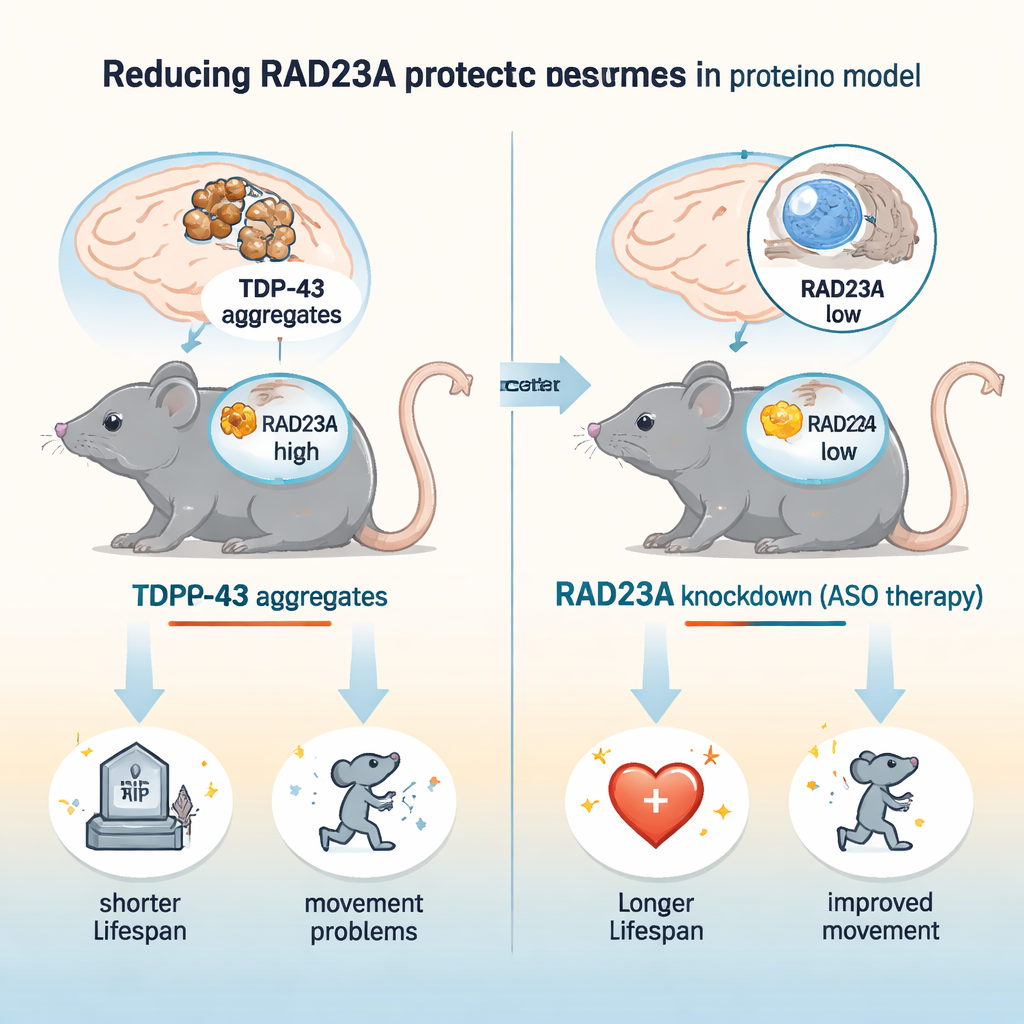
Een eiwitfile in zieke neuronen
Neurodegeneratieve ziekten worden vaak gekenmerkt door hopen verkeerd gevouwen eiwitten die de afvalverwerkingsmachinerie van de cel niet weet te verwijderen. Bij ALS en FTD verplaatst TDP-43 zich uit de kern, vormt plakkerige klonters en wordt sterk gemerkt met ubiquitine, een signaal dat normaal eiwitten naar het proteasoom stuurt, de belangrijkste versnipperaar van de cel. RAD23A is een van meerdere “shuttle”-eiwitten die ubiquitine-gemarkeerd materiaal naar het proteasoom kunnen brengen. Eerder werk in wormen en gekweekte neuronen suggereerde echter dat verlies van RAD23-achtige eiwitten TDP-43–geïnduceerde schade juist kon beperken, een paradox die deze studie in een levend zoogdierbrein onderzocht.
RAD23A verlagen in een TDP-43-muismodel
De onderzoekers gebruikten een goed ingeburgerd muismodel, TAR4/4 genoemd, dat menselijke TDP-43 in neuronen overproduceert en bewegingsproblemen, wervelkolomverkromming, tremor en vroegtijdige sterfte ontwikkelt, kenmerkend voor ALS/FTD. Ze verlaagden RAD23A op twee manieren: door pasgeboren muizen te injecteren met antisense-oligonucleotiden (ASO’s) die Rad23a-RNA verminderen, en door muizen te kruisen die een genetische knockout van Rad23a dragen. Een enkele ASO-behandeling verlaagde RAD23A-niveaus in hersenen en ruggenmerg met ongeveer driekwart. Bij deze TDP-43-muizen verlengde RAD23A-knockdown de levensduur met ongeveer 50% en vertraagde het begin en de ernst van loopstoornissen, tremor, wervelkolomverkromming en het dichtklappen van de achterpoten. Interessant genoeg bracht volledig genetisch verlies van RAD23A geen extra voordeel, wat suggereert dat gedeeltelijke reductie optimaal is en dat langdurige totale afwezigheid compenserende veranderingen kan veroorzaken.
Minder ontsteking, schonere eiwitverwerking en een rustiger genoom
Microscopisch onderzoek van de motorische cortex toonde aan dat TDP-43-muizen neuronen verloren en sterke activatie van astrocyten en microglia ontwikkelden, de steun- en immuuncellen van de hersenen. Verlaging van RAD23A behield het aantal neuronen en verminderde markers van ontsteking en celdood. Biochemische analyses toonden aan dat overproductie van TDP-43 cellen overspoelde met ubiquitine-gemerkte, detergenstongevoelige eiwitten en proteasoomsubunits in deze aggregaten trok, waardoor het vermogen van de cel om beschadigde eiwitten te verwijderen verzwakte. Het verminderen van RAD23A verlaagde de totale belasting van geubiquitineerde eiwitten, hield meer proteasomen in de oplosbare, werkende pool en bracht verschillende typen proteasoomactiviteit meer in de richting van normaal. Tegelijkertijd verminderde RAD23A-knockdown zowel totale als geaggregeerde vormen van TDP-43, waaronder een bijzonder toxisch fragment van 25 kilodalton, en verschoof TDP-43 van het cytoplasma terug naar de kern. Genoomwijde RNA-sequencing toonde dat duizenden genexpressieveranderingen veroorzaakt door TDP-43 gedeeltelijk werden teruggedraaid wanneer RAD23A werd verminderd, vooral genen die betrokken zijn bij neuronale functie, mitochondriale energieproductie en aggregaatopruimende routes zoals aggrephagy.
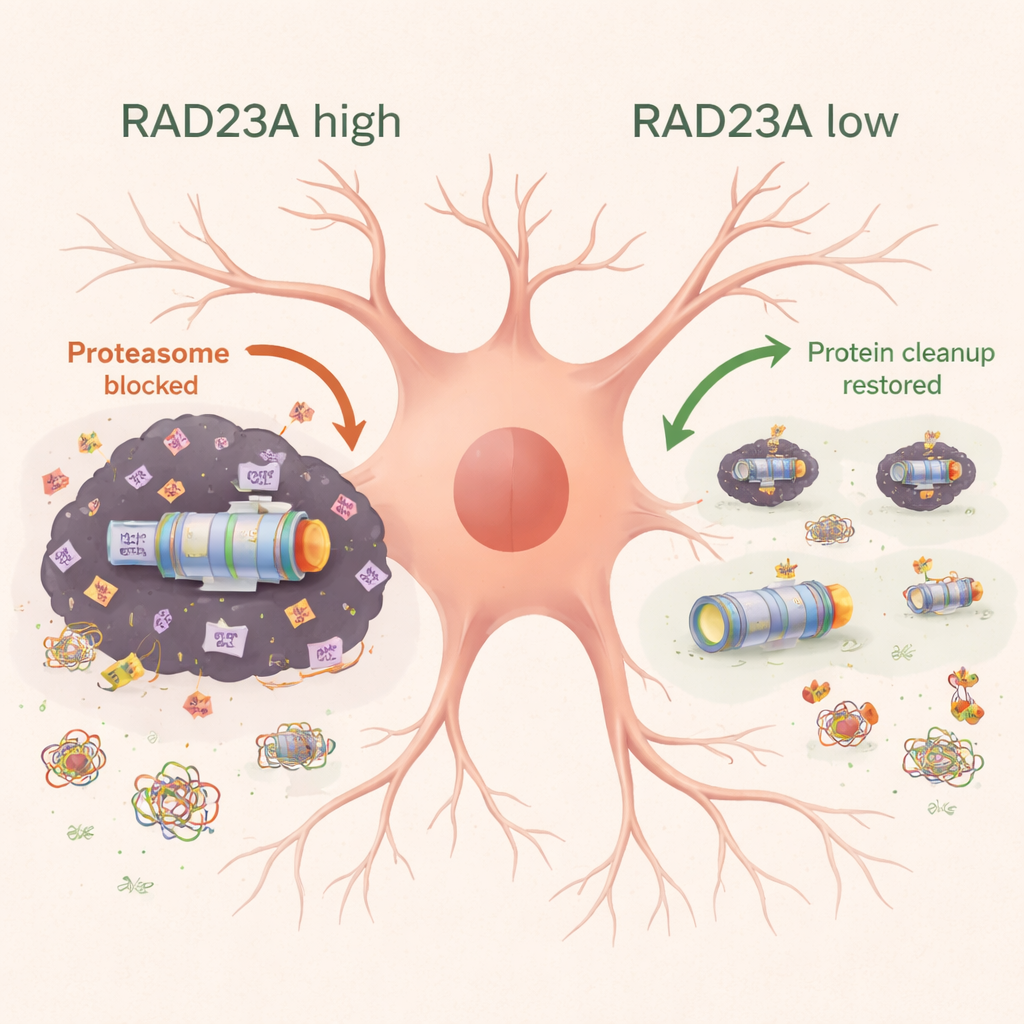
Het herschikken van het verborgen "onoplosbare" proteoom
Om de hardnekkige aggregaten die normale detergenten weerstaan nader te bekijken, gebruikte het team zware-isotoop-massaspectrometrie om eiwitten in de onoplosbare fractie van muiscortex in kaart te brengen. Expressie van menselijke TDP-43 lokte proteasoomcomponenten, cytoskelet- en transporteiwitten en andere cellulaire machinerie aan. Toen RAD23A werd verlaagd, veranderde de algehele samenstelling van dit onoplosbare proteoom: minder proteasoom- en transportgerelateerde eiwitten werden aangespoord, terwijl sommige ribosomale en stressgerelateerde eiwitten in de aggregaten toenamen. Opmerkelijk is dat deze herinrichting niet eenvoudigweg de veranderingen in RNA-niveaus weerspiegelde, wat suggereert dat RAD23A voornamelijk beïnvloedt hoe bestaande eiwitten worden verdeeld tussen oplosbare en geaggregeerde toestanden, in plaats van hoeveel van elk eiwit wordt aangemaakt.
Wat dit kan betekenen voor toekomstige therapieën
Samen schetsen deze bevindingen RAD23A als een krachtige tuner van eiwitkwaliteitscontrole in gestreste neuronen. Door RAD23A gedeeltelijk te verlagen in een TDP-43–gedreven muismodel konden de auteurs toxische eiwitklonters verminderen, de activiteit van de eiwitafvalmachinerie herstellen, schadelijke veranderingen in genexpressie dempen, hersenontsteking beperken en levensduur en motorische functie verlengen. Omdat abnormale ophoping van TDP-43 wijdverbreid is in zowel erfelijke als sporadische vormen van ALS, FTD en verwante aandoeningen, zou het richten op RAD23A met mensvriendelijke antisense-medicijnen een manier kunnen bieden om neuronen te beschermen zonder TDP-43 zelf direct te blokkeren, een essentieel eiwit. Hoewel veel nog getest moet worden in andere modellen en bij mensen, identificeert dit werk RAD23A als een veelbelovend nieuw aanknopingspunt voor een gemeenschappelijk pad van neurodegeneratie.
Bronvermelding: Guo, X., Prajapati, R.S., Chun, J. et al. Reduction of RAD23A extends lifespan and mitigates pathology in a mouse model of TDP-43 proteinopathy. Nat Commun 17, 1820 (2026). https://doi.org/10.1038/s41467-025-65104-4
Trefwoorden: TDP-43, ALS, proteinaggregation, proteasoom, antisense therapie