Clear Sky Science · nl
Het zenuwcentrum van orgaanengineering
Waarom het aansluiten van organen ertoe doet
Wetenschappers komen steeds dichter bij het in het lab bouwen van vervangende organen om het grote tekort aan donorharten, -levers, -nieren en meer aan te pakken. Maar de meeste kunstmatige organen richten zich op bloedvaten en negeren een andere cruciale component: zenuwen. Dit overzichtsartikel legt uit waarom de elektrische bedrading van het lichaam essentieel is voor orgaangroei, dagelijkse functie en genezing, en hoe onderzoekers leren zenuwnetwerken in in vitro gekweekte organen te integreren.
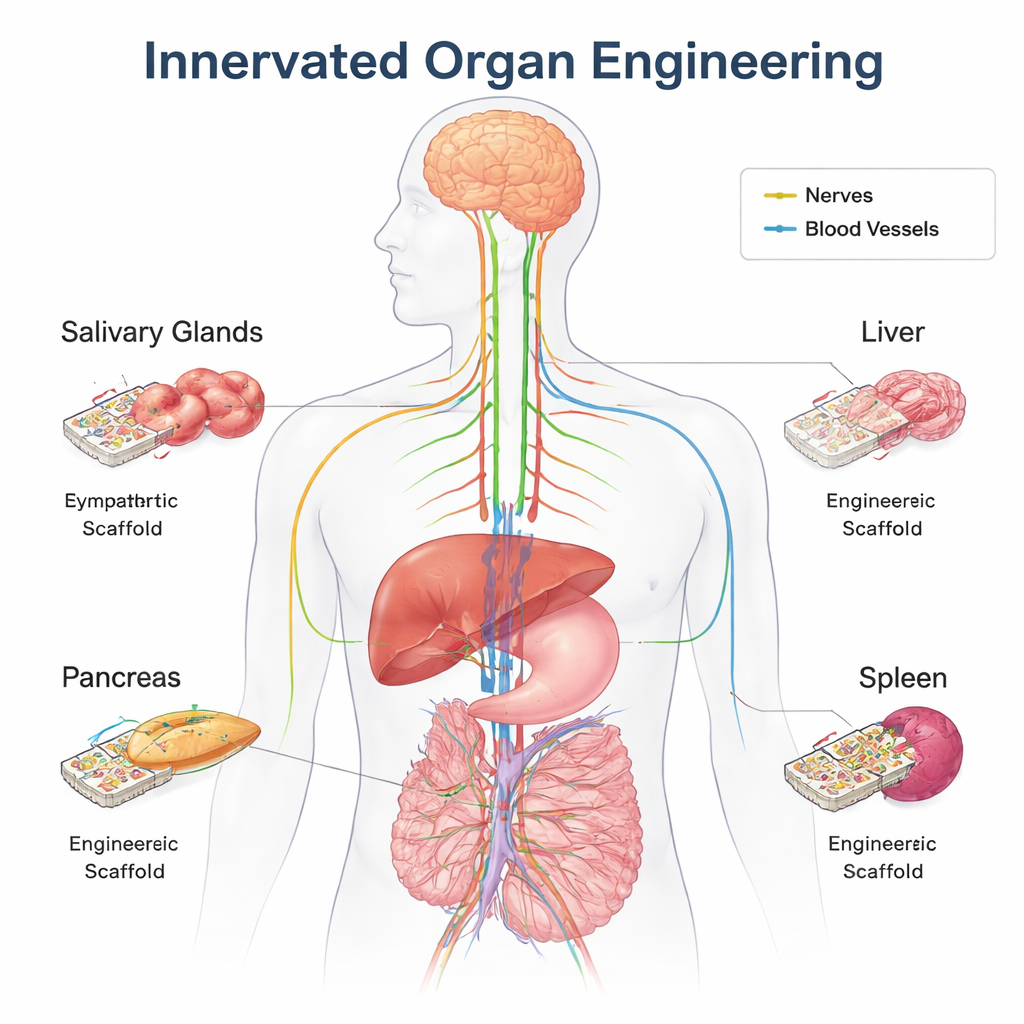
Het verborgen regelnetwerk van het lichaam
Elk groot orgaan is doordrongen van zenuwvezels die voortdurend communiceren met de hersenen en het ruggenmerg. Via het autonome zenuwstelsel — de ‘vecht-of-vlucht’ en ‘rust-en-vertering’ takken — regelen deze zenuwen stilletjes bloedsuiker, spijsvertering, immuunreacties, bloedstroom en meer. Ze doen dit door chemische boodschappen te sturen zoals acetylcholine en noradrenaline, en door veranderingen te voelen zoals rek, temperatuur of voedingsniveaus. Buiten de dagelijkse regulatie helpen zenuwen ook organen vorm te geven vóór de geboorte, wondgenezing te begeleiden en stamcellen te ondersteunen die weefsel herstellen. Op veel plaatsen groeien zenuwen naast bloedvaten en gebruiken vergelijkbare geleidingssignalen, zodat bedrading en leidingen samen ontwikkelden.
Waarom transplantaties het zonder zenuwen redden — maar laborganen niet
Bij traditionele orgaantransplantaties worden de oorspronkelijke zenuwen meestal niet mee overgeplant. Een getransplanteerde lever of nier kan nog steeds functioneren omdat hij hormonen en andere signalen via de bloedbaan ontvangt, en na verloop van tijd kunnen nieuwe zenuwvezels vanuit de ontvanger ingroeien. Die ‘genadeperiode’ ontbreekt bij engineered organen die vanaf nul zijn opgebouwd. Deze constructen missen doorgaans de volledige mix van rijpe celtypen en de complexe ondersteunende matrix die in een natuurlijk orgaan aanwezig is. Precieze zenuwverbindingen zijn vooral belangrijk voor de coördinatie van de vele gespecialiseerde cellen in organen zoals de alvleesklier, lever, speekselklieren en milt. De auteurs betogen dat bij bottom-up orgaanengineering — waarbij organen worden samengesteld uit kleine bouwstenen — geplande innervatie moet worden behandeld als een ontwerpeis, niet als een optionele toevoeging.
Hoe zenuwen vier sleutelorganen vormen
Het overzicht onderzoekt in detail hoe zenuwen invloed uitoefenen op vier voorbeeldorganen. In de alvleesklier helpen sympathische en parasympathische vezels de architectuur van de insulineproducerende eilandjes tijdens de ontwikkeling te vormen en later de vrijgave van insulin en glucagon fijn af te stemmen als de bloedsuiker stijgt en daalt. In de speekselklieren houdt vroege parasympathische input epitheliale stamcellen in leven en stuurt het de vertakkende kanalen die uiteindelijk speeksel afscheiden; het doorknippen van deze zenuwen op het verkeerde moment verstoort de normale kliervorming. De zenuwen van de lever voelen zout-, water-, suiker- en vetniveaus in het bloed en passen metabolisme, bloeddruk en regeneratie na letsel aan. In de milt communiceren sympathische vezels rechtstreeks met immuuncellen, dempen of versterken ze ontsteking en helpen zo het lichaam te reageren op infectie en stress. In al deze organen hangt het verlies of verkeerd bedraden van zenuwen samen met diabetes, spijsverteringsproblemen, leverziekte en verstoorde immuniteit.
Organen bouwen met ingebouwde bedrading
Om innervatie in bio-geëngineerde organen te brengen, combineren wetenschappers geavanceerd 3D-printen, slim scaffold-ontwerp en stamcel-afgeleide zenuwcellen. Extrusie- en lichtgebaseerd bioprinten kunnen verschillende celtypen en materialen in precieze patronen plaatsen, terwijl gespecialiseerde hydrogels en polymeren zijn afgestemd om lange, vertakkende zenuwvezels te ondersteunen. Studies hebben al geprinte neurale netwerken, zenuw-spier-eenheden en miniatuur hersenachtige weefsels gecreëerd die realistische elektrische activiteit tonen. De auteurs schetsen praktische blauwdrukken voor geïnnerveerde versies van de alvleesklier, speekselklier, lever en milt: isoleer of derivéer de sleutelorgaancellen, meng ze met autonome neuronen (sympathisch en parasympathisch) in compatibele bio-inks, print ze in orgaanvormige structuren en rijp ze in bioreactoren zodat zenuwen zich in het weefsel kunnen uitstrekken vóór implantatie.
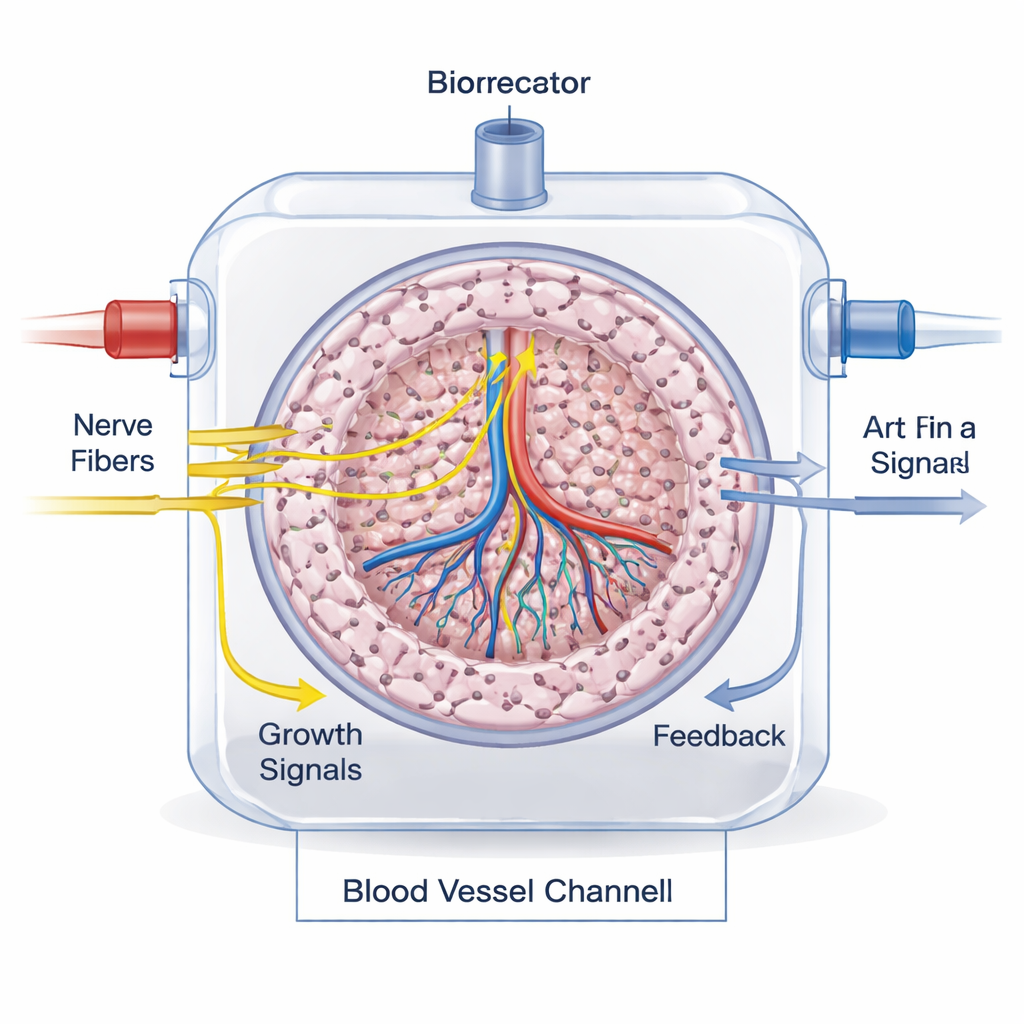
Meten of de bedrading werkt
Controleren of zenuwen daadwerkelijk geïntegreerd en functioneel zijn is een grote uitdaging. In het lab kleuren onderzoekers voor zenuwspecifieke eiwitten, meten ze neurotransmitters met biochemische tests en gebruiken ze live-imaging om axonen te volgen en cellen te zien reageren. Microfluidische ‘organ-on-a-chip’-platforms helpen realistische bloedstroom en zenuw‑orgaan‑signalering te modelleren. Bij dieren en uiteindelijk bij patiënten kan innervatie worden gevolgd door weefselkleuring, zenuwtracers en moderne beeldvormingstechnieken zoals MRI, CT en PET-scans te combineren met gespecialiseerde radioactieve verbindingen die sympathische of parasympathische vezels zichtbaar maken.
Van idee naar therapie
Het artikel concludeert dat zenuwen geen luxe zijn maar een kernvereiste voor echt functionele kunstmatige organen. Om van veelbelovende labdemo’s naar echte therapieën te komen, moet toekomstig werk grootschalig bioprinten van ingewikkelde zenuwnetwerken verbeteren, bronnencellen verfijnen (vooral humane stamcel-afgeleide autonome neuronen) en praktische klinische beeldvormingstools ontwikkelen om neuronale integratie na implantatie te monitoren. Als deze hobbels worden overwonnen, kunnen next-generation engineered organen niet alleen verloren weefsel vervangen maar ook naadloos aansluiten op de controlecircuits van het lichaam, en zo betrouwbaardere en levensgetrouwere behandelingen bieden voor diabetes, leverfalen, aandoeningen met een droge mond, immuundeficiënties en meer.
Bronvermelding: Das, S., Gordián-Vélez, W.J., Dave, J.R. et al. The nerve center of organ engineering. Nat Commun 16, 9834 (2025). https://doi.org/10.1038/s41467-025-64801-4
Trefwoorden: orgaanengineering, innervatie, biofabricage, 3D-bioprinten, autonoom zenuwstelsel