Clear Sky Science · nl
Optische superresolutie-histologie van formaline-gefixeerde, in paraffine ingebedde weefselmonsters: uitdagingen en kansen
Meer zien in bewaarde weefselmonsters
Ziekenhuizen over de hele wereld bewaren dunne plakjes van patiëntorganen in wasblokken zodat ziekten zoals kanker of nierschade jarenlang bestudeerd kunnen worden. Dit overzichtsartikel legt uit hoe nieuwe typen lichtmicroscopen van die routinematige monsters krachtige vensters op ziekte maken, waarbij details zichtbaar worden die te klein zijn voor standaardziekenhuismicroscopen. Deze vooruitgang kan artsen helpen ziekten eerder te detecteren, te begrijpen hoe ze zich ontwikkelen en behandelingen preciezer af te stemmen.
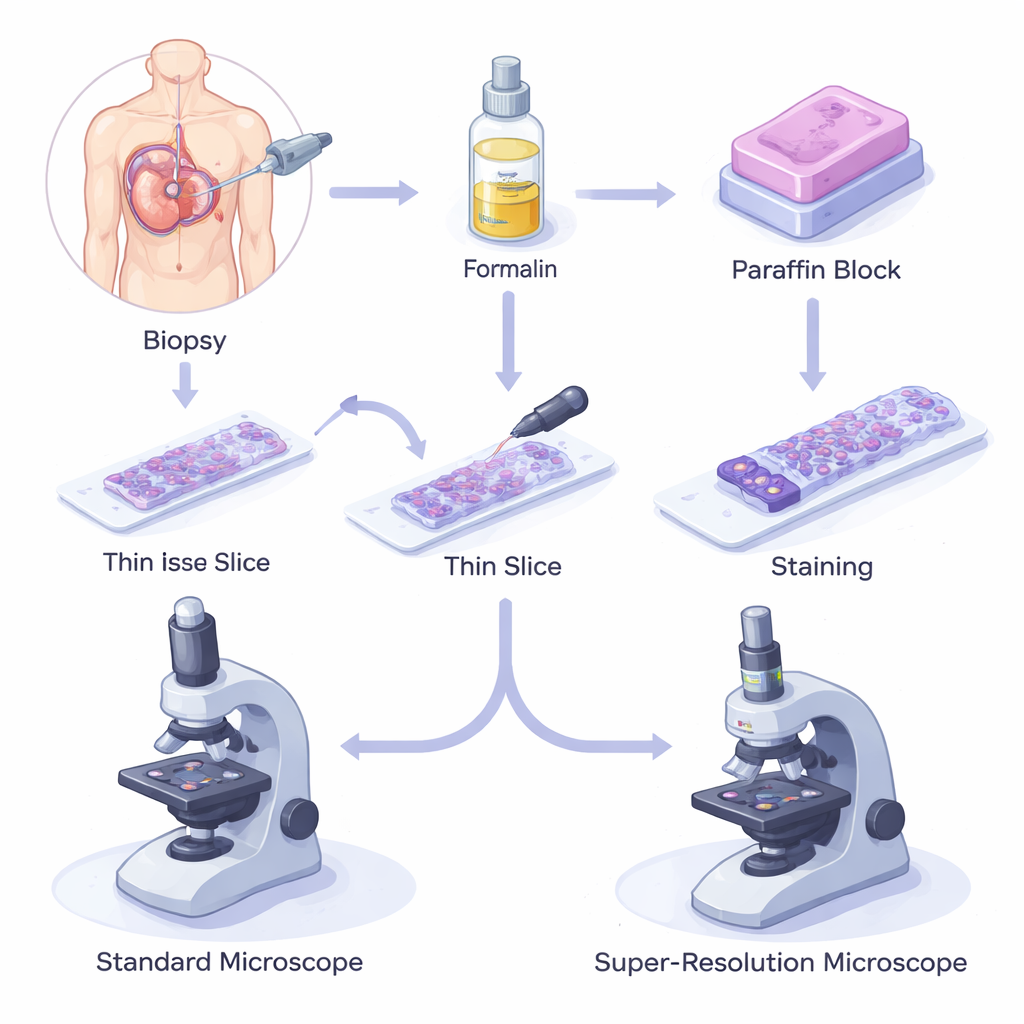
Hoe in was geconserveerde weefsels de moderne geneeskunde voeden
Wanneer een patiënt een biopsie ondergaat, wordt een klein weefselstuk verwijderd, gefixeerd in een chemische stof genaamd formaline om bederf te stoppen, en vervolgens ingebed in paraffinewas. Het blok wordt in haardunne secties gesneden, op glasplaatjes geplaatst, gekleurd en onder een lichtmicroscoop onderzocht. De methode van formaline-gefixeerd, in paraffine ingebed (FFPE) is goedkoop, betrouwbaar en kan monsters decennialang bij kamertemperatuur bewaren. Daardoor liggen er wereldwijd miljoenen FFPE-monsters opgeslagen in biobanken, die alles ondersteunen van fundamentele biologie tot geavanceerde genetische en proteïnestudies, en die de ruggengraat vormen van moderne diagnostiek en prognose.
Waarom gewone microscopen niet meer volstaan
Traditionele optische microscopen worden begrensd door de fysica van licht: details kleiner dan ongeveer 250 nanometer vervagen. Veel ziektagerelateerde structuren — zoals de fijne filters in de nieren, de verbindingen tussen zenuwcellen, of microscopische wijzigingen in de DNA-architectuur in de kern — vallen onder deze grens. De huidige werkwijze combineert vaak standaard lichtmicroscopie voor een globaal overzicht met elektronenmicroscopie voor nanometerschaaldetails, maar die aanpak is traag, duur en vereist totaal andere preparatie van monsters. Klinici en onderzoekers zoeken daarom naar een enkel, flexibel systeem dat grote gebieden snel kan scannen en tegelijk kan inzoomen om nanoschaalsoorten te zien in dezelfde FFPE-secties die ze al gebruiken.
Nieuwe manieren om het beeld te verscherpen
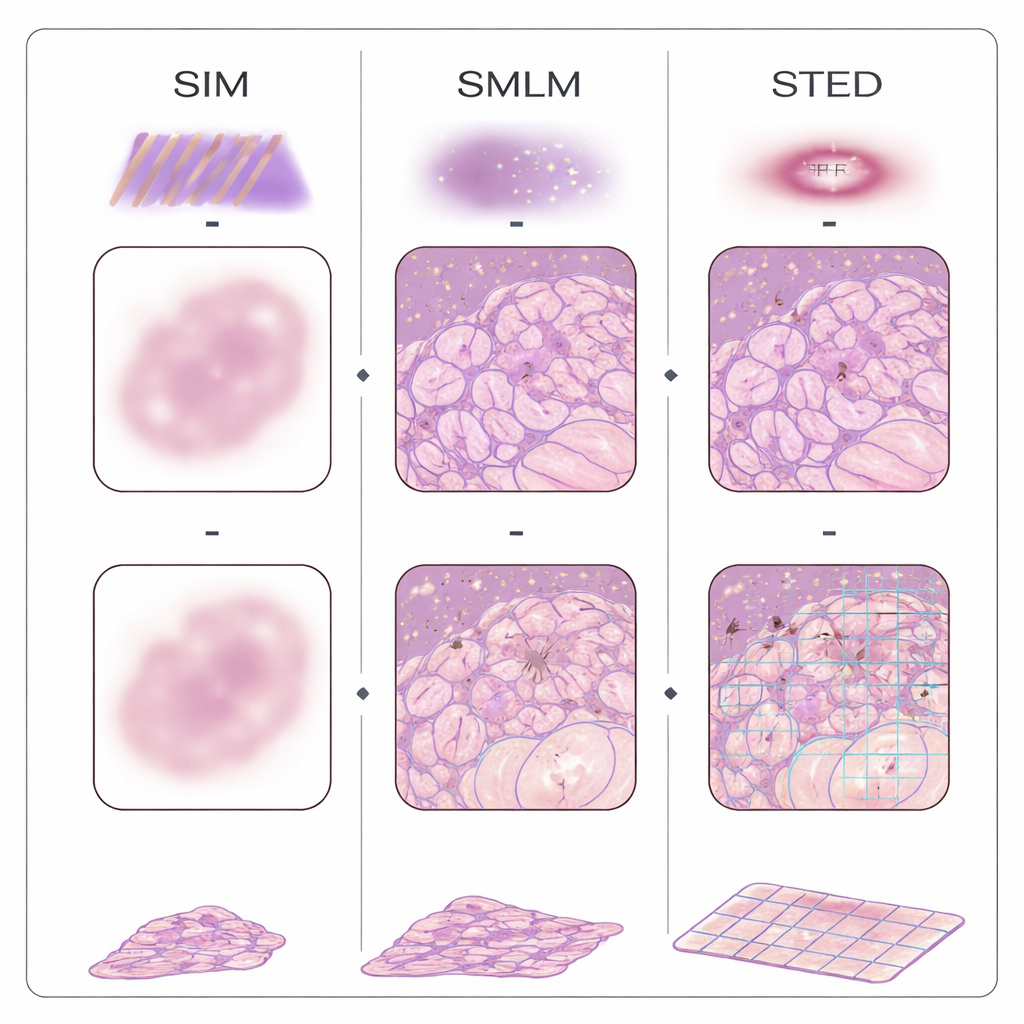
In de afgelopen twee decennia hebben meerdere families van "superresolutie"-microscopen de traditionele resolutiebarrière doorbroken met fluorescentie en slimme optiek. Single-molecule-localisatiemethoden schakelen moleculen aan en uit en bepalen hun posities één voor één; gestructureerde illuminatie projecteert gestreepte lichtpatronen op het weefsel en gebruikt berekening om fijnere details te reconstrueren; gestimuleerde emissie‑depletie snijdt een klein oplichtend punt uit met een donutvormige bundel; en fluctuaties gebaseerde benaderingen analyseren subtiele flikkeringen in het beeld om structuur af te leiden. Een andere strategie, expansiemicroscopie genoemd, omzeilt complexe optiek door het weefsel fysiek op te zwellen in een gel, zodat gewone microscopen voorheen onzichtbare details kunnen zien. Deze methoden zijn al toegepast op FFPE-monsters van borst, dikke darm, alvleesklier, nier, hersenen, huid, placenta en andere organen, en tonen hoe mitochondriën in tumoren veranderen, hoe nierfilters falen en hoe eiwitophopingen zich vormen bij de ziekte van Alzheimer.
Hobbels op weg naar dagelijks gebruik
Ondanks hun potentie zijn deze technieken nog niet klaar om routine-instrumenten in de meeste pathologielabs te worden. Veel superresolutiesystemen zijn traag, bestrijken slechts kleine velden of vereisen tienduizenden afbeeldingen om één gedetailleerd beeld op te bouwen, wat onpraktisch is wanneer een patholoog grote weefselgebieden moet beoordelen. FFPE-weefsels zelf zijn optisch uitdagend: ze verstrooien licht, geven autofluorescentie en kunnen de moleculen verbergen die gelabeld moeten worden, wat leidt tot vage beelden of valse structuren. Sommige methoden vragen om speciale kleurstoffen, maatwerkmengsels of meerstapschemische behandelingen die moeilijk in standaardhistologieworkflows passen. Daarbovenop zijn commerciële instrumenten kostbaar en complex in gebruik, en de resulterende data vragen zware rekenkundige verwerking en opslag.
Samensmelting van slimme optiek en slimme software
Om deze obstakels te overwinnen combineren onderzoekers verbeterde optiek met labelvrije beeldvorming en kunstmatige intelligentie. High-throughput, diffractie‑gelimiteerde methoden zoals Fourier-ptychografie en niet-lineaire optische microscopie kunnen snel grote, zelfs ongekleurde, FFPE-secties scannen en kwantitatieve kaarten van weefselstructuur leveren. Digitale pathologieplatforms leggen nu hele objectglaasjes vast op hoge resolutie en gebruiken machinaal leren om tumoren te detecteren en biomarkers zoals HER2, Ki‑67 en PD‑L1 te scoren. Deep‑learningmodellen kunnen zelfs laagresolutiebeelden omzetten in superresolutiebeelden, wat mogelijk de noodzaak van sommige gespecialiseerde hardware vermindert en beter gebruikmaakt van bestaande bioptenarchieven.
Wat dit betekent voor toekomstige patiënten
De auteurs concluderen dat ware "superresolutie‑histologie" van FFPE-monsters — die nanometerschalige details, hoge snelheid, redelijke kosten en compatibiliteit met huidige labroutines combineert — nog niet volledig is gerealiseerd, maar binnen bereik ligt. Naarmate optische methoden sneller en robuuster worden en AI‑gebaseerde analyse volwassen wordt, kunnen deze instrumenten subtiele vroege veranderingen in weefsels onthullen die nu onopgemerkt blijven, de nauwkeurigheid van diagnoses verbeteren en meer gepersonaliseerde behandelbeslissingen sturen. Op de lange termijn zou het omzetten van elk gearchiveerd wasblok in een high-definition kaart van ziekte zowel onderzoek als klinische zorg kunnen transformeren.
Bronvermelding: Villegas-Hernández, L.E., Dubey, V.K., Acharya, G. et al. Optical super-resolution histology of formalin-fixed paraffin-embedded tissue samples: challenges and opportunities. Nat Commun 16, 9760 (2025). https://doi.org/10.1038/s41467-025-64626-1
Trefwoorden: superresolutiemicroscopie, FFPE-weefsel, digitale pathologie, optische beeldvorming, kankerdiagnostiek