Clear Sky Science · nl
Nanozymen die de grenzen van biokatalyse verleggen
Kleine hulpmiddelen die chemie versnellen
Van bierbrouwen tot het verteren van avondmaal: ons leven hangt af van onzichtbare hulpjes, katalysatoren, die chemische reacties versnellen. Meer dan een eeuw lang dacht men dat de katalysatoren in de biologie alleen fragiele eiwitten en later katalytische RNA-moleculen waren. Deze review introduceert “nanozymen” – kleine, ontworpen deeltjes die zich als enzymen gedragen maar zijn opgebouwd uit robuuste materialen zoals metalen, oxiden en koolstof. Ze overleven hitte, kou en vijandige omstandigheden en beginnen onze opvatting over chemie in levende systemen, ziekte, industrie en zelfs het ontstaan van het leven te veranderen.
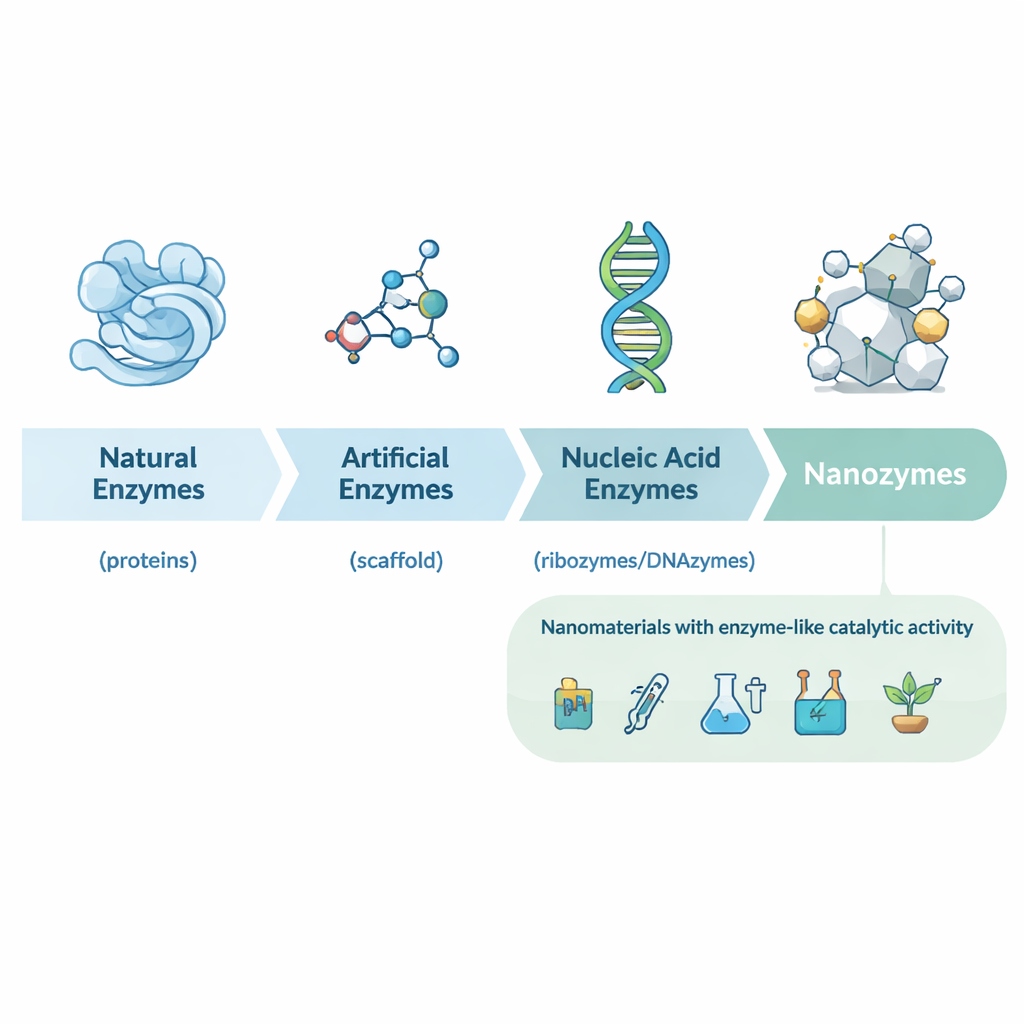
Van natuurlijke enzymen naar ontworpen nanokatalysatoren
Het artikel beschrijft eerst de geschiedenis van biokatalyse, van vroege ontdekkingen van proteïne-enzymen in gist en maagzuur tot ribozymen (katalytisch RNA) en een breed scala aan kunstmatige enzymen opgebouwd uit kleine moleculen en antilichamen. Deze traditionele katalysatoren zijn krachtig maar vaak duur, onstabiel en moeilijk in massaproductie. Begin jaren 2000 ontdekten onderzoekers dat sommige nanomaterialen – bijvoorbeeld ijzeroxide-nanodeeltjes – het gedrag van klassieke enzymen zoals horseradish-peroxidase kunnen nabootsen. Dit leidde tot het concept van nanozymen: nanometer-schaal deeltjes waarvan de eigen structuur enzymachtige activiteit geeft, in plaats van een gebonden eiwit of kleine-molecuulkatalysator.
Wat nanozymen anders maakt
In tegenstelling tot enzymen, die één precies gevormd actief 'pocket' hebben, tonen nanozymen veel actieve plekken over hun oppervlak. Deze plekken kunnen zich bevinden aan kristalranden, defecten of interfaces tussen twee materialen, en samen kunnen ze veel moleculen tegelijk omzetten. Een enkel actief centrum op een nanozyme is doorgaans minder efficiënt dan dat van een enzym, maar één nanodeeltje kan duizenden van zulke centra herbergen, zodat de totale katalytische kracht kan concurreren met of zelfs groter zijn dan die van natuurlijke enzymen. Hun activiteit kan ook worden bijgesteld door grootte, vorm, chemische doping en oppervlaktecoatings te veranderen – vergelijkbaar met het aanpassen van de architectuur en bedrading van een klein machientje. Omdat ze uit robuuste vaste stoffen in plaats van fragiele gevouwen eiwitten bestaan, blijven nanozymen werken bij hoge en lage temperaturen of hoge zoutconcentraties die de meeste enzymen snel zouden uitschakelen.
Hoe nanozymen werken en hoe ze worden gemeten
De auteurs tonen aan dat nanozymen vaak dezelfde basale kinetische regels volgen die biochemici voor enzymen gebruiken, zoals Michaelis–Menten-gedrag, waarbij de reactiesnelheid afhangt van hoe gemakkelijk een katalysator zijn substraat bindt en omzet. Er zijn echter belangrijke verschillen. Eén deeltje kan meerdere typen actieve centra herbergen, zodat een enkel nanozyme verschillende of zelfs conflicterende reacties kan uitvoeren, zoals zowel het vormen als het afbreken van reactieve zuurstofsoorten. Dit kan complexe “niet-tekstboek” kinetische curven opleveren die meerdere processen verbergen onder één vloeiende trend. De review legt uit hoe onderzoekers deze gedragingen ontleden, inschatten hoeveel actieve sites er werkelijk zijn, en de totale activiteit van verschillende nanozymen vergelijken met gestandaardiseerde eenheden — allemaal cruciaal om een intrigerend materiaal tot een betrouwbaar hulpmiddel te maken.
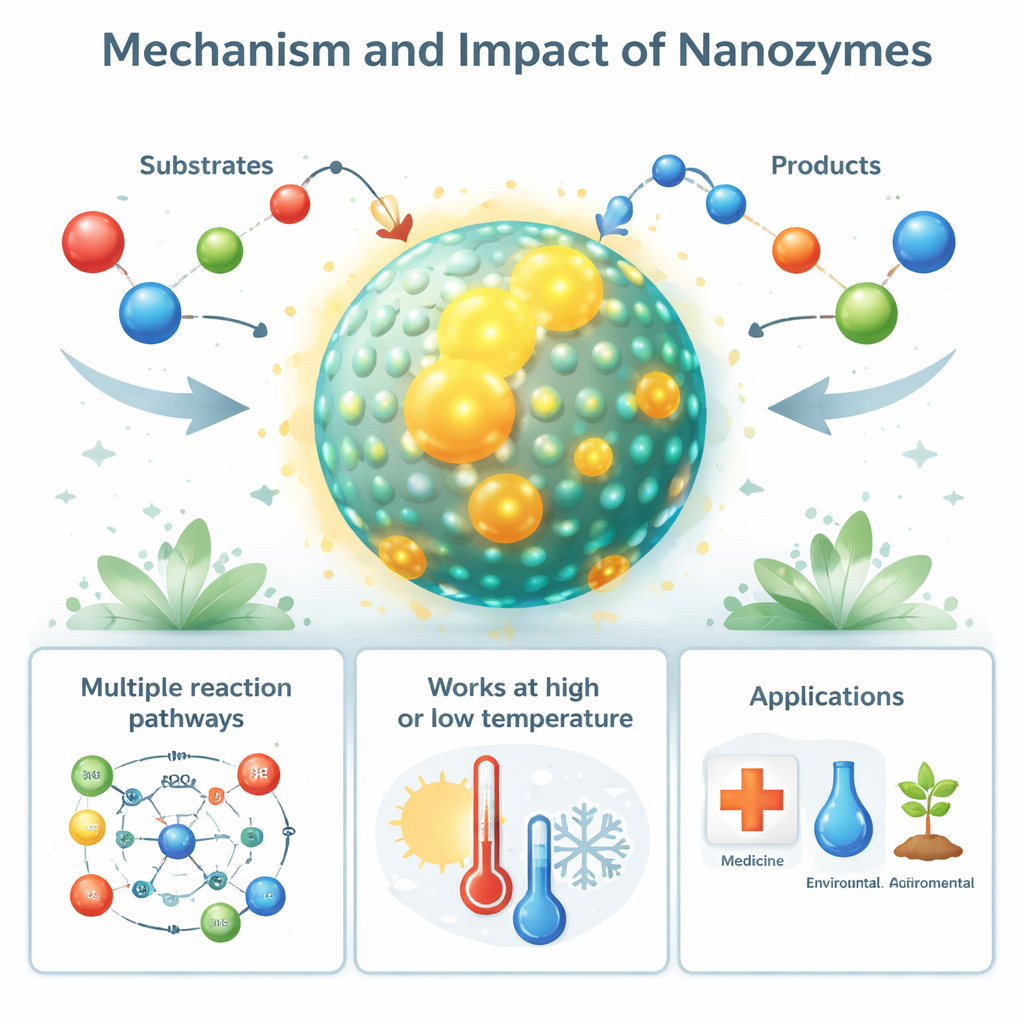
Van natuurlijke nanozymen naar toepassingen in de echte wereld
Intrigerend genoeg beperkt nanozyme-achtig gedrag zich niet tot het laboratorium. Bepaalde biologische nanostructuren, zoals ijzer gevulde proteïnekooien (ferritine) en magnetische deeltjes in bacteriën (magnetosomen), fungeren als natuurlijke nanozymen die helpen schadelijke reactieve zuurstofsoorten te beheersen. Zelfs ziektegerelateerde eiwitvezels, zoals amyloïde afzettingen bij de ziekte van Alzheimer, kunnen peroxidase-achtige nanozyme-activiteit aannemen die omliggende cellen beschadigt. Aan de toegepaste kant worden synthetische nanozymen gebruikt als goedkopere, stevigere vervangers van enzymen in diagnostische tests, biosensoren en industriële assays. Hun vermogen om reactieve zuurstofsoorten te genereren of te verwijderen wordt benut om tumorcellen en bacteriën te doden, weefsels te beschermen tegen oxidatieve stress en gewassen te helpen tegen droogte, zoutbelasting en vervuiling.
De volgende generatie slimme katalysatoren ontwerpen
Vooruitkijkend benadrukken de auteurs kernuitdagingen: het nauwkeurig vaststellen van de exacte atomaire structuren die als actieve centra fungeren, het verbeteren van reactieselectiviteit zodat nanozymen alleen daar en wanneer gewenst werken, en het waarborgen van veiligheid en stabiliteit in het lichaam. Ze wijzen op geavanceerde beeldvorming, kwantumniveau-simulaties en machine learning als krachtige hulpmiddelen om nanozyme-prestaties te voorspellen en te optimaliseren. Omdat nanozymen in extreme omstandigheden kunnen werken, reageren op licht, warmte, geluid of magnetische velden, en soms meerdere reacties achtereen uitvoeren, zouden ze de basis kunnen vormen voor nieuwe therapieën, milieutechnologieën en industriële processen. De review besluit dat nanozymen de definitie van biokatalyse verbreden en wellicht zelfs aanwijzingen bieden over hoe primitieve katalysatoren ooit de chemie van het vroege leven aandreven.
Bronvermelding: Zhang, R., Yan, X., Gao, L. et al. Nanozymes expanding the boundaries of biocatalysis. Nat Commun 16, 6817 (2025). https://doi.org/10.1038/s41467-025-62063-8
Trefwoorden: nanozymen, biokatalyse, nanodeeltjes, enzymimitaties, reactieve zuurstofsoorten