Clear Sky Science · nl
Nanopore-detectie van eiwit- en peptidenconformaties voor point-of-care-toepassingen
Waarom kleine eiwitvormen je volgende controle kunnen veranderen
Nu de bevolking vergrijst, komen ziekten zoals Alzheimer, Parkinson, hartziekten en kanker steeds vaker voor. Veel van deze aandoeningen beginnen wanneer essentiële eiwitten en kleine eiwitfragmenten (peptiden) hun vorm subtiel veranderen, vaak lang voordat symptomen optreden. De huidige klinische tests meten meestal hoeveel van een biomarker aanwezig is, en niet of de vorm ervan normaal of verstoord is. Dit artikel verkent een technologie genaamd nanopore-detectie, die elektrisch de vorm en chemie van individuele eiwitmoleculen kan "voelen", en betoogt dat dit de basis zou kunnen vormen voor toekomstige point-of-care-tests die binnen enkele minuten op een klein apparaat uitgevoerd kunnen worden.
Van eenvoudige bloedtests naar vormbewuste biomarkers
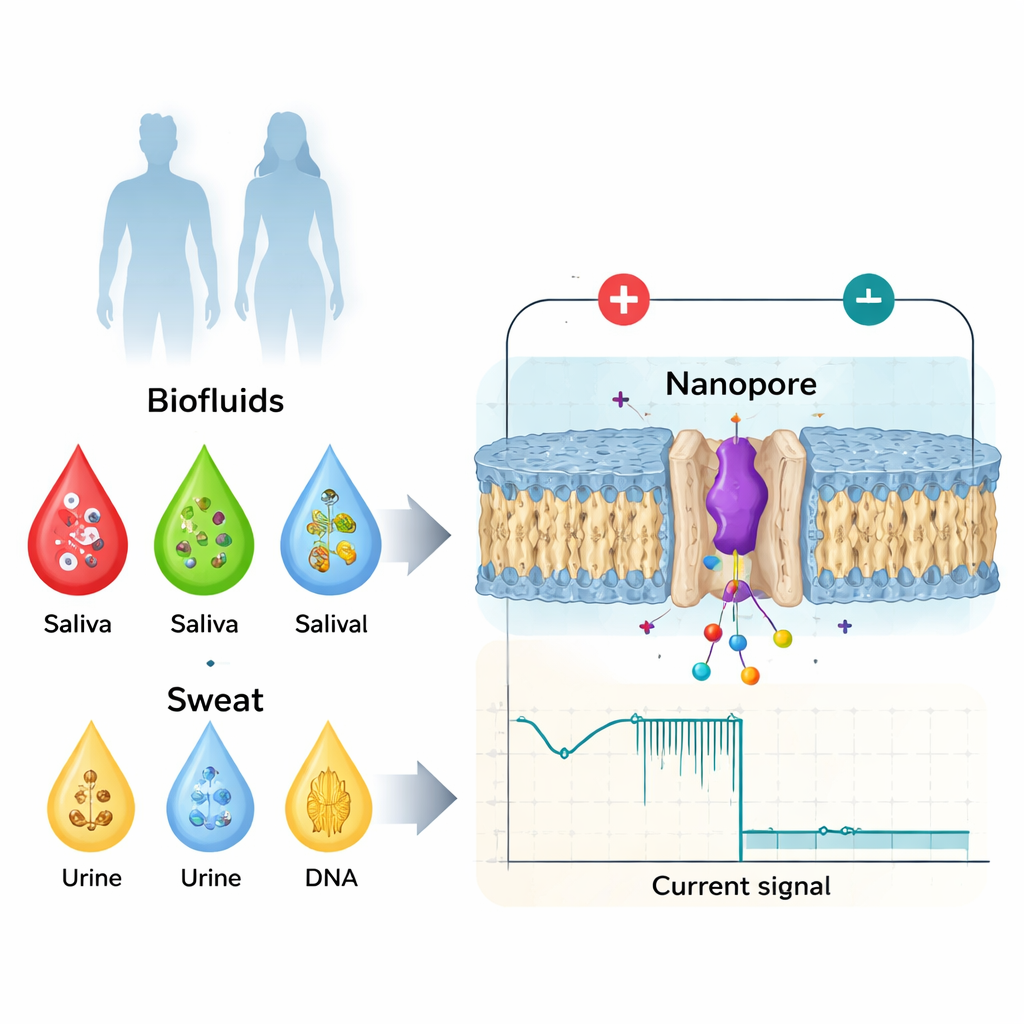
Artsen gebruiken al veel biomarkers afkomstig uit bloed, speeksel, urine of zweet — zoals eiwitten, hormonen of kleine moleculen — om gezondheid en ziekte te volgen. Traditioneel lag de nadruk op grote veranderingen: extra kopieën van een eiwit, beschadigd DNA, of de aanwezigheid van een virale component. Maar de biologie blijkt subtieler. Hetzelfde eiwit kan aan- of uitgezet worden door kleine veranderingen in zijn structuur, door chemische labels die na de vorming worden toegevoegd, of door spiegelbeeldvormen van de bouwstenen. Deze kleine veranderingen kunnen beïnvloeden hoe een eiwit aan partners bindt, klontert of signalen doorgeeft, en worden in verband gebracht met bloedstollingsproblemen, neurodegeneratieve ziekten en kanker. Standaardapparatuur in ziekenhuizen, zoals massaspectrometrie, antilichaamgebaseerde testen en hogeresolutiebeeldvorming, zijn krachtig, maar duur, traag, vereisen hoogopgeleid personeel en kunnen doorgaans niet worden ingezet als snelle, eenvoudige point-of-care-apparaten.
Wat een nanopore anders doet
Nanopore-detectie keert het probleem om. In plaats van te middelen over biljoenen moleculen onderzoekt het techniek één molecuul tegelijk terwijl het door een gaatje in een membraan passeert dat maar een paar miljardsten van een meter breed is. Er wordt een spanning aangelegd zodat ionen door de pore stromen en een constante elektrische stroom creëren. Wanneer een eiwit of peptide de pore binnenkomt, blokkeert het die stroom gedeeltelijk. De diepte van de stroomdaling, hoe lang deze duurt en de fijne details van het signaal hangen af van de grootte, lading en conformatie (de driedimensionale vouwing) van het molecuul. Door de pore zorgvuldig te ontwerpen — met behulp van gemodificeerde eiwitten of vaste-stofmaterialen — kunnen onderzoekers individuele biomoleculen lang genoeg vasthouden om rijke elektrische "vingerafdrukken" te genereren die niet alleen verschillende eiwitten onderscheiden, maar ook subtiele varianten van dezelfde biomarker.
Ziekte-relevante veranderingen lezen, molecuul voor molecuul
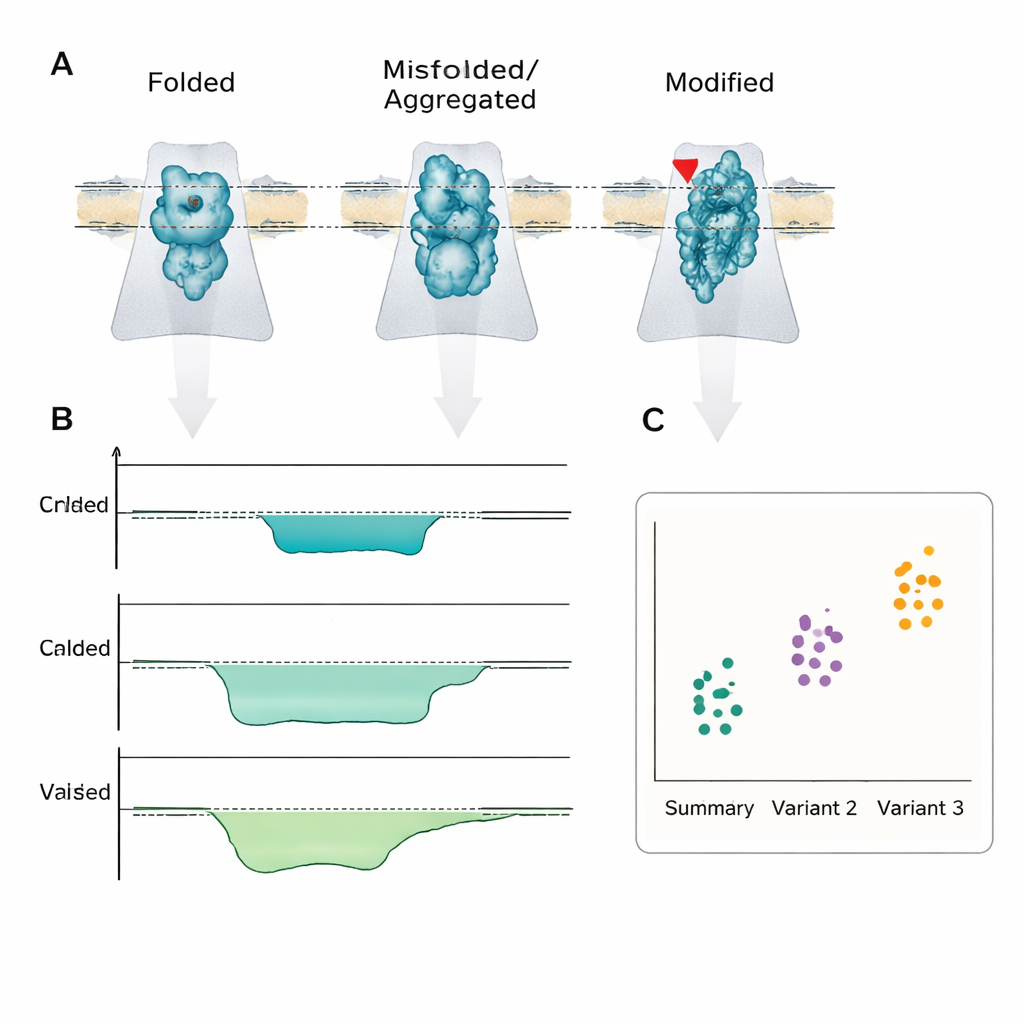
De review benadrukt hoe nanopores al zijn gebruikt om medisch belangrijke verschillen op te lossen die andere methoden moeilijk zien. Ze kunnen peptiden onderscheiden die slechts in één aminozuur verschillen, ziekte-geassocieerde varianten van hemoglobine direct uit bloed detecteren en korte hormoonachtige peptiden onderscheiden die slechts in één bouwsteen variëren of zelfs in de spiegelbeeldvorm van die bouwsteen. Nanopores kunnen ook post-translationele modificaties waarnemen — kleine chemische labels zoals fosfaat-, suiker- of sulfaatgroepen — die helpen bepalen of eiwitten die betrokken zijn bij Alzheimer, Parkinson, bloedstolling of kanker zich normaal of pathologisch gedragen. In sommige experimenten wordt een enkel enzym of bindingsproteïne binnen de pore vastgehouden, en veranderingen in het elektrische signaal onthullen in realtime hoe het aan partners bindt of reacties uitvoert, waardoor mogelijk defecte pathways in ziekte zichtbaar worden.
Op weg naar snelle bedzijde-tests
Aangezien elk blokkeringsevenement overeenkomt met één molecuul, kunnen nanopore-apparaten extreem gevoelig zijn en al duizenden kopieën van een biomarker in een complex vloeistofmonster detecteren. De auteurs bespreken strategieën om belangrijke obstakels voor klinisch gebruik te overwinnen: het verhogen van het tempo waarmee zeldzame moleculen worden gevangen, het stabiliseren van membranen of het gebruik van hybride vaste–biologische pores, en het inzetten van machine learning om complexe elektrische patronen automatisch in heldere diagnostische categorieën te classificeren. Ze tonen ook aan hoe indirecte benaderingen — zoals het bevestigen van DNA-tags of bindingspartners — zwakke signalen kunnen versterken of gelijktijdige meting van meerdere biomarkers mogelijk maken, terwijl veel van de conformationele details behouden blijven die nanopores uniek maken.
Wat dit voor patiënten kan betekenen
De kernboodschap is dat ziekte vaak minder wordt bepaald door de hoeveelheid eiwit en meer door welke vorm of chemische variant aanwezig is. Nanopore-detectie is een van de weinige technologieën die deze verschillen rechtstreeks op enkelmoleculair niveau kan lezen, snel en eenvoudig genoeg om te integreren in draagbare apparaten. Hoewel er nog aanzienlijke engineering- en standaardiseringsuitdagingen zijn, stellen de auteurs dat, vergelijkbaar met hoe nanopore-DNA-sequencers hun weg naar de kliniek hebben gevonden, nanopore-eiwit- en peptide-sensoren uiteindelijk snelle bedzijde-tests zouden kunnen leveren die niet alleen aangeven dat er iets mis is, maar ook de exacte moleculaire misvouwing of modificatie achter de aandoening van een patiënt blootleggen.
Bronvermelding: Ratinho, L., Meyer, N., Greive, S. et al. Nanopore sensing of protein and peptide conformation for point-of-care applications. Nat Commun 16, 3211 (2025). https://doi.org/10.1038/s41467-025-58509-8
Trefwoorden: nanopore-detectie, eiwit-biomarkers, point-of-care-diagnostiek, post-translationele modificaties, conformationele ziekten