Clear Sky Science · nl
Classificatie van 34 computationele methoden om ruimtelijk variabele genen te detecteren uit spatially resolved transcriptomics-gegevens
Waarom locatie belangrijk is voor onze genen
Ons lichaam bestaat uit cellen die niet alleen verschillen in functie, maar ook in hun plaats binnen weefsels en organen. Nieuwe "spatial transcriptomics"-technologieën kunnen nu aflezen welke genen actief zijn terwijl ze tegelijk het adres van elke cel op een weefselkaart bijhouden. Deze review legt uit hoe wetenschappers genen detecteren waarvan de activiteit van plaats tot plaats verschilt — zogenoemde ruimtelijk variabele genen — en waarom overeenstemming over hoe die te vinden essentieel is voor het begrijpen van kanker, hersenfunctie en vele andere ziekten.
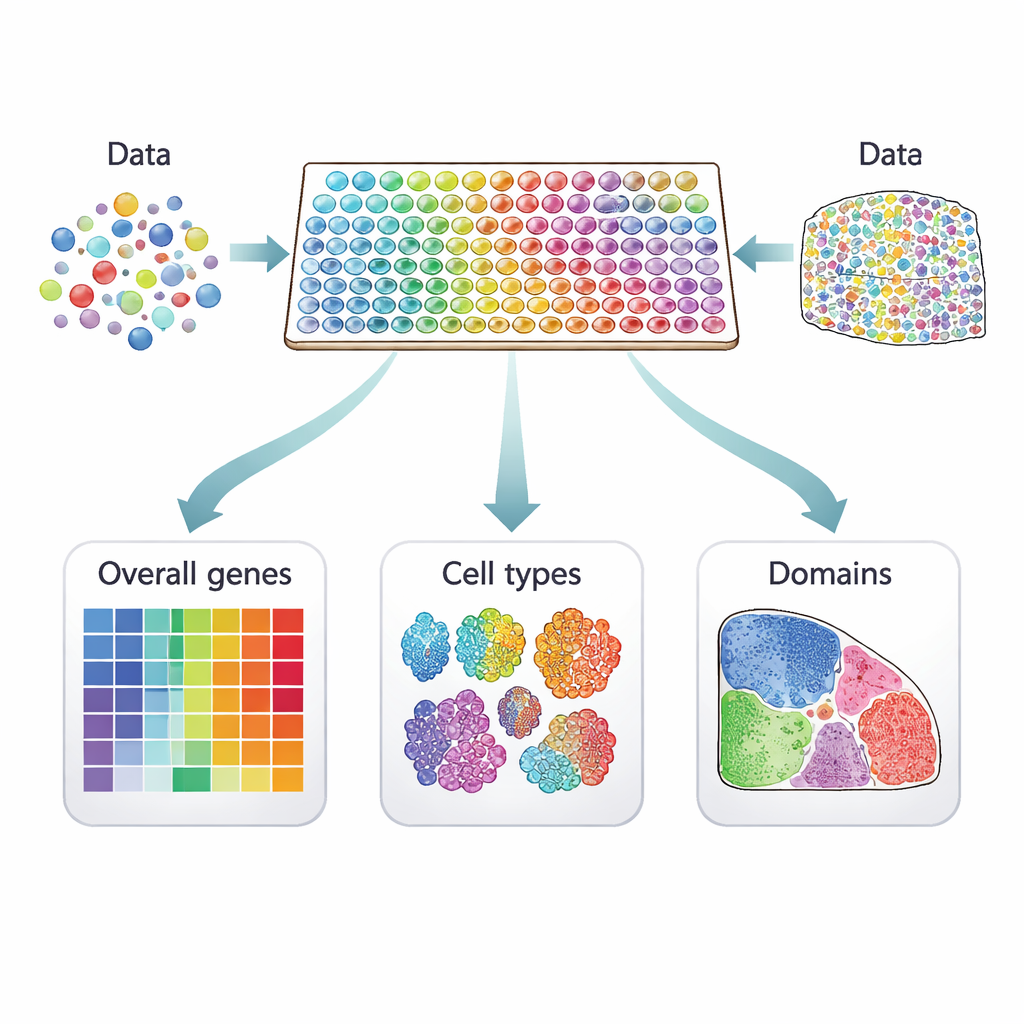
Van verspreide cellen naar levende kaarten
Traditionele single‑cell-studies meten genactiviteit in duizenden individuele cellen, maar verliezen daarbij de informatie over waar die cellen vandaan kwamen. Spatial transcriptomics vult dit gat door genactiviteit direct op dunne weefsellagen te meten. Elke meting is gekoppeld aan een "plek" op de coupe, die afhankelijk van de technologie één cel of meerdere cellen kan bevatten. Beeldgebaseerde methoden lokaliseren enkele honderden gekozen genen met zeer hoge ruimtelijke resolutie, terwijl sequencing-gebaseerde platforms bijna alle genen vastleggen maar met lagere resolutie. Samen veranderen deze benaderingen een weefseldoorsnede in een kleurrijke kaart van genactiviteit die verborgen structuren kan onthullen, zoals lagen in de hersenen of regio’s binnen een tumor.
Drie soorten locatiegevoelige genen
Veel computationele methoden zijn voorgesteld om genen te selecteren die betekenisvolle patronen laten zien op zulke weefselkaarten, maar ze zoeken niet allemaal naar hetzelfde. De auteurs verdelen 34 huidige methoden in drie duidelijke categorieën. De eerste groep zoekt naar "algemene" ruimtelijk variabele genen, waarvan de activiteit zich op niet‑willekeurige wijze over het weefsel verandert — mogelijk in strepen, clusters of gradiënten. De tweede groep richt zich op ruimtelijke genen die specifiek zijn voor een celtype en binnen één soort cel variëren, wat helpt bijvoorbeeld subtypes van neuronen of verschillende toestanden van immuuncellen te onderscheiden. De derde groep zoekt naar "domein‑marker"-genen die sterk aanstaan in bepaalde regio’s of lagen en daardoor nuttige merkers vormen voor die weefselzones.
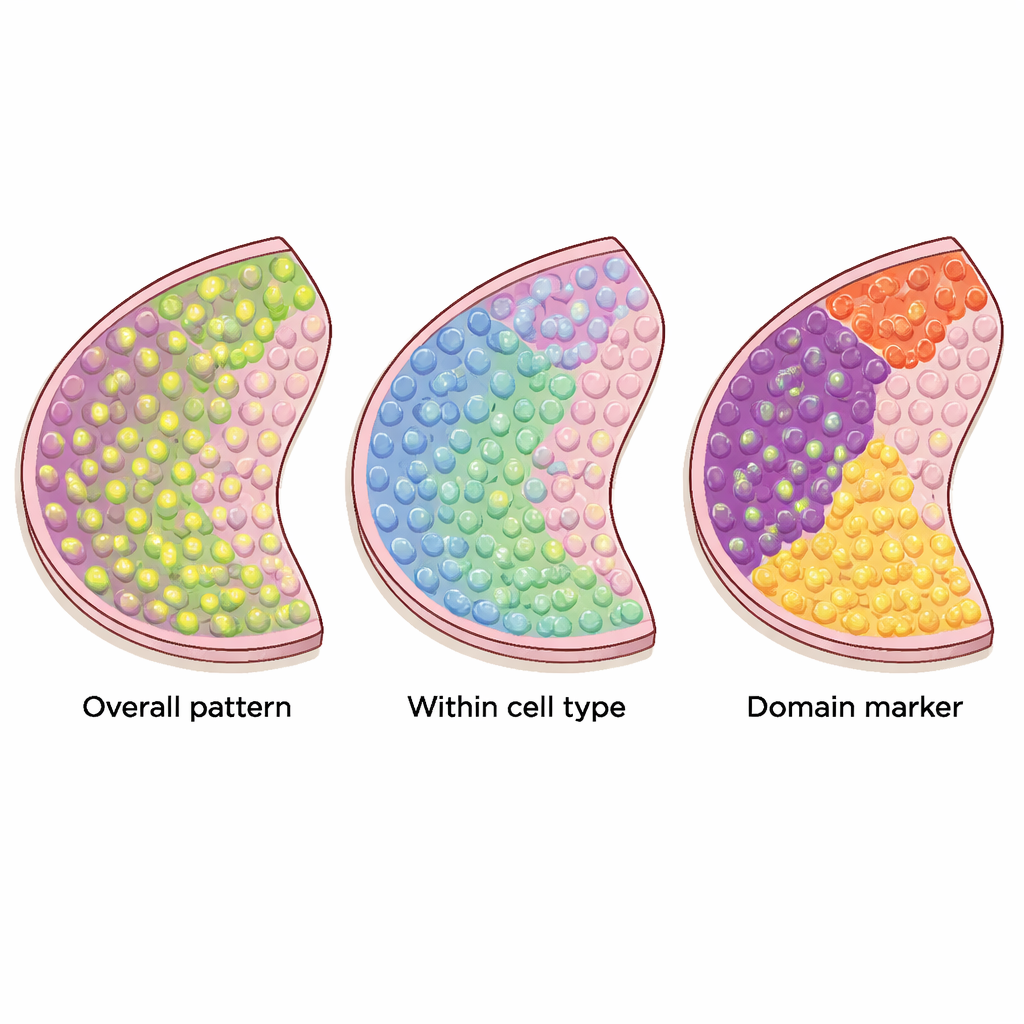
Verschillende tools voor verschillende patronen
De review licht toe hoe deze methoden onder de motorkap werken. Sommige behandelen de weefselcoupe als punten in een regulier tweedimensionaal vlak en gebruiken wiskundige "kernen" om naar patronen te zoeken zoals vlekken of golven. Andere leggen eerst nabijgelegen locaties vast in een netwerk, of graaf, en onderzoeken dan of hoge expressie de neiging heeft te clusteren langs de verbindingen van die graaf. Bepaalde tools vertrouwen op formele statistische toetsen met goed gedefinieerde foutkansen, terwijl anderen vooral genen rangschikken op hoe sterk hun patronen opvallen. Methodes die heel specifieke patronen targeten, kunnen krachtig zijn als de data aan hun verwachtingen voldoen, maar ze kunnen onregelmatiger of complexere vormen missen, zoals vaak gezien bij kanker. Er is ook een afweging tussen flexibiliteit en snelheid: sommige benaderingen schalen naar honderdduizenden plekken, terwijl andere moeite hebben met zeer grote datasets.
Wat deze genen kunnen onthullen
Als ruimtelijk variabele genen eenmaal zijn geïdentificeerd, vormen ze het uitgangspunt voor diepere biologische ontdekkingen. Algemene ruimtelijke genen worden vaak als eerste filter gebruikt om het aantal genen te verminderen voordat plekken in "ruimtelijke domeinen" worden gegroepeerd — regio’s waarvan de cellen vergelijkbare expressieprofielen delen. Deze domeinen kunnen samenvallen met bekende weefselstructuren, nieuwe subregio’s suggereren of onderscheidende celbuurten tonen, zoals invasieve randen in tumoren. Domein‑marker‑genen helpen vervolgens verklaren wat elk gebied uniek maakt en kunnen opnieuw gebruikt worden om vergelijkbare structuren in andere monsters te labelen. Intussen beloven celtype‑specifieke ruimtelijke genen een fijner beeld van hoe bepaalde celtypen door een weefsel heen veranderen, wat tumor–immuuninteracties of gespecialiseerde circuits in de hersenen kan verhelderen.
Uitdagingen en de weg vooruit
De auteurs benadrukken dat geen enkele methode voor elke taak het beste is en dat eerlijke vergelijking van tools zorgvuldige afweging vereist over naar welk soort ruimtelijk gen een methode daadwerkelijk zoekt. Ze pleiten voor betere benchmarks met realistische datasets, duidelijkere statistische standaarden om valse ontdekkingen te vermijden, en nieuwe benaderingen die rekening houden met verschillen tussen technologieën en weefseltypes. Voor niet‑experts is de kernboodschap dat ruimtelijk variabele genen platte genlijsten omzetten in levende kaarten die moleculaire activiteit koppelen aan weefselstructuur. Robuuste manieren om deze genen te detecteren en te interpreteren zullen cruciaal zijn om spatial transcriptomics om te zetten in praktische inzichten over ontwikkeling, hersenfunctie en ziekte.
Bronvermelding: Yan, G., Hua, S.H. & Li, J.J. Categorization of 34 computational methods to detect spatially variable genes from spatially resolved transcriptomics data. Nat Commun 16, 1141 (2025). https://doi.org/10.1038/s41467-025-56080-w
Trefwoorden: spatial transcriptomics, ruimtelijk variabele genen, genexpressiepatronen, weefselmicroomgevingen, computationele genomica