Clear Sky Science · nl
Het licht werpen op de impact van N-terminale acetylatie: van eiwit tot fysiologie
Hoe kleine chemische labels het gedrag van eiwitten kunnen veranderen
Elke cel in je lichaam bevat eiwitten die correct moeten vouwen, naar de juiste plaats moeten worden geleid, zich moeten assembleren tot moleculaire machines en verwijderd moeten worden wanneer ze beschadigd raken. Dit overzichtsartikel bespreekt een subtiele maar uiterst veelvoorkomende chemische wijziging aan één uiteinde van veel eiwitten — N-terminale acetylatie — en laat zien hoe deze kleine “dop” helpt bij het regelen van alles van celgroei en stressresponsen tot hartontwikkeling en hersenfunctie.
De eiwitdop die de meesten van ons nooit hoorden
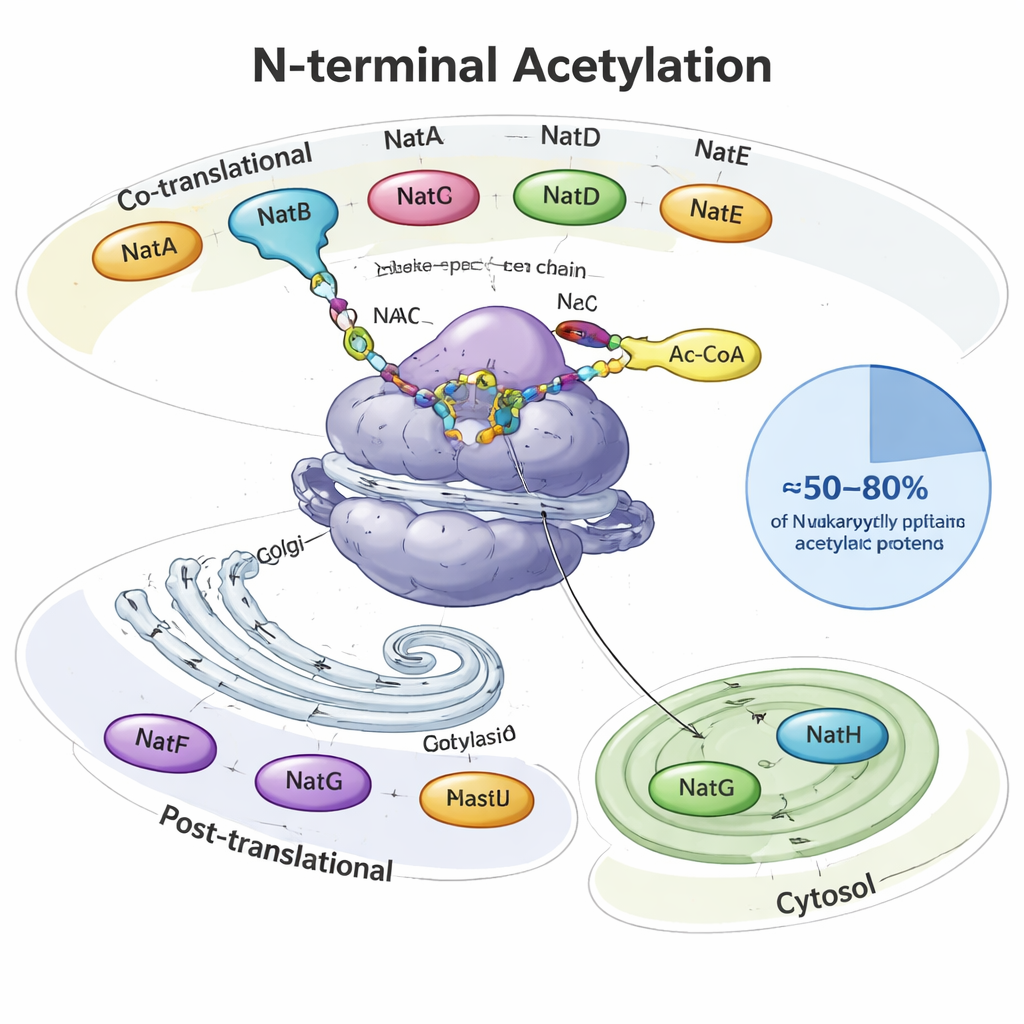
Wanneer een eiwit wordt gemaakt, komt het uit de eiwitfabriek van de cel, het ribosoom, tevoorschijn als een groeiende draad. Helemaal aan het begin — de N-terminus — krijgen veel eukaryote eiwitten een acetylgroep, een klein twee-koolstofs kapje. Gespecialiseerde enzymen, N-terminale acetyltransferases (NATs), voeren dit uit en gebruiken een veelvoorkomend metabool molecuul (acetyl‑CoA) als donor. In gisten, planten en dieren verdelen acht hoofdtypen NATs (NatA–NatH) het werk. Sommige werken terwijl het eiwit nog wordt gesynthetiseerd, andere werken achteraf en zitten op specifieke locaties zoals het Golgi-apparaat of plantplastiden. Samen modificeren ze ruwweg de helft tot vier vijfde van alle cellulaire eiwitten, waarbij elke NAT voorkeursbeginsequenties van twee tot vier aminozuren herkent.
Veel enzymen, elk met hun eigen specialiteit
NatA, NatB en NatC zijn de zwaargewichten; ze werken direct bij het ribosoom en dekken grote delen van het “N-terminale acetyloom.” Alleen al NatA kan ongeveer 40% van de menselijke eiwitten modificeren, meestal die waarvan de eerste methionine is verwijderd. NatB en NatC werken op eiwitten die hun initiële methionine behouden, maar verschillen in de voorkeur voor aangrenzende aminozuren. Andere NATs zijn selectiever: NatD richt zich op slechts enkele histoneiwitten die DNA verpakken, NatF richt zich op transmembraan eiwitten in het Golgi, NatG werkt in plantplastiden, en NatH (NAA80) voltooit een bijzondere tweestaps rijping van actine, een belangrijk onderdeel van het celskelet. Het artikel brengt structurele en biochemische studies samen die tonen hoe hulp-subunits deze enzymen ankeren aan ribosomen of membranen en fijnregelen op welke eiwitten ze inwerken.
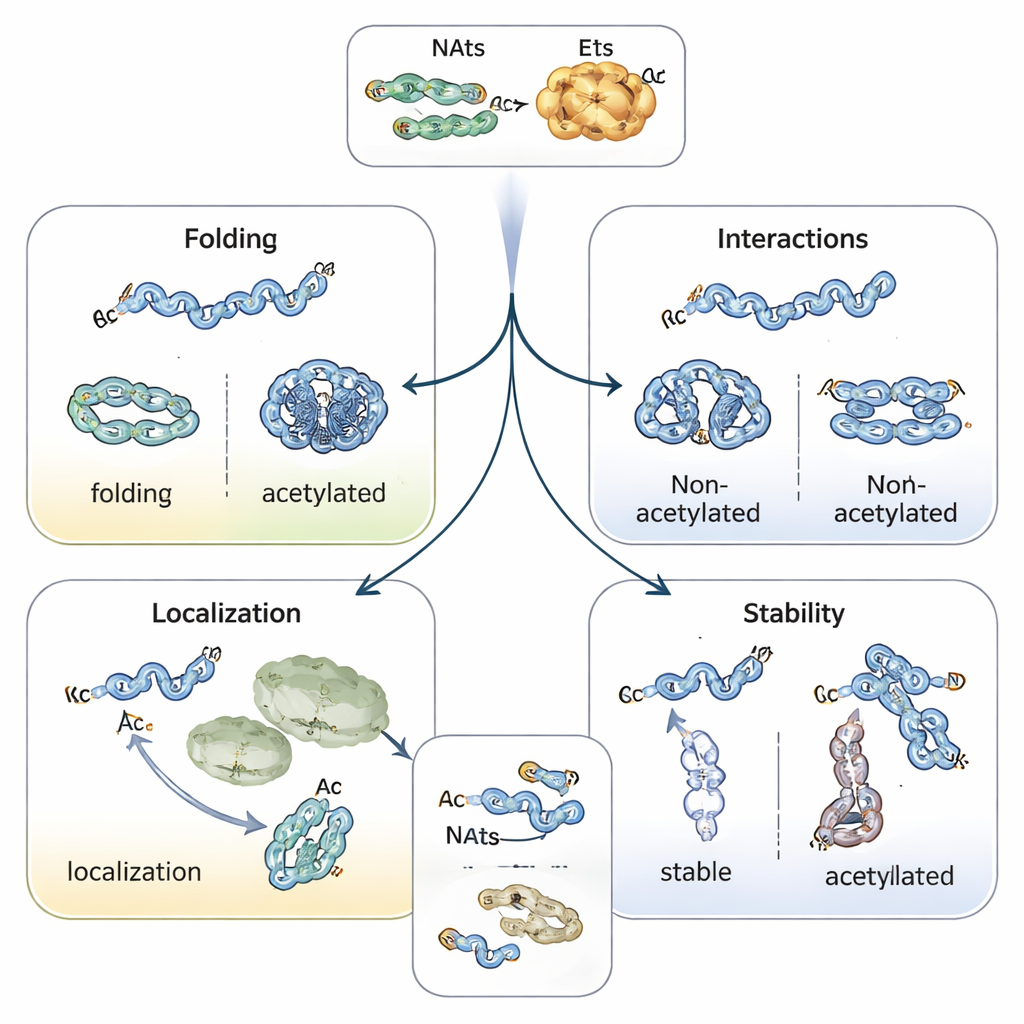
Het sturen van eiwitvouwing, locatie en levensduur
Het toevoegen van een acetylkapje verandert de chemische eigenschappen van het begin van het eiwit, stabiliseert vaak helixstructuren en beïnvloedt hoe eiwitten vouwen. Zo heeft het voor Parkinson geassocieerde eiwit alfa-synucleïne de neiging minder samen te klonteren en een veiligere conformatie aan te nemen wanneer de N-terminus geacetyleerd is. Tropomyosine, een partner van actine, bindt en reguleert actinefilamenten veel beter wanneer het correct is geacetyleerd. In planten en dieren kan N-terminale acetylatie fungeren als een soort adreslabel, dat eiwitten helpt chloroplasten, lysosomen of het Golgi te vinden. Misschien het meest opvallend is de rol ervan bij het bepalen hoe lang eiwitten blijven bestaan: een onbeschermde N-terminus kan door ubiquitine‑taggende enzymen worden gelezen als een “afbraaksignaal”, terwijl acetylatie dat signaal kan maskeren en het eiwit stabiliseert — of in sommige gevallen een conditioneel label kan creëren dat alleen wordt herkend wanneer het eiwit verkeerd gevouwen is of niet in het juiste complex zit.
Van cel-fysiologie tot ontwikkeling en ziekte
Aangezien N-terminale acetylatie zoveel eiwitten raakt, heeft verstoring van NATs brede gevolgen voor hele organismen. Het verwijderen van NatA, NatB of NatC in modelorganismen veroorzaakt vaak ernstige ontwikkelingsafwijkingen, veranderde stressresponsen of zelfs lethale effecten, terwijl meer gespecialiseerde enzymen zoals NatF en NatH smallere problemen geven, zoals hersencalcificaties of gehoorverlies. Bij mensen liggen erfelijke mutaties in meerdere NAT-genen ten grondslag aan zeldzame neuro‑ontwikkelingssyndromen met verstandelijke beperking, hartafwijkingen of spierzwakte. Dezelfde machinerie is vaak overactief in kankers, waar verhoogde NAT-niveaus correleren met een slechtere prognose en mogelijk tumorontwikkeling, metastase en therapieresistentie bevorderen. Veranderingen in N-terminale acetylatie beïnvloeden ook aggregatie‑gevoelige eiwitten zoals alfa-synucleïne en huntingtine, waarmee deze modificatie wordt verbonden met mechanismen van neurodegeneratieve ziekten.
Toekomstige richtingen en medische belofte
De auteurs concluderen dat hoewel we nu de meeste kernenzymen kennen die deze N‑terminale dopjes toevoegen, we nog maar een fractie begrijpen van de specifieke eiwitdoelen en regulerende regels. Een belangrijk thema is dat acetylatie aan het begin van het eiwit het vaak beschermt tegen voortijdige afbraak, terwijl het ook contextafhankelijke signalen voor kwaliteitscontrole creëert. Het aanwijzen welke ubiquitine-ligasen welke N‑terminale patronen lezen, en het ontdekken of enig enzym deze dopjes kan verwijderen, zijn belangrijke open vragen. Omdat NATs op het kruispunt liggen van eiwitstabiliteit, genregulatie en celstressresponses, zijn selectieve NAT-remmers — en mogelijk toekomstige instrumenten die N-terminale acetylatie van specifieke ziekte-gerelateerde eiwitten beïnvloeden — veelbelovende wegen voor nieuwe therapieën bij kanker, hartziekten en neurodegeneratie.
Bronvermelding: McTiernan, N., Kjosås, I. & Arnesen, T. Illuminating the impact of N-terminal acetylation: from protein to physiology. Nat Commun 16, 703 (2025). https://doi.org/10.1038/s41467-025-55960-5
Trefwoorden: eiwitmodificatie, N-terminale acetylatie, eiwitkwaliteitscontrole, neurodegeneratieve ziekte, kankerbiologie