Clear Sky Science · nl
m6A-RNA-methylering moduleren antivirale respons bij coeliakie
Wanneer een virus en gluten de krachten bundelen
Coeliakie wordt vaak gezien als een eenvoudig voedingsprobleem: gluten eten beschadigt je darm. Deze studie laat echter een diepere dynamiek zien, waarbij een veelvoorkomend darminfecterend virus en een klein chemisch merkteken op onze RNA-moleculen samenwerken om het immuunsysteem richting blijvende schade te duwen. Het begrijpen van deze verborgen regellaag kan helpen verklaren waarom slechts sommige mensen coeliakie ontwikkelen en kan wijzen op nieuwe behandelingen die verder gaan dan alleen een glutenvrij dieet. 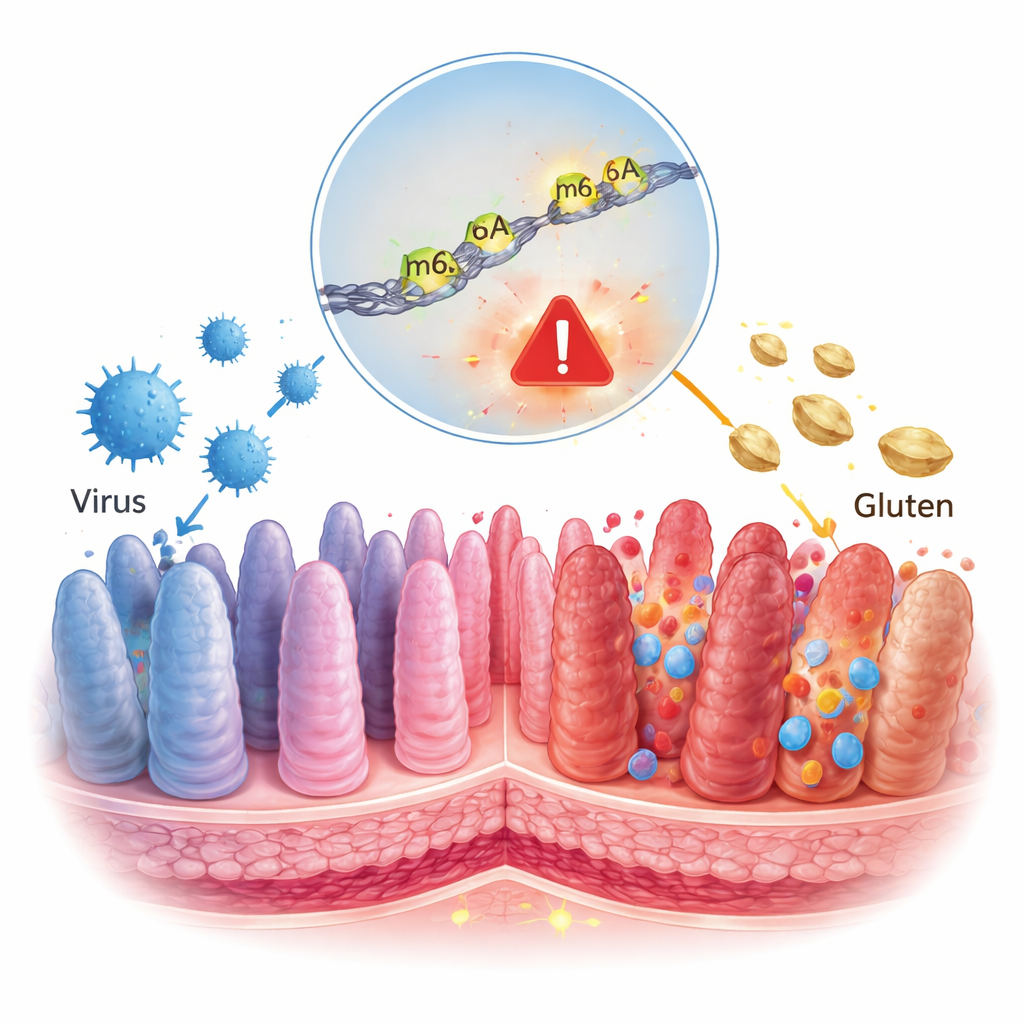
Een verborgen merkteken op onze genetische berichten
Onze cellen lezen continu genen en kopiëren ze naar RNA, korte “berichtjes” die de cel vertellen welke eiwitten gemaakt moeten worden. Deze berichtjes zijn niet statisch; ze kunnen worden versierd met chemische signalen die als markeerpennen werken en bepalen hoe sterk een bericht wordt afgelezen. Een van de meest voorkomende signalen heet m6A, een kleine wijziging in de RNA-letters. Virussen staan erom bekend deze RNA-markeringen in geïnfecteerde cellen te veranderen, en eerder werk koppelde m6A al aan de manier waarop gluten ontsteking in de coeliakiedarm opwekt. De auteurs van dit artikel vroegen zich af of een door een virus veroorzaakte verandering in m6A kan helpen het immuunsysteem van tolerantie voor voedsel naar aanval te laten overslaan.
Bewijs uit patiënten met coeliakie
De onderzoekers keken eerst naar bloed- en darmbiopten van mensen met actieve coeliakie en van niet-coeliakie controles. Ze vonden dat coeliakiepatiënten hogere niveaus van antilichamen tegen reovirus droegen, een dubbelstrengs RNA-virus dat de darm infecteert, wat wijst op frequentere of sterkere blootstelling. In het darmweefsel van deze patiënten waren sleutelgenen voor antivirale waarschuwing, vooral een genaamd IRF7, sterker aangezet, samen met ontstekingsmoleculen zoals STAT1 en de immuuncel-aantrekker CXCL10. Tegelijkertijd was de machinerie die m6A-markeringen toevoegt en afleest actiever, en waren de totale m6A-niveaus op RNA verhoogd. De expressie van antivirale genen steeg en daalde samen met m6A-gerelateerde genen, wat suggereert dat hetzelfde regelsysteem zowel antivirale verdediging als auto-immuunschade kan aansturen.
Hoe gluten het virale alarm versterkt
Om oorzaak en gevolg te onderzoeken bouwde het team een coeliakie-achtig model in darmcellen gekweekt in het laboratorium. Ze bootsten een virale infectie na met synthetisch dubbelstrengs RNA en voegden vervolgens verteerde glutenfragmenten toe die lijken op wat in de darm na een maaltijd zou voorkomen. De virale mimiek verhoogde zowel IRF3 als IRF7, twee hoofdschakelaars voor antivirale responsen. Maar wanneer gluten daar bovenop werd toegevoegd, vertoonde IRF7 een duidelijke extra piek, terwijl IRF3 dat niet deed. De onderzoekers ontdekten dat onder deze omstandigheden m6A-markeringen toenamen op een specifiek gebied binnen het IRF7-RNA en dat dit RNA fysiek interageerde met een m6A-schrijfenzym (METTL3) en een m6A-wisenzym (ALKBH5). Het verhogen van m6A, hetzij door meer METTL3 toe te voegen of door ALKBH5 te verminderen, dreef IRF7-niveaus nog hoger, waarmee de gluten-plus-virussynergie direct werd gekoppeld aan deze RNA-modificatie. 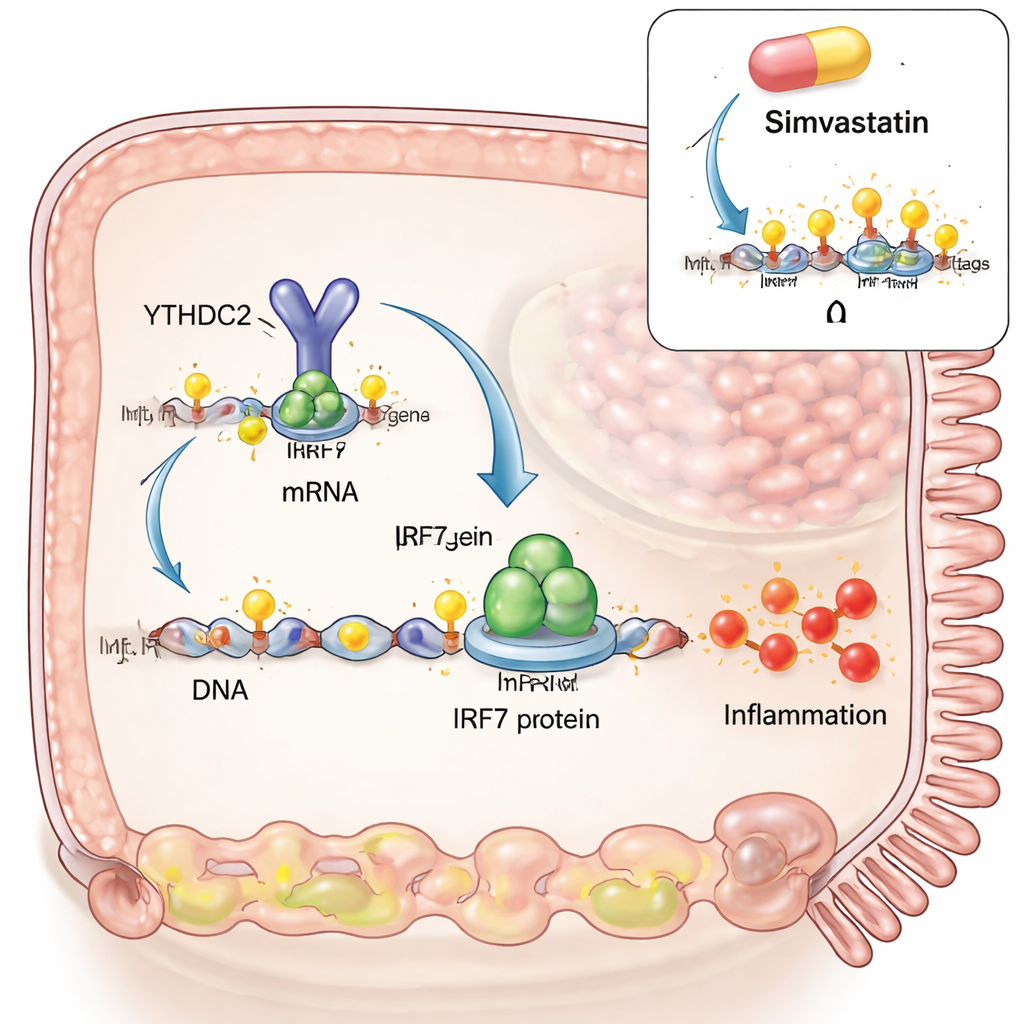
De moleculaire tussenpersoon en een verrassend medicijn
Vervolgens onderzochten de auteurs hoe m6A-markeringen op IRF7-RNA daadwerkelijk het gedrag van de cel veranderen. Ze maakten een versie van het IRF7-RNA met dezelfde eiwitcode maar zonder de m6A-sites. Dit RNA produceerde vergelijkbare hoeveelheden transcript, maar veel minder IRF7-eiwit en het faalde in het activeren van downstream ontstekingsgenen zoals STAT1 en CXCL10. De ontbrekende schakel was een lezer-eiwit genaamd YTHDC2, dat normaal gesproken m6A binnen het coderende gebied bindt en bijdraagt aan efficiënte translatie naar eiwit. Zonder de m6A-sites kon YTHDC2 niet langer aan IRF7-RNA hechten. Het blokkeren van de m6A-schrijver METTL3 in het celmodel verminderde IRF7-eiwit en CXCL10, waardoor de ontstekingsoutput daalde. Een cholesterolverlagend medicijn, simvastatine, dat recentelijk is getoond m6A in andere weefsels te verminderen, verlaagde ook m6A op IRF7-RNA, verminderde IRF7-eiwit in cellen en temperde IRF7-gerelateerde genen in vers verkregen coeliakiedarmbiopten die ex vivo werden gekweekt. Grootschalige vergelijkingen van genexpressie suggereerden dat simvastatine coeliakieweefsel richting een profiel duwt dat meer lijkt op dat van patiënten op een glutenvrij dieet.
Wat dit betekent voor mensen met coeliakie
Dit werk schetst een beeld waarin een darminfectie en gluten samen inwerken op een fijn afgestelde laag van RNA-regulatie. Bij gevoelige mensen lijkt een virale infectie de m6A-taggig van IRF7-RNA in darmcellen te versterken. Blootstelling aan gluten versterkt dat getagde signaal verder, wat leidt tot meer IRF7-eiwit, sterkere antivirale alarmen en hogere niveaus van ontstekingsboodschappers die de auto-immuunreactie op het darmslijmvlies aandrijven. Door m6A-markeringen te verminderen — hetzij genetisch, hetzij met een middel zoals simvastatine — kan de kettingreactie worden verzwakt, althans in laboratorium- en ex vivo-modellen. Voor niet‑specialistische lezers is de kernboodschap dat coeliakie niet alleen gaat over wat je eet, maar ook over hoe infecties en subtiele chemische markeringen op RNA de beslissing van het immuunsysteem om te tolereren of aan te vallen vormgeven. Het gericht benaderen van deze RNA-markeringen zou in de toekomst het glutenvrije dieet kunnen aanvullen en nieuwe behandelingen kunnen inspireren voor een breder scala aan auto-immuunziekten.
Bronvermelding: Sebastian-delaCruz, M., Olazagoitia-Garmendia, A., Pascual-Gonzalez, I. et al. m6A RNA methylation modulates antiviral response in celiac disease. Genes Immun 27, 130–139 (2026). https://doi.org/10.1038/s41435-025-00373-z
Trefwoorden: coeliakie, RNA-methylering, antivirale immuniteit, IRF7, simvastatine