Clear Sky Science · nl
CRISPR-AuNP: fysisch-chemische optimalisatie van een goudnanodeeltjesplatform voor kosteneffectieve en modulaire niet-virale genbewerking in HSPC's
Genbewerking toegankelijker maken voor meer patiënten
Genbewerkingsinstrumenten zoals CRISPR hebben het leven van mensen met erfelijke bloedziekten al veranderd, maar de behandelingen zijn nog duur, technisch veeleisend en grotendeels beperkt tot enkele gespecialiseerde centra. Dit artikel beschrijft een nieuwe manier om CRISPR in bloedvormende stamcellen te krijgen met behulp van kleine goudgebaseerde deeltjes die op een laboratoriumbank in slechts een paar uur kunnen worden gemengd. Het doel is krachtige genbewerkingsbenaderingen eenvoudiger, goedkoper en gemakkelijker inzetbaar te maken op meer plaatsen wereldwijd.
Waarom bloedstamcellen ertoe doen
Bloedvormende stam- en voorlopercellen leven in het beenmerg en vullen voortdurend alle verschillende soorten bloedcellen in het lichaam aan. Als artsen ziekteveroorzakende mutaties in deze cellen veilig kunnen herstellen, zou een éénmalige behandeling een levenslange genezing kunnen bieden voor aandoeningen zoals sikkelcelziekte en bepaalde immuundeficiënties. Vandaag de dag is de meest gebruikelijke manier om CRISPR in deze cellen te krijgen gebaseerd op elektroporatie, een proces dat elektrische pulsen gebruikt om openingen in celmembranen te maken. Hoewel krachtig, is elektroporatie zwaar voor de cellen, vereist het dure apparatuur en gespecialiseerde reagentia, en is het niet eenvoudig te schalen of over te dragen naar gebieden met beperkte middelen. Veiligere virale vectoren zijn uitstekend voor veel gentherapieën, maar minder geschikt voor CRISPR-afgifte omdat ze de bewerkingsinstrumenten te lang blijven produceren, wat het risico op off-target veranderingen verhoogt.
Het bouwen van een klein goudgedragen aflevervoertuig
De onderzoekers wilden een eerder gerapporteerd systeem met goudnanodeeltjes verbeteren dat CRISPR-componenten op het oppervlak droeg. In eerdere ontwerpen werd het RNA dat het CRISPR-knipenzym naar zijn doel leidt direct aan de goudkern verankerd en vervolgens gepaard met het Cas9-eiwit. Dit werkte redelijk goed voor één type CRISPR-enzym maar presteerde slecht met Cas9, dat centraal staat in veel therapeutische strategieën. Door nauwkeurig te onderzoeken hoe Cas9 en zijn gids-RNA zich gedragen onder de zure omstandigheden die tijdens de assemblage van de deeltjes worden gebruikt, ontdekte het team dat het gids-RNA-duplex onstabiel werd op het goudoppervlak, wat leidde tot weinig of geen actief Cas9 dat aan het deeltje was gebonden. Confocale microscopie suggereerde ook dat de polymerencoating die bedoeld was om de deeltjes te helpen ontsnappen uit cellulaire compartimenten losraakte voordat deze zijn werk kon doen.
Stapsgewijze herontwerp van het platform
Om deze problemen te overwinnen bouwden de wetenschappers het systeem van de grond af opnieuw op in drie fasen. Ten eerste vormden ze in plaats van naakt RNA aan het goud te verankeren en daarna eiwit toe te voegen, volledige CRISPR-ribonucleoproteïnecomplexen (eiwit plus gids-RNA) voordat ze in contact werden gebracht met het goudoppervlak. Ze identificeerden een licht zure conditie die deze complexen toestond zich aan de deeltjes te binden terwijl het knipenzym nog actief bleef. Vervolgens omwikkelden ze de geladen deeltjes met speciaal ontworpen polymeren die positief geladen ketens — nodig om uit cellulaire compartimenten te ontsnappen — combineerden met flexibele, waterminnende polyethyleenglycolsegmenten die klontering voorkomen. Door grootte, oppervlaktespanning en eiwitgehalte te meten, toonden ze aan dat ze reproduceerbaar tientallen CRISPR-complexen per deeltje konden laden en toch stabiliteit in oplossing behielden.
De verdediging van de cel kraken
Zelfs met betere belading hadden de deeltjes van de tweede generatie nog steeds moeite met een belangrijke hindernis: het krijgen van CRISPR uit de interne vesikels van de cel en naar het deel van de cel waar het DNA zich bevindt. Het team stemde daarom systematisch de chemie van de polymerelaag af en de verhouding tussen positieve groepen op de polymeer en negatieve groepen op het CRISPR-complex. Ze ontdekten dat het toevoegen van meer korte polyethyleenglycolketens en een gecontroleerd aantal zwavelhoudende ankers zowel de stabiliteit van de deeltjes als het vermogen om endosomale membranen te verstoren verbeterde zonder de cellen te beschadigen. In het uiteindelijke, derdegeneratieontwerp creëerden ze eerst compacte complexen van CRISPR en polymeer en bevestigden deze vervolgens aan geconcentreerde goudkernen. Elektronenmicroscopie toonde een dunne schaal van CRISPR en polymeer rond elke gouden bol, en beeldvorming in levende stamcellen bevestigde dat de lading uit de compartimenten kon ontsnappen en de kern bereikte.
Bewerkingsresultaten met meerdere CRISPR-instrumenten
Om te testen hoe goed de geoptimaliseerde deeltjes werkten, richtten de onderzoekers zich op een gen dat beta-2-microglobuline heet, dat een eiwit produceert dat op het oppervlak van bijna alle bloedcellen voorkomt en eenvoudig meetbaar is met flowcytometrie. Met hun derdegeneratie goudplatform bereikten ze meer dan 10% precieze verstoringen van dit gen in primaire menselijke bloedstam- en voorlopercellen — niveaus die als betekenisvol worden beschouwd voor veel therapeutische toepassingen — terwijl de cellen goed bleven overleven. Hoewel deze efficiëntie lager is dan wat met elektroporatie kan worden bereikt, vereiste het goudsysteem geen gespecialiseerde apparatuur en veroorzaakte het minimale stress voor de cellen. Belangrijk is dat hetzelfde platform met verschillende CRISPR-eiwitten kon worden gebruikt, waaronder Cas9, Cas12a en een nieuwer enzym genaamd Cas12a-M29-1, met vergelijkbare bewerkingsniveaus en geen detecteerbare toxiciteit, wat de modulaire aard van het ontwerp benadrukt.
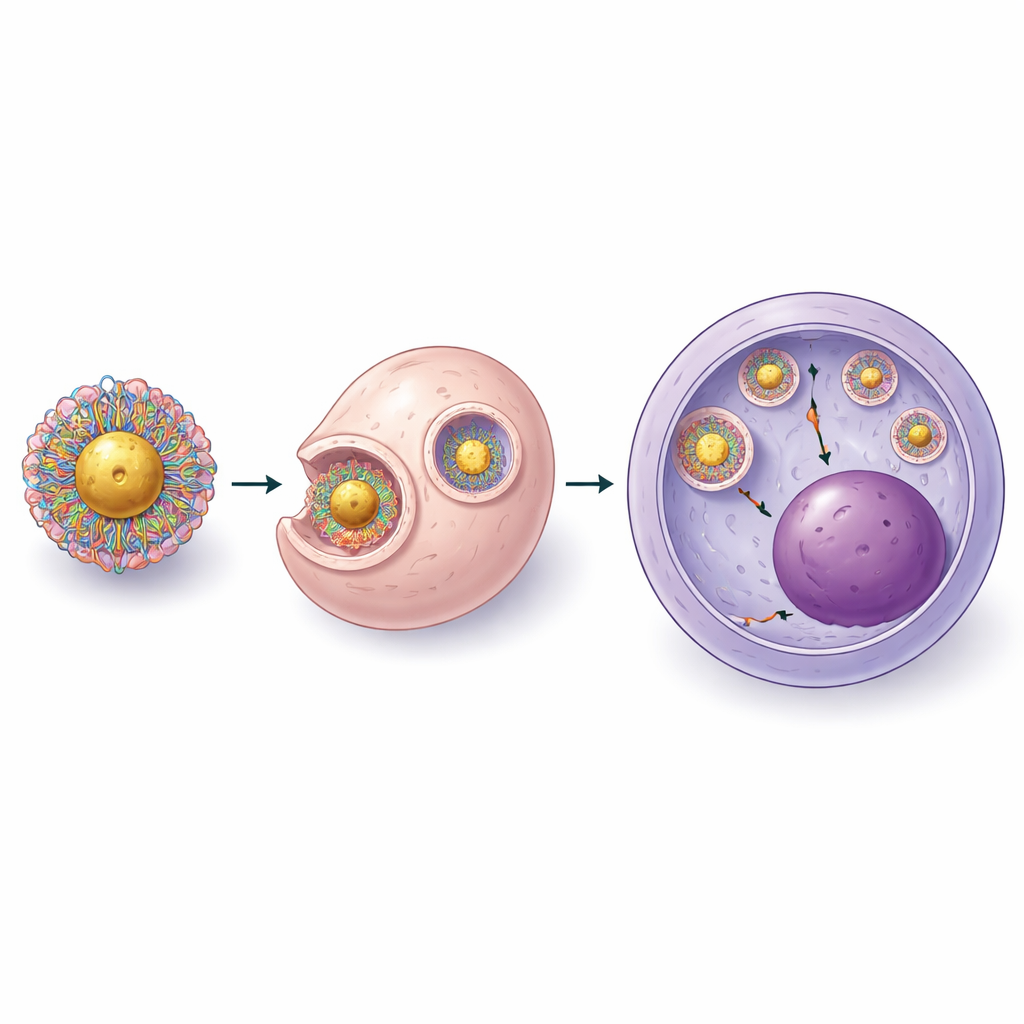
Wat dit kan betekenen voor toekomstige therapieën
Eenvoudig gezegd laat dit werk zien dat het mogelijk is een klein, zorgvuldig ontworpen goudgebaseerd drager te bouwen die CRISPR-instrumenten in gevoelige bloedstamcellen kan brengen zonder elektriciteit of virussen, met kant-en-klare materialen voor minder dan zeventig dollar per miljoen cellen. Hoewel verdere verbeteringen nodig zijn om de efficiëntie van de best beschikbare klinische methoden te evenaren, met name voor ziekten die zeer hoge niveaus van gecorrigeerde cellen vereisen, verlaagt dit op de werkbank samengestelde platform de praktische barrières voor het uitvoeren van geavanceerde genbewerking. Met voortdurende verfijning en veiligheidstesten zouden dergelijke nanodeeltjes kunnen helpen de voordelen van CRISPR-gebaseerde therapieën verder te verspreiden dan gespecialiseerde centra, waardoor curatieve behandelingen wereldwijd beter bereikbaar worden voor patiënten.
Bronvermelding: Gottimukkala, K.S.V., Lane, D.D., Cunningham, R. et al. CRISPR-AuNP: physicochemical optimization of a gold nanoparticle platform for cost-effective and modular non-viral gene editing in HSPCs. Gene Ther 33, 188–202 (2026). https://doi.org/10.1038/s41434-025-00591-0
Trefwoorden: CRISPR-genbewerking, goudnanodeeltjes, hematopoëtische stamcellen, niet-virale aflevering, nanogeneeskunde