Clear Sky Science · nl
Herziening van de genomica van facioscapulohumerale spierdystrofie in het telomeer-tot-telomeer-tijdperk: valkuilen in het verborgen landschap van D4Z4-herhalingen
Waarom dit verhaal over een spierziekte ertoe doet
Facioscapulohumerale spierdystrofie (FSHD) is een van de meest voorkomende erfelijke spierafbraakziekten en verzwakt vaak de spieren van het gezicht en de schouders bij anders gezonde jongvolwassenen. Jarenlang richtten onderzoekers zich op één DNA-stukje vlakbij het uiteinde van chromosoom 4 als de boosdoener. Deze nieuwe studie laat zien dat het beeld veel complexer is: vergelijkbare DNA-herhalingen liggen verspreid over het genoom, en veel standaardlaboratoriumtests kunnen ze niet van elkaar onderscheiden. Inzicht in dit verborgen landschap is essentieel voor een nauwkeurige diagnose, beter onderzoek en uiteindelijk veiliger therapieën.
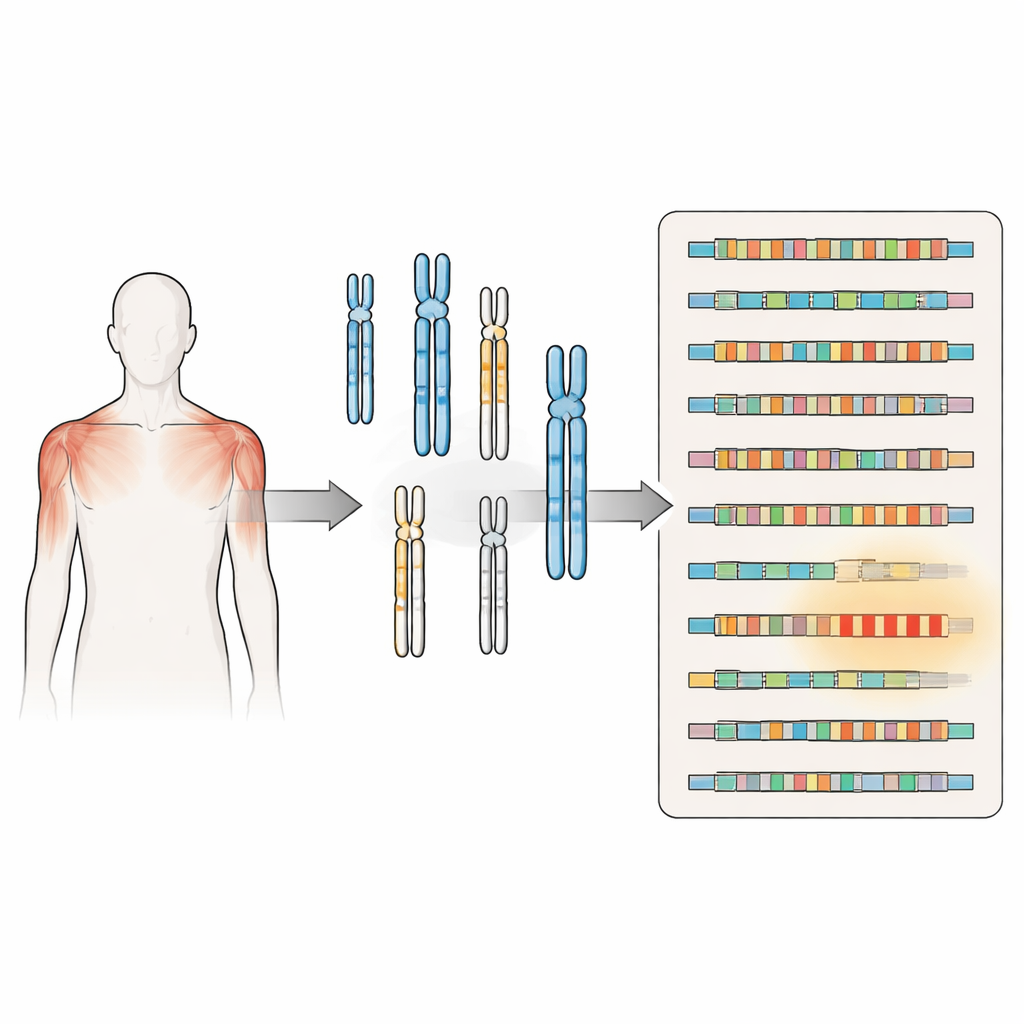
Een nadere keerzijde van een raadselachtige spierziekte
FSHD wordt al lange tijd in verband gebracht met het inkorten van een herhaalde DNA-sequentie die D4Z4 heet, dichtbij het uiteinde van chromosoom 4. Wanneer dit herhalingsgebied onder een bepaalde grootte krimpt en zich op een specifieke genetische achtergrond bevindt, kan dat de productie van een eiwit genaamd DUX4 mogelijk maken, wat spierscellen kan beschadigen. Een tweede vorm van de ziekte ontstaat wanneer genen die dit gebied normaal strak ingepakt en stil houden gemuteerd zijn, waardoor DUX4 ook weer tot expressie kan komen. Beide routes lopen uit op hetzelfde probleem: een gen dat bij volwassen spierweefsel grotendeels uitgeschakeld zou moeten zijn, wordt sporadisch actief en draagt bij aan spierzwakte en -verlies.
Verborgen herhalingen door het hele genoom
Vroege kaarten van het menselijk genoom waren onvolledig, vooral in regio’s rijk aan repetitief DNA bij chromosoomuiteinden en in de buurt van centromeren. Met behulp van de nieuwe telomeer-tot-telomeer menselijke genoomassemblage, die deze gaten opvult, hebben de auteurs het hele genoom opnieuw gescand met de D4Z4-sequentie van chromosoom 4 als zoektemplate. Ze ontdekten clusters en geïsoleerde kopieën van D4Z4-achtige herhalingen op ten minste tien extra chromosomen. Sommige van deze herhalingen zijn structureel compleet en liggen naast signalen die DUX4-achtige RNA’s zouden kunnen stabiliseren, wat suggereert dat ze onder bepaalde omstandigheden verwante eiwitten of RNA-moleculen zouden kunnen produceren.
Wanneer laboratoriumtests meer dan één locatie tegelijk zien
FSHD-onderzoek en -diagnostiek vertrouwen vaak op tests die specifieke DNA- of RNA-fragmenten vermeerderen met korte primersequenties, een strategie die bekendstaat als PCR. Deze primers waren oorspronkelijk ontworpen onder de veronderstelling dat D4Z4-herhalingen alleen op chromosomen 4 en 10 voorkwamen. Door computerpredicties te combineren met experimenten op cellen die enkele menselijke chromosomen dragen, tonen de auteurs aan dat veel gebruikte primersets niet alleen binden aan het ziektelinkt gebied op chromosoom 4, maar ook aan gelijkende herhalingen verspreid over het genoom. Primers gericht op het belangrijkste DUX4-exon of op aangrenzende lange niet-coderende RNA’s vermeerderen vaak producten van meerdere chromosomen tegelijk, waardoor niet meer te achterhalen is waar een bepaald signaal werkelijk vandaan komt.
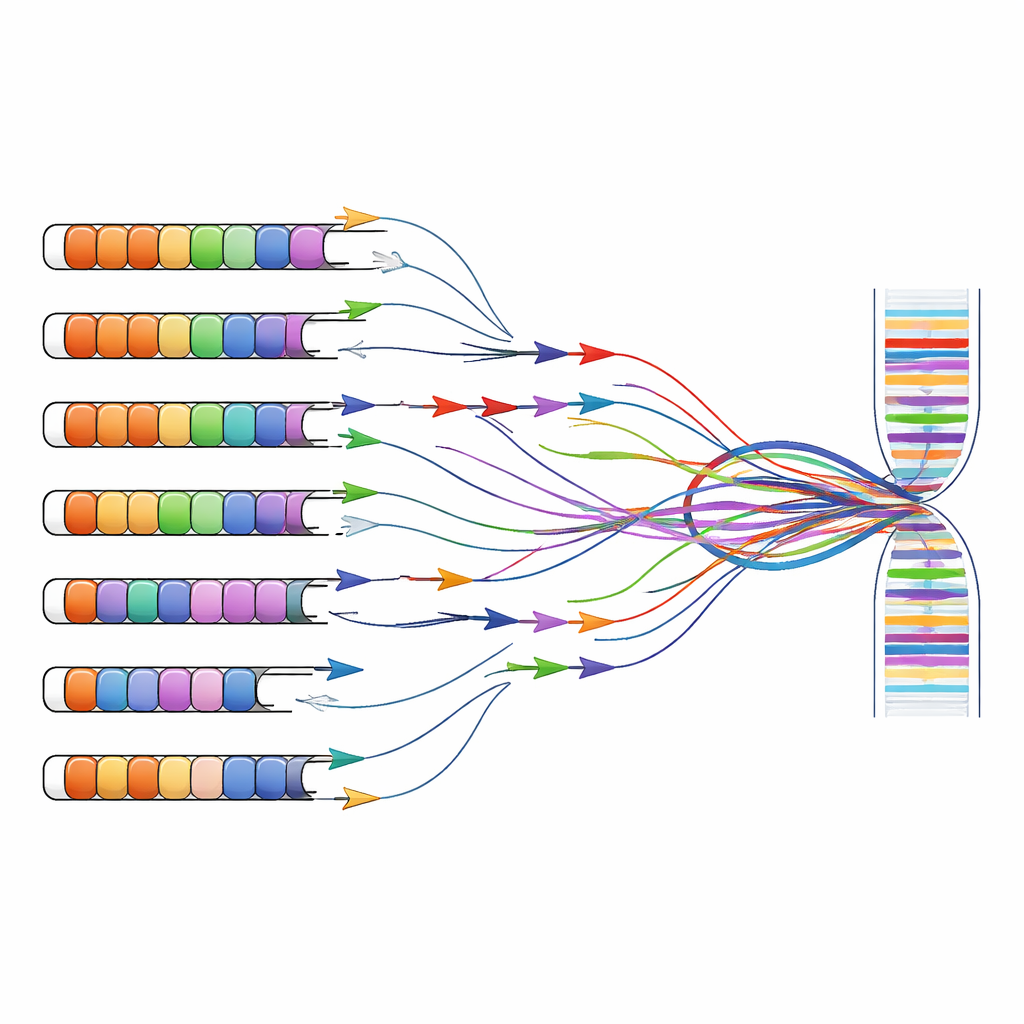
Herziening van diagnostische en onderzoekstools
Dit probleem met meerdere locaties reikt verder dan fundamenteel onderzoek en raakt ook de kliniek. Nieuwere testen die DNA-methylering meten (een chemische markering geassocieerd met genuitschakeling) of die korte-read sequencing gebruiken, verenigen vaak signalen van vele vrijwel identieke herhalingen. Daardoor kunnen metingen van “D4Z4-methylering” of “DUX4-transcripten” in openbare datasets in werkelijkheid een mengsel zijn van bijdragen van chromosoom 4, chromosoom 10 en andere plekken. De auteurs stellen dat om genetische veranderingen correct aan symptomen te koppelen, wetenschappers nu repeat-bewuste methoden moeten gebruiken die individuele loci onderscheiden—bijvoorbeeld lang-read sequencing die volledige herhalingsblokken kan overspannen en hun methyleringspatronen en RNA-producten in hun geheel kan vastleggen.
Wat dit betekent voor patiënten en toekomstige therapieën
De studie ontkracht niet de centrale rol van het ingekorte D4Z4-gebied op chromosoom 4 bij FSHD, maar laat zien dat dit gebied leeft in een drukke buurt van vergelijkbare sequenties. Signalementen die ooit werden verondersteld activiteit op het ziektelocus te bewijzen, kunnen in werkelijkheid deels afkomstig zijn van genomische neven. Voor patiënten betekent dit dat de meest betrouwbare diagnostische tools degenen zullen zijn die fysiek het exacte chromosoom en de betrokken herhalingsarray kunnen onderscheiden, in plaats van alleen te vertrouwen op indirecte metingen. Voor onderzoekers en geneesmidd ontwikkelaars benadrukt het de noodzaak van zeer specifieke ontwerpen die voorkomen dat per ongeluk onschuldige herhalingen elders in het genoom worden gemoeid. In het telomeer-tot-telomeer-tijdperk zal het begrijpen en behandelen van FSHD afhangen van het zien van het volledige herhalingslandschap, niet slechts een enkel herkenningspunt.
Bronvermelding: Salsi, V., Losi, F., Pini, S. et al. Rethinking genomics of facioscapulohumeral muscular dystrophy in the telomere-to-telomere era: pitfalls in the hidden landscape of D4Z4 repeats. Eur J Hum Genet 34, 357–367 (2026). https://doi.org/10.1038/s41431-025-02000-x
Trefwoorden: facioscapulohumerale spierdystrofie, D4Z4-herhalingen, DUX4, telomeer-tot-telomeer-genoom, genetische diagnostiek