Clear Sky Science · nl
Superatomaire moleculen: natuurlijke en niet-natuurlijke atoomachtige binding tussen superatomen
Miniatuurbouwstenen die zich als atomen gedragen
De meesten van ons leren dat atomen de fundamentele bouwstenen van materie zijn. Dit overzichtsartikel laat zien dat groepen van tientallen metaalatomen op zeer kleine schaal zelf kunnen optreden als "super‑atomen", en dat deze superatomen kunnen samenkomen tot "superatomaire moleculen." Door deze ongewone bouwstenen te begrijpen en te ontwerpen, hopen wetenschappers nieuwe materialen te creëren met fijn afgestemde licht-, elektronische en katalytische eigenschappen die gewone moleculen niet kunnen bieden.
Klustera die één atoom nadoen
Superatomen zijn ultrakleine metaalclusters—vaak van goud, zilver of koper—waarbij de elektronen zich ordenen in nette, schilachtige patronen, vergelijkbaar met de schillen in een tekentekening van een atoom. Wanneer die schillen volledig gevuld zijn, bij bepaalde "magische aantallen" elektronen, wordt het cluster bijzonder stabiel. Chemici kunnen deze clusters verder stabiliseren door ze te omhullen met organische moleculen genaamd ligandia, waardoor ze precieze nano-objecten met goed gedefinieerde maten en vormen worden. Veel van deze superatomen zijn bijna bolvormig, en hun stabiliteit is te verklaren met een eenvoudig model waarin de vrije elektronen van het metaal rond draaien alsof ze in een glad, positief geladen druppel zitten.
Wanneer superatomen binden als gewone moleculen
Sommige metaalclusters zijn helemaal niet bolvormig. In plaats daarvan lijken ze op twee of meer samengevoegde superatomen, die vormen wat de auteur superatomaire moleculen noemt. Om deze structuren te verklaren ontwikkelden onderzoekers de "supervalentiebinding"-theorie, die elk superatoom behandelt als een reusachtig atoom met eigen orbitalen, en beschrijft hoe deze orbitalen mengen om gedeelde "superatomaire moleculaire orbitalen" te creëren. In veel gevallen gedragen deze combinaties zich precies als bekende chemische bindingen. Zo kunnen paren goudsuperatomen superatomaire versies vormen van de binding in het fluorwaterstofmolecuul, terwijl complexere fusies analogen van zuurstofmoleculen met hogere bindingsordes geven, of zelfs driecentrumbindingen die aan ozon doen denken. Deze samenstellingen creëren rijke bindingspatronen—enkelvoudig, meervoudig en meercentrum—die de bindregels van de gewone chemie echoën, maar dan op de schaal van clusters met tientallen atomen. 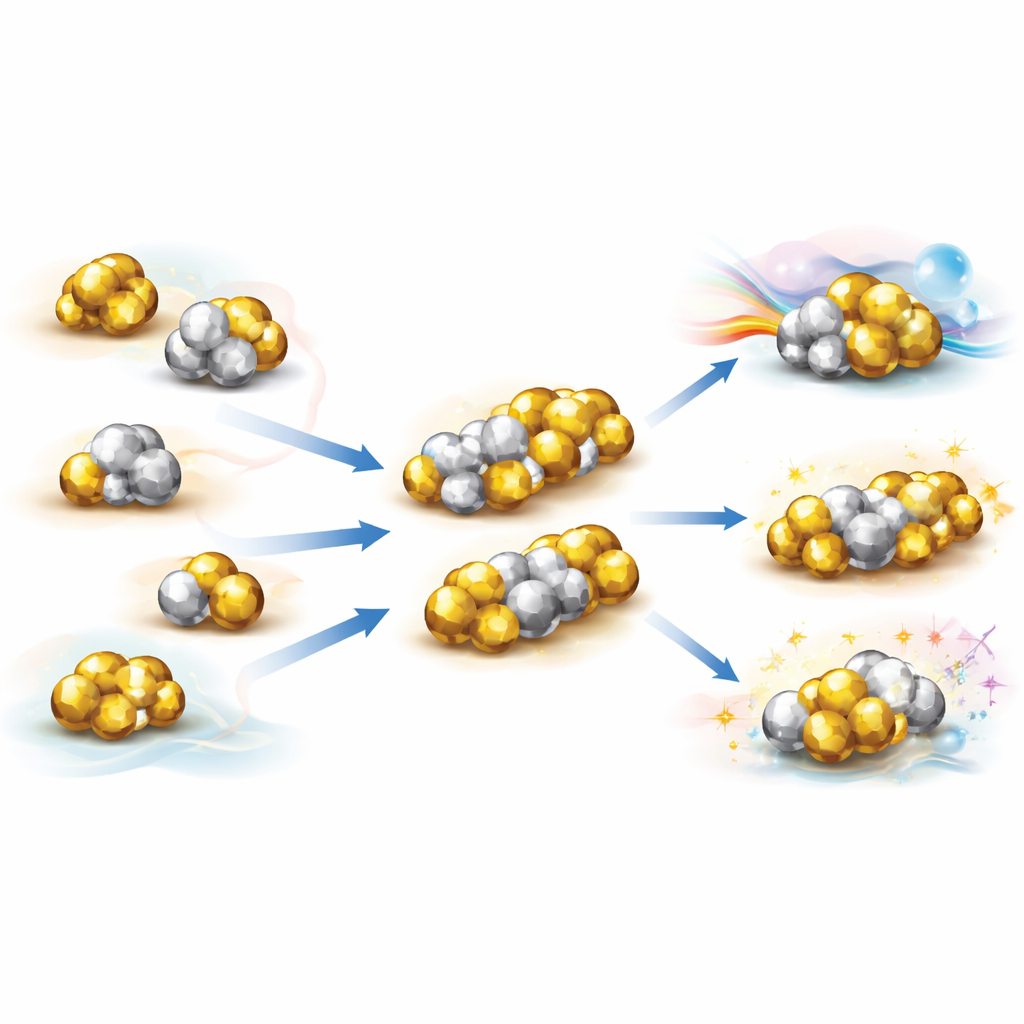
Vreemde bindingen met edelgasachtige eenheden
Superatomaire moleculen beperken zich niet tot nette analogieën met alledaagse bindingen. De review belicht "niet‑natuurlijke" bindingsmotieven waarbij superatomen met gesloten elektronische schillen—vergelijkbaar in geest met edelgassen zoals helium of neon—zich tot grotere structuren voegen, ook al zou er volgens standaard telregels geen binding moeten zijn. In deze systemen kunnen superatomen een enkele metaalatoom delen, rand‑aan‑rand zitten, of zich verbinden tot cyclische en staafachtige assemblages. Formeel is hun bindingsorde nul, maar interacties tussen hun elektronenwolken en de omringende liganden stabiliseren de totale structuur. Opmerkelijk genoeg tonen deze assemblages nieuwe absorptiebanden en andere elektronische kenmerken die afwezig zijn in de geïsoleerde superatomen, wat onthult dat subtiele orbitaalinteracties geheel nieuwe optische reacties kunnen voortbrengen.
Van superringen tot superketens
Het artikel onderzoekt ook meer exotische voorbeelden waarbij superatomen ringen en ketens vormen met collectief gedrag. Een opmerkelijk geval is een goudcluster opgebouwd uit vijf icosaëdrische superatomen gerangschikt in een ring; theoretische studies suggereren dat deze "super‑ring" met het juiste aantal elektronen aromatisch kan worden, waarbij de elektronen zich rond de lus verspreiden op een manier die direct analoog is aan klassieke aromatische moleculen zoals benzeen of het cyclopentadienylion. Een andere familie structuren koppelt kleine drie‑atoom goudunits tot staafvormige ketens. Hoewel de verbindingen tussen naburige eenheden zwak en deels antibindend zijn, werkt het herhalende patroon van interagerende orbitalen als een "superatomaire polymeer," wat leidt tot sterke absorptie in het nabij‑infrarode en wijst op toepassingen in fotothermische en opto-elektronische apparaten. 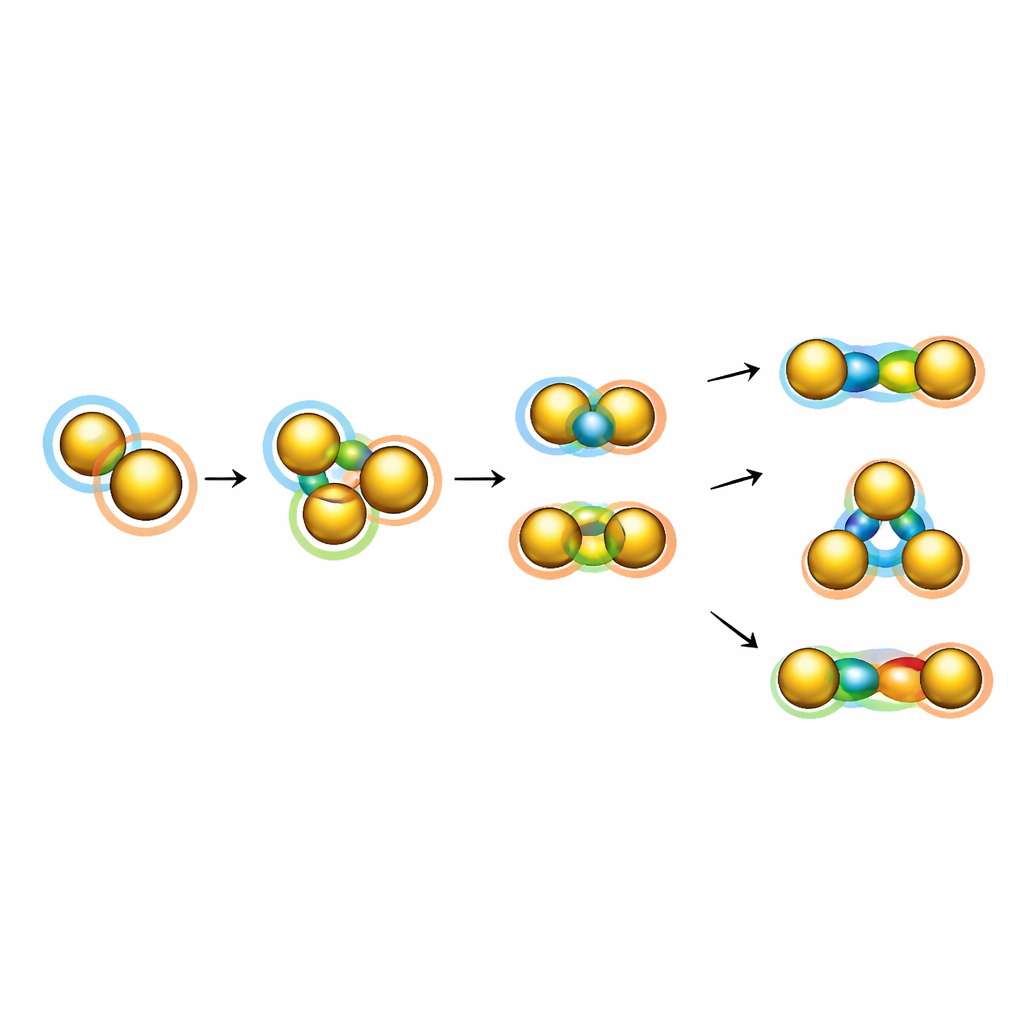
Waarom deze mini‑supermoleculen ertoe doen
Al met al betoogt de review dat het behandelen van metaalclusters als atoomachtige eenheden die kunnen binden tot superatomaire moleculen een krachtig ontwerptaal biedt voor nieuwe materialen. Door te kiezen hoeveel elektronen elk superatoom draagt, hoe ze gekoppeld zijn en welke ligandia hen omringen, kunnen wetenschappers niet alleen stabiliteit ontwerpen maar ook lichtabsorptie, ladingstransport, magnetisme en katalytische activiteit. Natuurlijke‑stijl binding geeft vertrouwde ontwerprichtlijnen, terwijl niet‑natuurlijke en zwak gebonden assemblages gedrag ontgrendelen zonder directe tegenhanger in de gewone chemie. Naarmate dit begrip rijpt, kunnen superatomaire moleculen een gereedschapskist worden voor het vervaardigen van volgende‑generatie katalysatoren, lichtopvangsystemen en elektronische componenten gebouwd uit precies gerangschikte clusters van atomen.
Bronvermelding: Isozaki, K. Superatomic molecules: natural and non-natural atom-like bonding between superatoms. NPG Asia Mater 18, 9 (2026). https://doi.org/10.1038/s41427-026-00636-9
Trefwoorden: superatomen, metalen nanoklustera, superatomaire moleculen, nanomaterialen, opto-elektronische eigenschappen