Clear Sky Science · nl
De strijd tegen cuproptose: van metabole herprogrammering tot therapeutische benutting bij kanker
Wanneer een behulpzaam metaal zich tegen kanker keert
Koper is vooral bekend als onderdeel van elektrische bedrading en loodgieterswerk, maar het stroomt ook stilletjes door onze cellen en helpt enzymen energie te maken en ons tegen schade te beschermen. Dit overzichtsartikel onderzoekt een verrassende wending: onder de juiste omstandigheden kan teveel koper kankercellen in een speciaal soort celdood duwen. Inzicht in dit proces — “cuproptose” genoemd — kan nieuwe manieren openen om tumoren te behandelen die traditionele therapieën hebben weten te ontwijken.
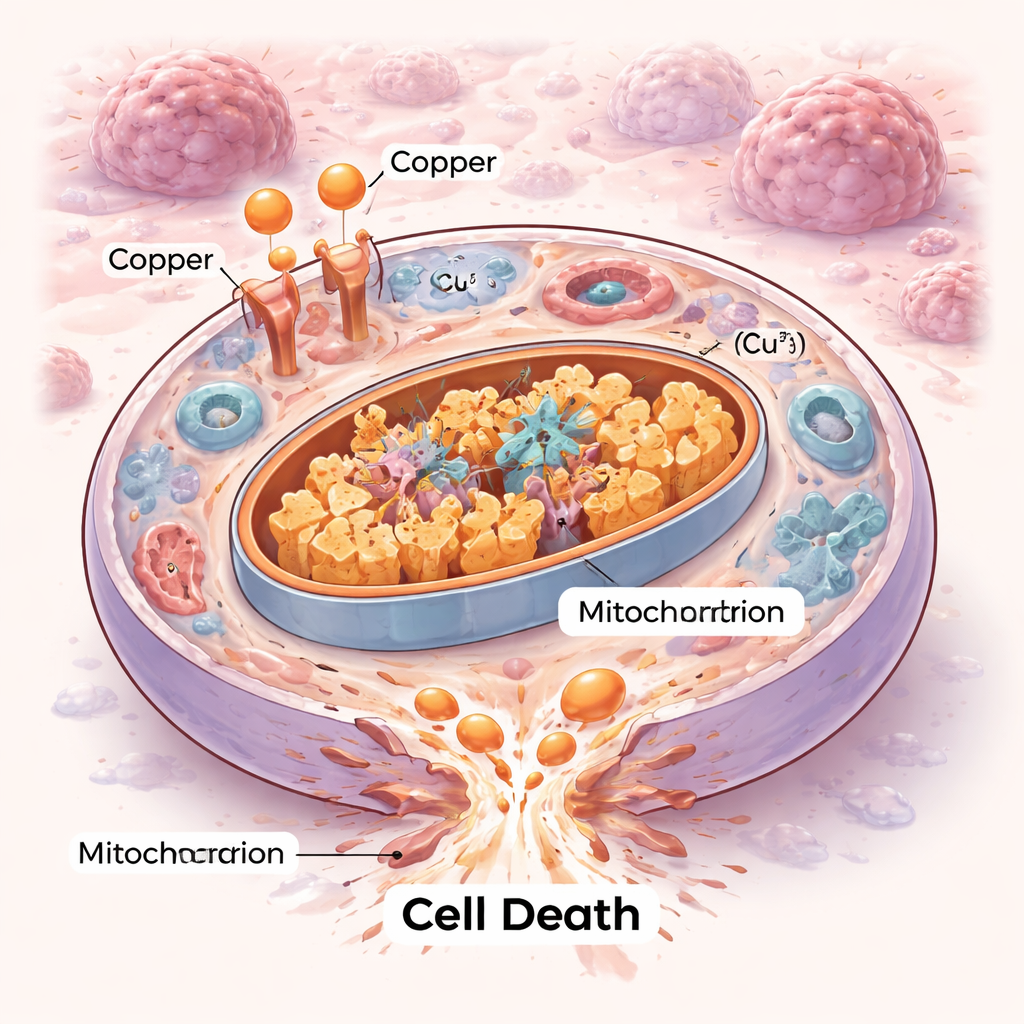
Een nieuwe manier waarop cellen kunnen sterven
Cellen sterven niet allemaal op dezelfde manier. Decennialang hebben wetenschappers geordende zelfvernietigingsprogramma’s in kaart gebracht zoals apoptose en nieuwere vormen zoals ferroptose. Cuproptose voegt een nieuw hoofdstuk toe. Hierbij overstroomt overtollig koper de energiecentrales van een cel — de mitochondriën — en bindt het aan specifieke metabole enzymen die normaal brandstof verbranden. Deze binding veroorzaakt dat die enzymen samenklonteren en destabiliseert kleine ijzer–zwavelcomponenten die mitochondriën nodig hebben om te functioneren. Het resultaat is een soort interne file en mechanische instorting die de cel niet kan herstellen, wat eindigt in celdood door proteotoxische stress in plaats van via de klassieke zelfmoordroutes.
Hoe kankercellen koper en energie regelen
Aangezien koper zowel essentieel als gevaarlijk is, onderhouden cellen een ingewikkeld logistiek netwerk om het veilig te verplaatsen. Specifieke transporters brengen koper de cel in, chaperonne-eiwitten begeleiden het naar mitochondriën en andere bestemmingen, en opslagmoleculen zoals metallothioneïnen en glutathion vangen overtollig koper op. Tumoren herbedraden dit systeem vaak. Sommige tumoren verhogen importeurs of chaperonnes om hun hoge energiebehoefte te voeden; andere vergroten exporteurs of opslagproteïnen om koper-overschot te vermijden. Tegelijk schakelen veel kankers hun metabolisme bij — ze wisselen tussen suikerverbranding aan het celoppervlak en diepere mitochondriale ademhaling. De review legt uit dat cuproptose het hardst toeslaat in cellen die nog sterk afhankelijk zijn van mitochondriën, waardoor tumoren met dit metabole profiel bijzonder kwetsbaar zijn.
Hoofdschakelaars die kopergevoeligheid afregelen
Belangrijke cellulaire “beslissers” beïnvloeden of cuproptose kan optreden. De tumorsuppressor p53 bijvoorbeeld duwt cellen doorgaans weg van snelle suikerfermentatie richting meer ordelijke mitochondriale brandstofverwerking. Daardoor, en door de aanpassing van de omgang met koperbindende enzymen, kan p53 kankers gevoeliger maken voor koper-geïnduceerde dood — terwijl gemuteerde vormen van p53 vaak het tegenovergestelde doen. Daarentegen helpt de hypoxiefactor HIF‑1α, geactiveerd in slecht geoxygeneerde tumorkernen, cellen ontsnappen aan cuproptose door sleutelmitochondriale enzymen te onderdrukken en koperbindende schilden te versterken. Andere routes, zoals Wnt/β‑catenine en AKT, bevorderen resistentie door koperexport aan te jagen of cruciale eiwitten chemisch te modificeren zodat ze niet meer op koperintoxicatie reageren. Samen werken deze netwerken als thermostaten en verhogen of verlagen ze de gevoeligheid van een tumor voor kopergebaseerde behandelingen.
Koper, het immuunsysteem en slimere geneesmiddellevering
De rol van koper beperkt zich niet tot het direct doden van kankercellen; het vormt ook het immuunlandschap rond tumoren. Gecontroleerde koperstress kan dode of stervende kankercellen zichtbaarder maken door gevarensignalen vrij te geven die T‑cellen, dendritische cellen en macrofagen aantrekken en activeren. Koper kan ook de niveaus van immuuncheckpoints zoals PD‑L1 beïnvloeden, die tumoren gebruiken om antitumor T‑cellen uit te schakelen, wat kansen suggereert om koper‑gerichte middelen te combineren met moderne immunotherapieën. Omdat vrij koper gezonde weefsels kan schaden, ontwikkelen onderzoekers precisiegereedschappen — kleine ionoforen die koper selectief in kankercellen begeleiden, en nanomedische platforms die koper of kopergestuurde geneesmiddelen verpakken in gerichte deeltjes of hydrogelconstructies. Deze technologieën zijn bedoeld om koper binnen tumoren tot dodelijke niveaus te verhogen terwijl de rest van het lichaam in een veilige marge blijft.
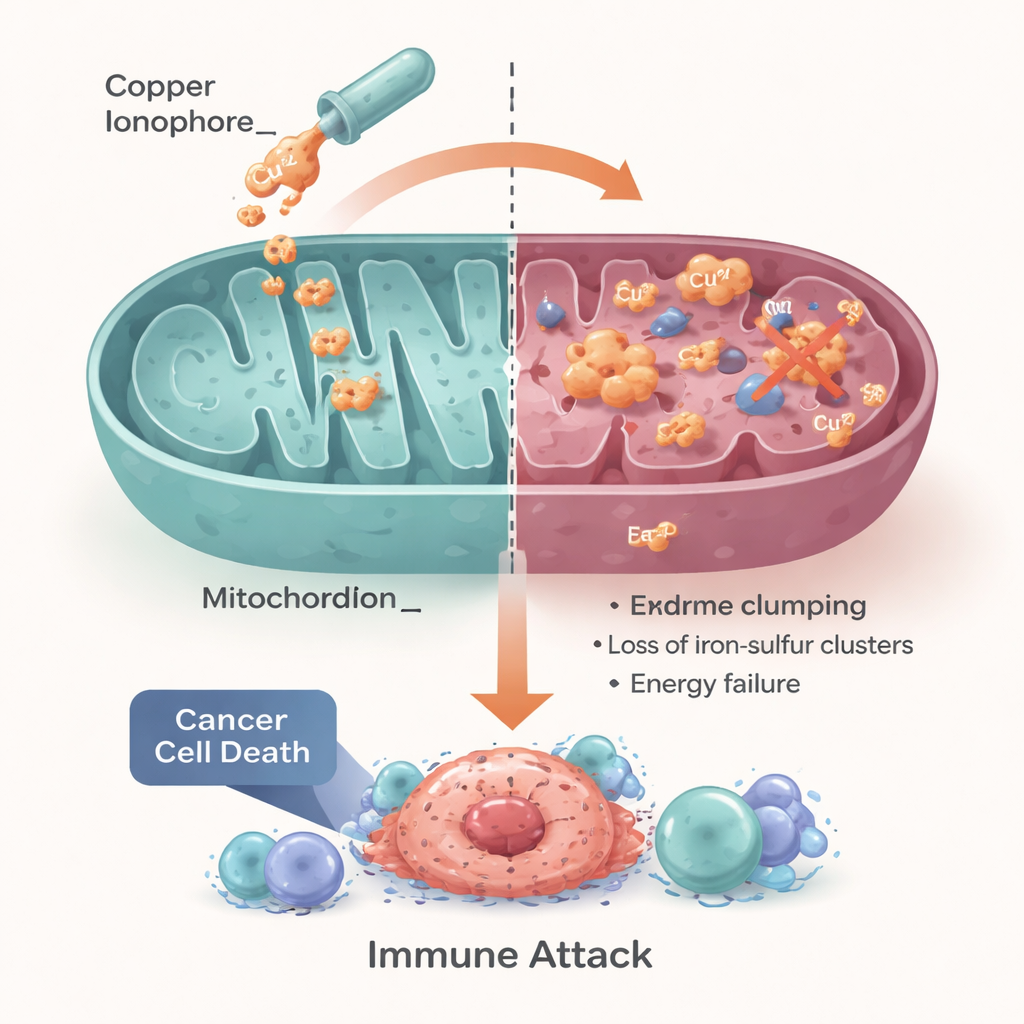
Een cellulaire zwakte omzetten in een behandeling
De auteurs concluderen dat cuproptose een basisbehoefte van de cel — zorgvuldige koper- en energieregulatie — verandert in een potentiële achilleshiel voor kanker. Kankers met verstoorde koperhandling of een overmatige afhankelijkheid van mitochondriaal metabolisme kunnen bijzonder gevoelig zijn voor kopergebaseerde strategieën, waaronder herbestemde middelen zoals disulfiram en elesclomol, evenals next‑generation nanodeeltjes. Ze benadrukken echter dat succes afhangt van het matchen van de juiste patiënten met de juiste benadering, met behulp van biomarkers die rapporteren over kopertransporteurs, mitochondriale activiteit en de immuun- en zuurstofstatus van de tumor. Als deze obstakels overwonnen kunnen worden, zou het benutten van cuproptose oncologen een nieuw, metaal-aangedreven hefboom kunnen bieden om tumoren te behandelen die momenteel weinig goede opties hebben.
Bronvermelding: Hao, Q., Gan, Y. & Zhou, X. Tackling cuproptosis: from metabolic rewiring to therapeutic exploitation in cancer. Cell Mol Immunol 23, 239–260 (2026). https://doi.org/10.1038/s41423-026-01387-x
Trefwoorden: cuproptose, koperstofwisseling, kankergeneeskunde, tumormetabolisme, kankerimmunotherapie