Clear Sky Science · nl
Dynamische magneto-mechanische kracht in lysosomen induceert duurzame herprogrammering van macrofagen voor antitumorele immuniteit
Met zachte krachten het immuunsysteem wekken
Kanker overleeft vaak door de afweer van het lichaam te laten slapen. Deze studie onderzoekt een onverwachte manier om die afweer opnieuw wakker te maken: door fysiek aan kleine compartimenten binnen immuuncellen te trekken met magnetisch aangedreven nanodeeltjes. In plaats van alleen op geneesmiddelen te vertrouwen, gebruiken de onderzoekers zorgvuldig afgestemde mechanische krachten binnen cellen om immuuncellen, genaamd macrofagen, om te programmeren tot langdurige tumorkillers.
Waarom solide tumoren moeilijk te behandelen zijn
Moderne kankerimmunotherapieën, zoals remmers van checkpoint-eiwitten en genetisch gemodificeerde immuuncellen, hebben voor sommige bloedkankers de behandeling veranderd. Voor veel patiënten met solide tumoren zoals longkanker helpen deze benaderingen echter slechts een minderheid. Een belangrijke reden is de tumormicroomgeving. Tumoren zijn omgeven door een beschermende niche vol cellen en signalen die de immuniteit dempen. Macrofaagjes, die tumors kunnen aanvallen (een M1-achtig stadium) of ondersteunen (een M2-achtig stadium), worden vaak in de tumorondersteunende M2-modus geduwd. Het op een duurzame manier omkeren van deze ‘slechte’ programmering is moeilijk geweest met conventionele biochemische geneesmiddelen alleen.
Nanodeeltjes als kleine mechanische motoren
Het team ontwierp magnetische nanomotoren—nanoschaal deeltjes van zinkgedopeerd ijzeroxide bekleed met een positief geladen polymeer—die gemakkelijk door macrofagen worden opgenomen en zich concentreren in lysosomen, de recycling- en signaalhubs van de cel. Eenmaal binnen laat een rotend extern magnetisch veld deze deeltjes zich uitlijnen tot staafachtige ketens en draaien, waardoor de stroperige vloeistof in lysosomen wordt geroerd en kleine wervels ontstaan. Computersimulaties en modelmembraanexperimenten toonden aan dat door de rotatiefrequentie zorgvuldig af te stemmen, de schuifspanning op het lysosomale membraan op een zoete plek kan worden ingesteld: sterk genoeg om het membraan kort lek te maken, maar niet zo sterk dat het permanent wordt vernietigd.
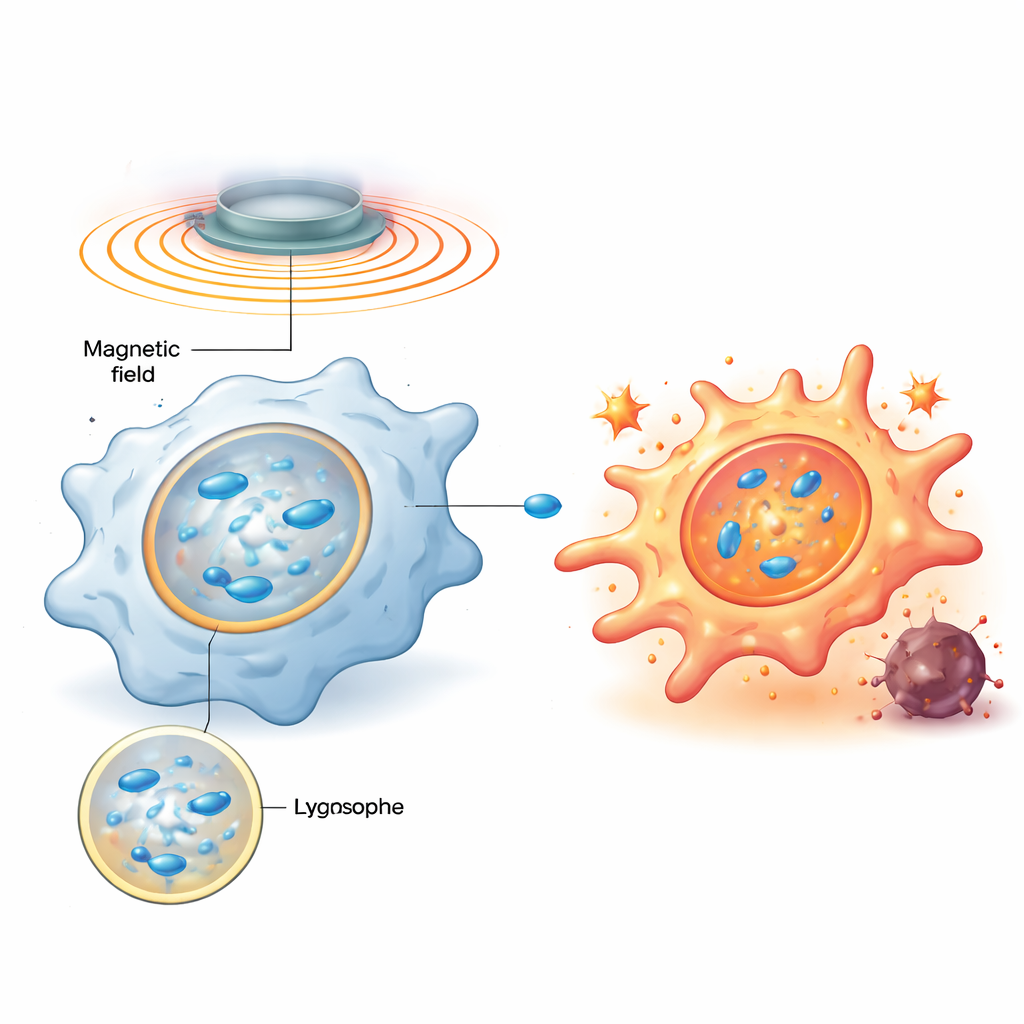
Mechanische duw zet een biochemisch alarm in werking
Wanneer het lysosomale membraan kort wordt verstoord, haast een suikerbindend eiwit genaamd galectine-9 zich naar de beschadigde plekken en fungeert als sensor voor deze mechanische stress. De studie laat zien dat dit op zijn beurt een sleutel-eiwit voor energiebewaking, AMPK, activeert, dat vervolgens het NF-κB-signaleringspad versterkt—bekend om ontstekings- en antimicrobiële reacties aan te sturen. Gezamenlijk herprogrammeren deze signalen het metabolisme van macrofagen weg van een rustige, brandstofefficiënte toestand naar snelle glycolyse, een patroon dat gekoppeld is aan vijandig, M1-achtig gedrag. Belangrijk is dat wanneer het magnetische veld wordt uitgeschakeld, het lysosoom zichzelf repareert en de signalering afneemt; wanneer het veld later weer wordt aangezet, wordt hetzelfde pad opnieuw geactiveerd. Dit programmeerbare aan-uit cyclen stelt onderzoekers in staat herhaaldelijk aan diezelfde mechanische schakelaar te ‘tikken’ zonder de cellen te doden.
Macrofaagjes heropvoeden om tumoren te bestrijden
In kweekexperimenten zette deze magnetisch geïnduceerde lysosomale permeabilisatie—MagLMP genoemd—macrofagen die naar een tumorondersteunende M2-achtige toestand waren geduwd, terug in een pro-inflammatoire M1-achtige toestand. Deze hergeprogrammeerde cellen produceerden meer ontstekingsbevorderende cytokinen en behielden hun M1-achtige profiel gedurende dagen, zelfs in tumormedia die hen normaal naar M2 zouden sturen. In muismodellen met tumoren vertraagde het inbedden van magnetische nanomotoren in tumoren en het toepassen van dagelijkse cycli van het roterende veld de groei van meerdere kankertypes. Toen macrofagen experimenteel werden uitgeput, verdween het voordeel grotendeels, wat laat zien dat deze cellen centraal staan voor het effect van de behandeling. Single-cell RNA-sequencing van tumorweefsel toonde verder aan dat MagLMP het aandeel M1-achtige macrofagen verhoogde, antitumorale neutrofielen en effector CD8-T-cellen versterkte, en NF-κB-gerelateerde en glycolysegenen binnen macrofagen omhoogreguleerde.
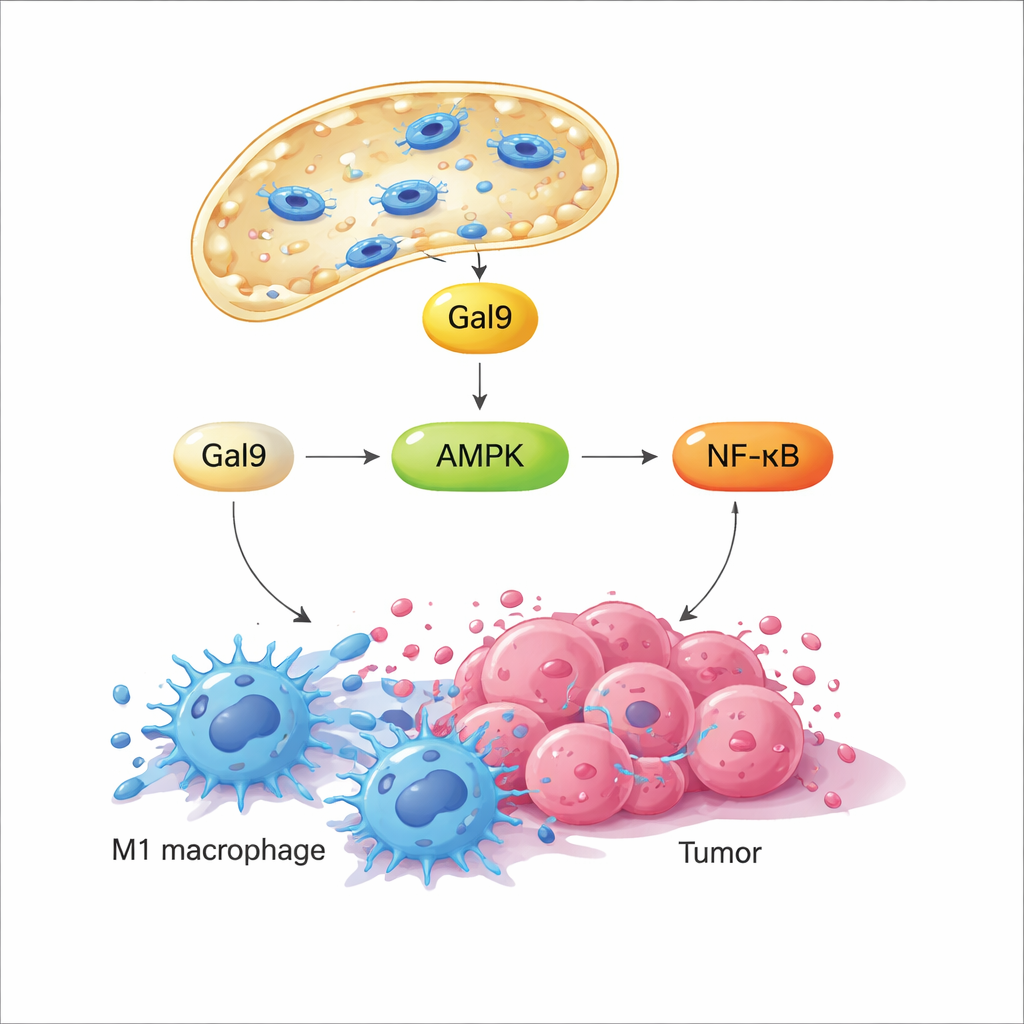
Van lokale controle naar systemische therapie
De onderzoekers vroegen zich vervolgens af of deze benadering meer als een realistische behandeling via de bloedbaan kon werken. Ze injecteerden de nanomotoren intraveneus en gebruikten een eenvoudige externe magneet om ze in tumoren te concentreren, waarmee ze efficiënte opname door macrofagen in het tumorbeds aantoonden. Een daaropvolgende MagLMP-behandeling verschuift opnieuw macrofagen richting de M1-achtige toestand en remde de tumorgroei. In een muismodel van vroegstadium longkanker die in de long zelf groeide, leidde het combineren van magnetische geleiding met cyclische MagLMP tot sterk verlengde overleving: ongeveer een derde van de behandelde muizen leefde meer dan 300 dagen, vergeleken met slechts weken in controlegroepen. Het combineren van MagLMP met een PD-1 checkpointremmer verbeterde de tumorcontrole in moeilijk behandelbare modellen verder.
Een nieuwe manier om immuniteit van binnenuit te sturen
Dit werk toont aan dat kleine, goed gecontroleerde mechanische krachten binnen een specifiek organel kunnen worden gebruikt om immuungedrag in levende dieren te sturen. Door lysosomen herhaaldelijk en omkeerbaar te ‘porren’, activeert MagLMP een galectine-9–AMPK–NF-κB-as die macrofagen herprogrammeer tot duurzame tumorkillers zonder cellen op grote schaal te beschadigen. Voor niet-specialisten is het belangrijkste idee dat fysieke signalen—afgegeven door magnetisch aangedreven nanomotoren—kunnen werken als een draaiknop voor het immuunsysteem, en zo een nieuwe klasse instrumenten bieden die geneesmiddelen in toekomstige kankerimmunotherapieën kunnen aanvullen.
Bronvermelding: Li, Y., Zheng, M., Zhu, Z. et al. Dynamic magneto-mechanical force in lysosomes induces durable macrophage repolarization for antitumor immunity. Cell Res 36, 197–218 (2026). https://doi.org/10.1038/s41422-025-01217-1
Trefwoorden: kankerimmunotherapie, herprogrammering van macrofagen, magnetische nanodeeltjes, mechanotransductie, lysosomaal signaleren