Clear Sky Science · nl
Bilirubine activeert rechtstreeks RIPK3 om niet‑klassieke necroptose te veroorzaken
Wanneer een nuttig molecuul schadelijk wordt
Bilirubine is vooral bekend als het gele pigment achter pasgeboren geelzucht en de vertrouwde kleur van bloeduitstortingen. In lage concentraties helpt het onze cellen juist beschermen tegen schade. Maar wanneer bilirubine in het lichaam ophoopt en in de hersenen doordringt, kan het blijvende schade veroorzaken, vooral bij pasgeborenen en mensen met ernstige leverziekte. Deze studie onthult een verrassende manier waarop overtollige bilirubine rechtstreeks een moleculaire "doodschakelaar" in hersencellen kan activeren, een destructieve vorm van celdood in gang zet en daarmee een nieuw doelwit voor toekomstige therapieën aanwijst.
Van bloedpigment tot bedreiging voor de hersenen
Bilirubine ontstaat wanneer ons lichaam rode bloedcellen recycleert. Normaal past de lever het aan en verwijdert het, waardoor de niveaus laag en relatief veilig blijven. In bepaalde omstandigheden — zoals neonatale geelzucht, ernstige infecties of leverfalen — kan onbehandelde bilirubine zich ophopen. Omdat het gemakkelijk oplost in vetten, kan deze "vrije" vorm de bloed‑hersenbarrière passeren, vooral wanneer die barrière verzwakt is door ziekte of ontsteking. Eenmaal in de hersenen is bilirubine bekend als toxisch, maar de precieze stappen waardoor het zenuwcellen beschadigt, waren tot nu toe onduidelijk.
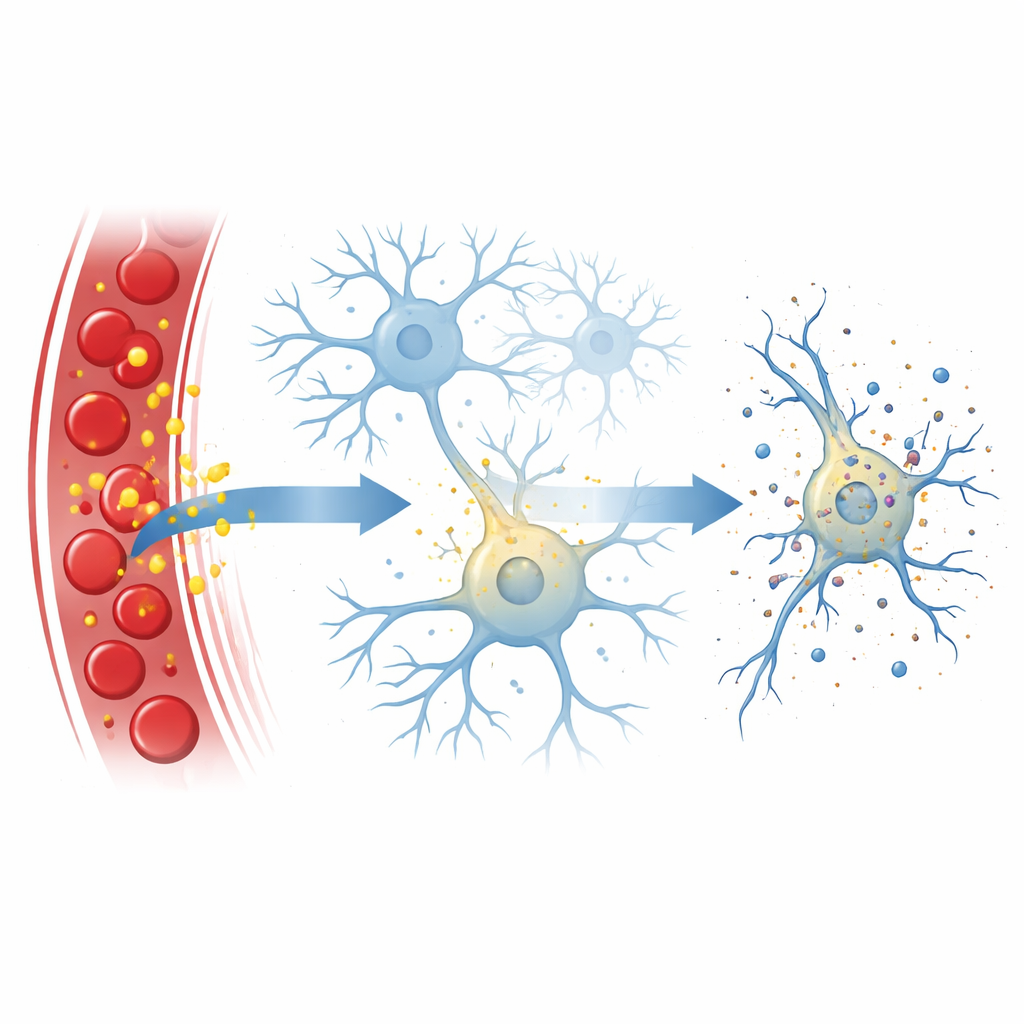
Een gecontroleerde celnexplosie
De onderzoekers richtten zich op necroptose, een gereguleerde vorm van celdood die lijkt op een kleine explosie: de cel zwelt op, het buitenmembraan scheurt en de inhoud stroomt eruit, wat vaak ontsteking veroorzaakt. Dit proces wordt normaal aangedreven door een keten van eiwitten, waarbij één eiwit, RIPK3, fungeert als een centraal knooppunt en een ander, MLKL, gaten in het celmembraan slaat. In de gebruikelijke leerboeken wordt RIPK3 geactiveerd door partner‑eiwitten die gevaar signalen herkennen, zoals ontstekingseiwitten of viraal genetisch materiaal. Hier vonden de onderzoekers dat bilirubine deze gebruikelijke partners kan omzeilen en toch necroptose in zenuwcellen kan induceren.
Bilirubine grijpt de doodsschakelaar van de cel
Met gekweekte neuronen, hersenplakjes en muismodellen lieten de wetenschappers zien dat bilirubine selectief RIPK3 en zijn downstream‑partner MLKL activeert in zenuwcellen, terwijl de gebruikelijke upstream‑eiwitten grotendeels ongewijzigd blijven. Genetische experimenten toonden aan dat wanneer RIPK3 of MLKL werden verwijderd, bilirubine neuronen niet langer efficiënt kon doden. Biochemische tests gingen verder: bilirubine bond fysiek aan RIPK3 op twee specifieke plekken binnen zijn actieve kern, veroorzaakte clustering van RIPK3‑moleculen en versterkte hun kinase‑activiteit — de chemische functie die het sterftepad inschakelt. Deze directe binding aan RIPK3 was niet afhankelijk van het gebruikelijke interactieoppervlak van het eiwit (de RHIM‑domein) of van andere adaptereiwitten, en markeert daarmee een niet‑klassieke route naar necroptose.
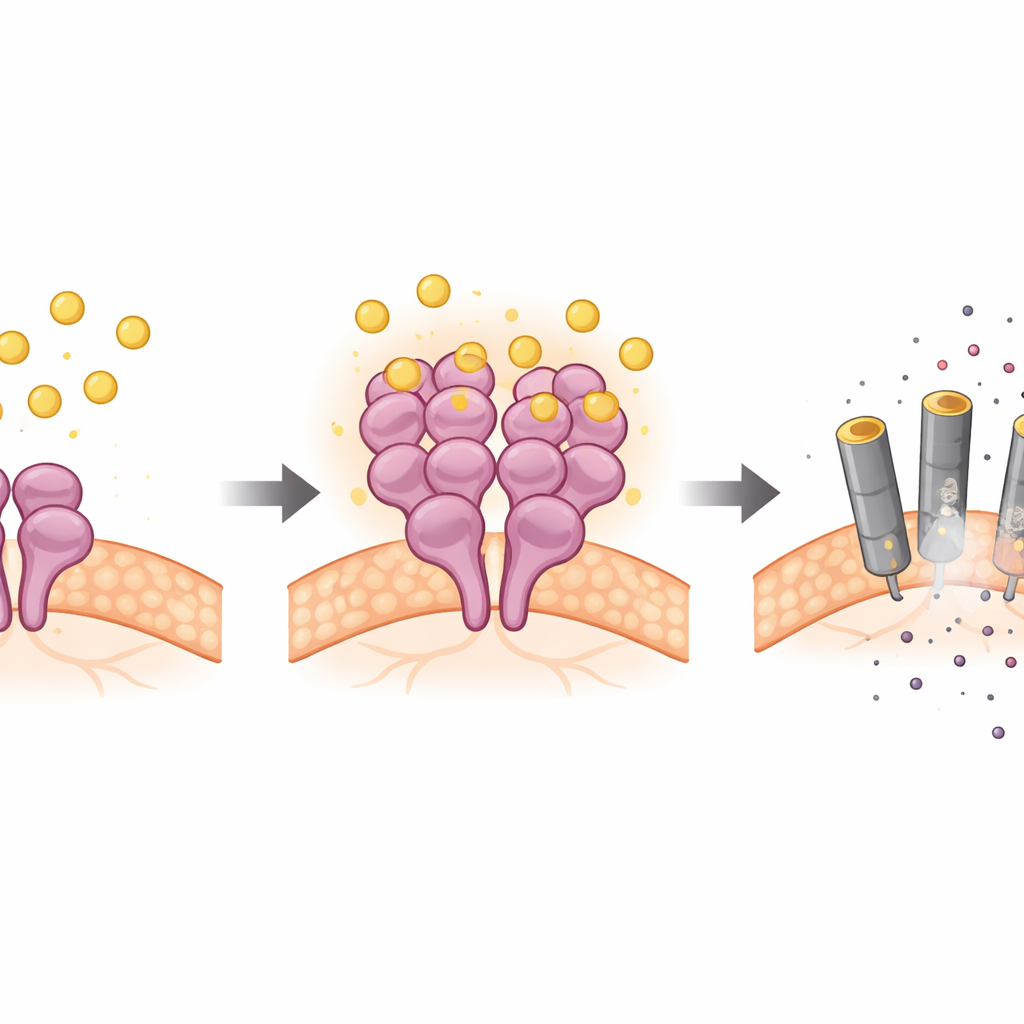
Bewijs uit het levende brein
Om te beoordelen of dit mechanisme ook in het hele dier van belang is, verhoogde het team het bilirubinegehalte bij muizen door het in de hersenen te injecteren of door leverletsel en ontsteking op te wekken zodat bilirubine op natuurlijke wijze de hersenen binnendrong. Bij normale muizen leidde dit tot sterke activatie van RIPK3 en MLKL in kwetsbare hersengebieden, meer markers van celdood en zichtbaar verlies van gezonde neuronen. Muizen zonder RIPK3 waren beschermd: hun neuronen toonden veel minder schade, minder doodsignalen en verminderde ontstekingsreacties, hoewel de bilirubinespiegels even hoog waren. Belangrijk was dat een verwerkte, wateroplosbare vorm van bilirubine die gewoonlijk als onschadelijk wordt gezien, noch RIPK3 activeerde noch soortgelijk hersenletsel veroorzaakte, wat benadrukt dat de ongewijzigde, vetoplosbare vorm de echte boosdoener is.
Wat dit betekent voor patiënten
Dit werk toont aan dat overtollige niet‑geconjugeerde bilirubine RIPK3 rechtstreeks kan inschakelen en zo een gecontroleerde maar destructieve ruptuur van hersencellen via necroptose kan veroorzaken. In plaats van alleen als een algemene toxine of bron van oxidatieve stress te werken, gedraagt bilirubine zich als een klein‑molecuulactivator van een specifiek sterfteprogramma in neuronen en immuuncellen van de hersenen. Voor patiënten met ernstige geelzucht of leverfalen suggereert dit dat het blokkeren van RIPK3 of MLKL — vooral met geneesmiddelen die de hersenen kunnen bereiken — mogelijk ooit kan helpen neurologische schade te beperken. Simpel gezegd toont de studie hoe een normaal nuttig pigment een precieze moleculaire moordenaar kan worden, en het wijst op nieuwe manieren om het te ontwapenen zonder zijn dagelijkse beschermende rollen te verstoren.
Bronvermelding: Xue, Q., Ma, X., Chen, Z. et al. Bilirubin directly activates RIPK3 to induce non-classical necroptosis. Cell Discov 12, 21 (2026). https://doi.org/10.1038/s41421-026-00876-7
Trefwoorden: bilirubine neurotoxiciteit, necroptose, RIPK3, leverfalen en hersenletsel, celsterftepaden