Clear Sky Science · nl
Loss-of-function varianten in ODAD1 verstoren ODA‑aankoppeling en induceren actine cytoskelet‑herorganisatie bij primaire ciliäre dyskinesie
Als de microscopische borstels van het lichaam falen
Elke ademhaling hangt af van legers van piepkleine, haarachtige structuren die trilharen worden genoemd en die slijm, ziekteverwekkers en stof uit de luchtwegen vegen. Bij mensen met een zeldzame erfelijke aandoening, primaire ciliäre dyskinesie (PCD), werken deze microscopische borstels niet correct, wat leidt tot aanhoudende hoest, longinfecties en soms een omgekeerde plaatsing van organen in het lichaam. Deze studie onthult hoe schadelijke veranderingen in één enkel gen, ODAD1, niet alleen de interne motoren van de trilharen uitschakelen, maar onverwacht ook het geraamte van de cellen die ze herbergen herbedraden—en daarmee een nieuw, mogelijk met geneesmiddelen aan te pakken zwak punt in de ziekte blootleggen.
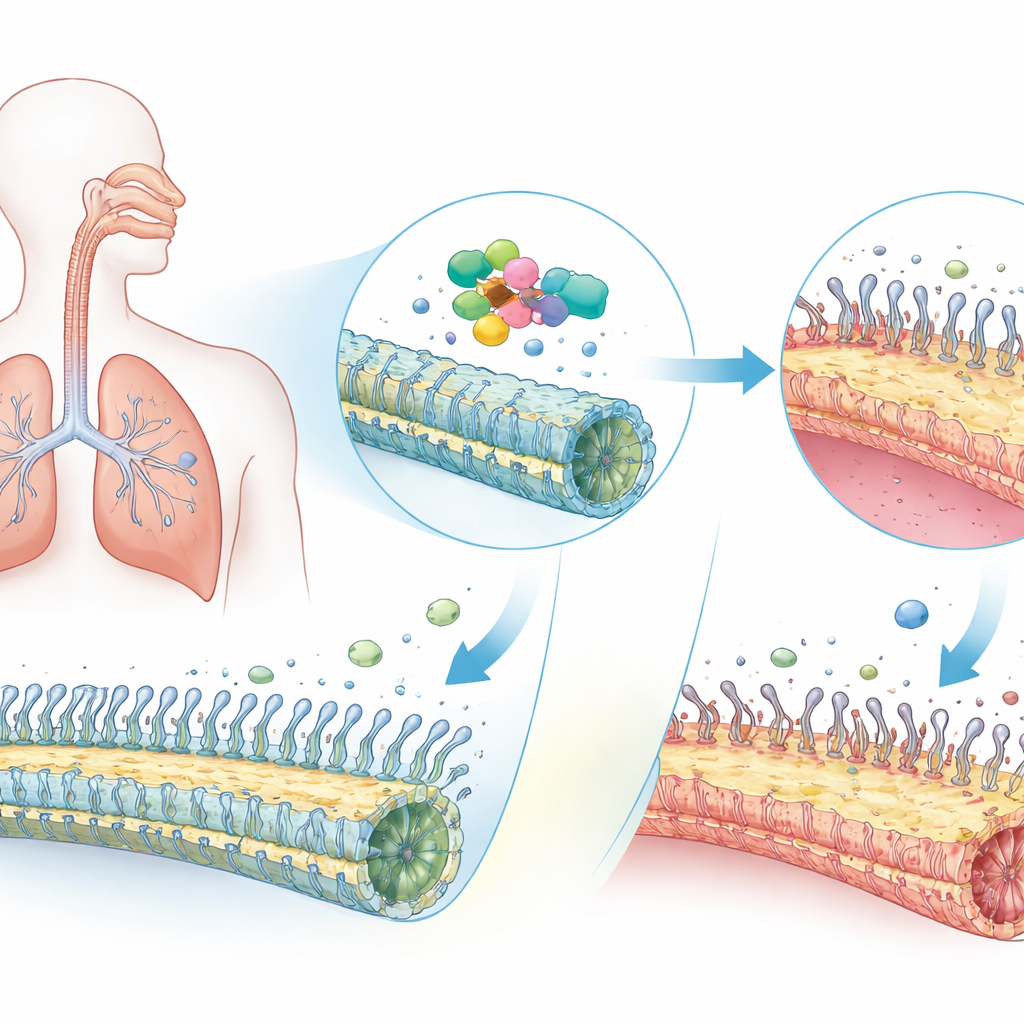
Een zeldzame longaandoening met grote gevolgen
PCD treft wereldwijd ongeveer één op enkele duizenden mensen en verschijnt vaak in de kinderjaren. Omdat de trilharen die de neus en longen bekleden niet effectief kunnen slaan, blijft slijm met ingesloten microben liggen, wat chronische bijholteproblemen, oorinfecties en progressieve longschade veroorzaakt. Veel patiënten hebben ook “situs inversus”, waarbij het hart en andere organen links‑rechts omgedraaid zijn — een teken dat trilharen in de embryo‑fase niet goed het vroege lichaamsplan hebben geleid. Artsen weten al geruime tijd dat defecten in tientallen verschillende genen PCD kunnen veroorzaken. ODAD1 is een van die genen en helpt de moleculaire motoren te verankeren die de zweepslagachtige beweging van elke trilharen aandrijven. Toch begrepen wetenschappers nog niet volledig hoe ODAD1‑defecten zich binnen menselijk luchtwegweefsel manifesteren.
Een defect gen volgen in cellen van patiënten
De onderzoekers bestudeerden negen individuen uit zeven Han‑Chinese families die klassieke tekenen van PCD vertoonden: ademhalingsproblemen als pasgeborene, levenslange natte hoest, frequente longinfecties en abnormaal lage niveaus van stikstofoxide in uitgeademde lucht, een klinische kenmerk van de ziekte. Genetisch onderzoek onthulde vier schadelijke varianten van het ODAD1‑gen, waaronder één die nog niet eerder was gezien. Al deze foutieve versies verminderden of elimineerden het normale ODAD1‑eiwit sterk in neusslijmvliescellen. Toen het team trilharen uit patiëntmonsters hoogsnelheidsfilmde, zagen ze dat de gebruikelijke vloeiende, golfachtige slag was vervangen door zwakke, ongecoördineerde flikkeringen. Laboratoriumkweken afkomstig van deze cellen, die een dun bekleedsel met trilharen van de luchtwegen op een lucht‑vloeistofinterface nabootsen, vertoonden dezelfde traagheid en gebrek aan coördinatie.
In de kapotte micromachines
Om te zien wat fysiek mis was, gebruikten de wetenschappers krachtige beeldvormingstechnieken. Standaard elektronenmicroscopie en geavanceerde cryo‑elektronenmicroscopie toonden aan dat de buitenste motorunits en hun aankoppellocaties volledig ontbraken in de trilharen van patiënten. In sommige gevallen waren ook andere sleutelstructuren in het ciliaire kerngebied verplaatst of misvormd. Deze defecten verklaren waarom de trilharen niet genoeg kracht kunnen genereren om slijm te verplaatsen. Toch reikte de schade verder dan de trilharen zelf. Het luchtwegoppervlak in patiënt‑afgeleide kweekmonsters herbergde veel minder multiciliated cellen, en de resterende cellen stonden vreemd uit elkaar en waren vergroot, met trilharen die in gemengde richtingen wezen. Verrassend genoeg was het aantal interne “basale lichamen” per cel — de zaden waaruit trilharen ontspruiten — normaal, wat suggereert dat het probleem lag in hoe deze cellen aan het weefseloppervlak georganiseerd waren in plaats van in hoeveel trilharen ze probeerden te bouwen.
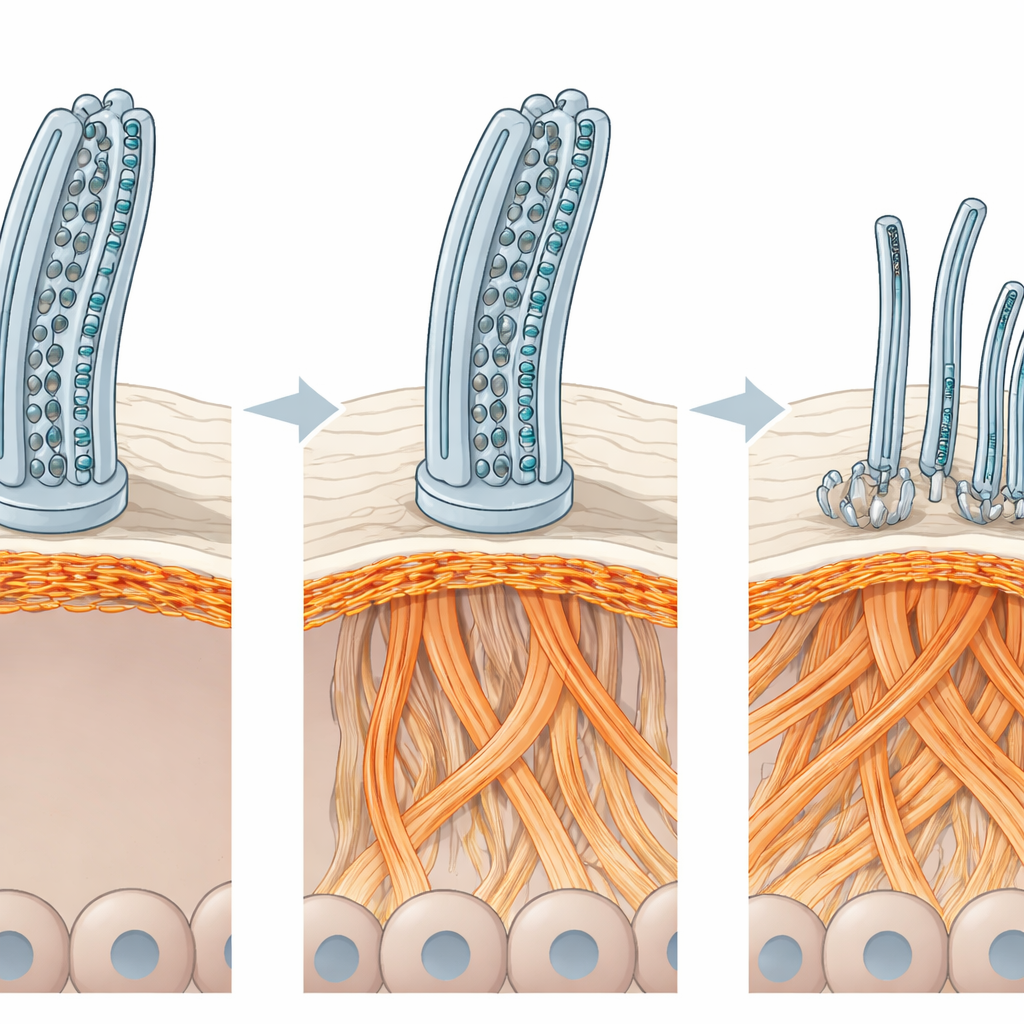
Het binnenste geraamte van de cel wordt herbedraad
Om vast te stellen wat deze organisatie verstoorde, maten de onderzoekers duizenden eiwitten in de patiënt‑afgeleide luchtwegkweken. Terwijl veel trilharen‑gerelateerde eiwitten verminderd waren, waren verschillende eiwitten die met actine geassocieerd zijn — de veelzijdige vezels die een groot deel van het interne celgeraamte vormen — juist in grotere hoeveelheid aanwezig. Beeldvorming van actinefilamenten bevestigde een dramatische herschikking van dit geraamte: verdikte actinebundels aan de bovenkant van multiciliated cellen, samengedrukte netwerken bij celgrenzen en geklomde ophopingen dieper in het weefsel. Deze veranderingen waren niet uniek voor de genetische achtergronden van de patiënten; het kunstmatig uitschakelen van ODAD1 in gezonde cellen produceerde dezelfde actine‑herorganisatie en het verlies van multiciliated cellen. Toen de onderzoekers de actine‑assemblage voorzichtig verstoorden met een klein molecuul middel, herstelde het aantal multiciliated cellen en hun oppervlakindeling gedeeltelijk, en werden trilharen talrijker en beter geordend — hoewel ze nog steeds niet normaal konden slaan zonder ODAD1’s rol in het motor‑aankoppelen.
Het ontbrekende onderdeel herstellen en vooruitkijken
Tenslotte onderzochten de wetenschappers of het vervangen van ODAD1 de trilharenbeweging kon herstellen. Ze kweekten “apicaal‑naar‑buiten” luchtweg‑organoïden — miniatuur, holle bolletjes van luchtwegweefsel met naar buiten gerichte trilharen — uit patiëntcellen en gebruikten een lentivirale vector om een werkende kopie van ODAD1 af te leveren. Het ingebracht eiwit nestelde zich correct in de trilharen, herstelde de ontbrekende motor‑aankoppellocaties en bracht de trilharenbeweging dicht bij normale snelheid en patroon terug. Gezamenlijk laten deze resultaten zien dat verlies van ODAD1 de luchtwegen op twee manieren schaadt: het schakelt direct het motorspringssysteem van de trilharen uit en verstoort indirect het actine‑geraamte dat het trilharenbekleedsel vormgeeft. Voor patiënten suggereert deze dubbele inzicht een tweesporen therapeutische toekomst — gentherapieën om het primaire motordefect te verhelpen en veiliger actine‑modulerende strategieën om te helpen een gezond tapijt van trilharen opnieuw opbouwen dat de longen weer helder kan houden.
Bronvermelding: Huo, C., Luo, T., Yang, S. et al. Loss-of-function variants in ODAD1 disrupt ODA docking and induce actin cytoskeletal remodeling in primary ciliary dyskinesia. Cell Discov 12, 25 (2026). https://doi.org/10.1038/s41421-026-00875-8
Trefwoorden: primaire ciliäre dyskinesie, ODAD1, motiele trilharen, actine cytoskelet, gentherapie