Clear Sky Science · nl
Integratieve ruimtelijke profileringsworkflow voor het bepalen van TME-architecturen in gearchiveerde klinische weefsels met CmTSA superplex-technologie
Waarom het verborgen landschap rond tumoren ertoe doet
Kankers groeien niet in isolatie. Ze worden omringd door een drukke buurt van immuuncellen, ondersteunende cellen, bloedvaten en littekenachtig weefsel die samen de “microomgeving” van de tumor vormen. Dit artikel introduceert een praktische manier om dat verborgen landschap in detail in kaart te brengen met standaard ziekenhuisweefselmonsters. Door te onthullen welke soorten cellen naast elkaar zitten en hoe ze zich organiseren in behulpzame of schadelijke buurten, kan de methode artsen helpen beter te voorspellen hoe de kanker van een patiënt zich gedraagt en welke behandelingen het meest waarschijnlijk werken.
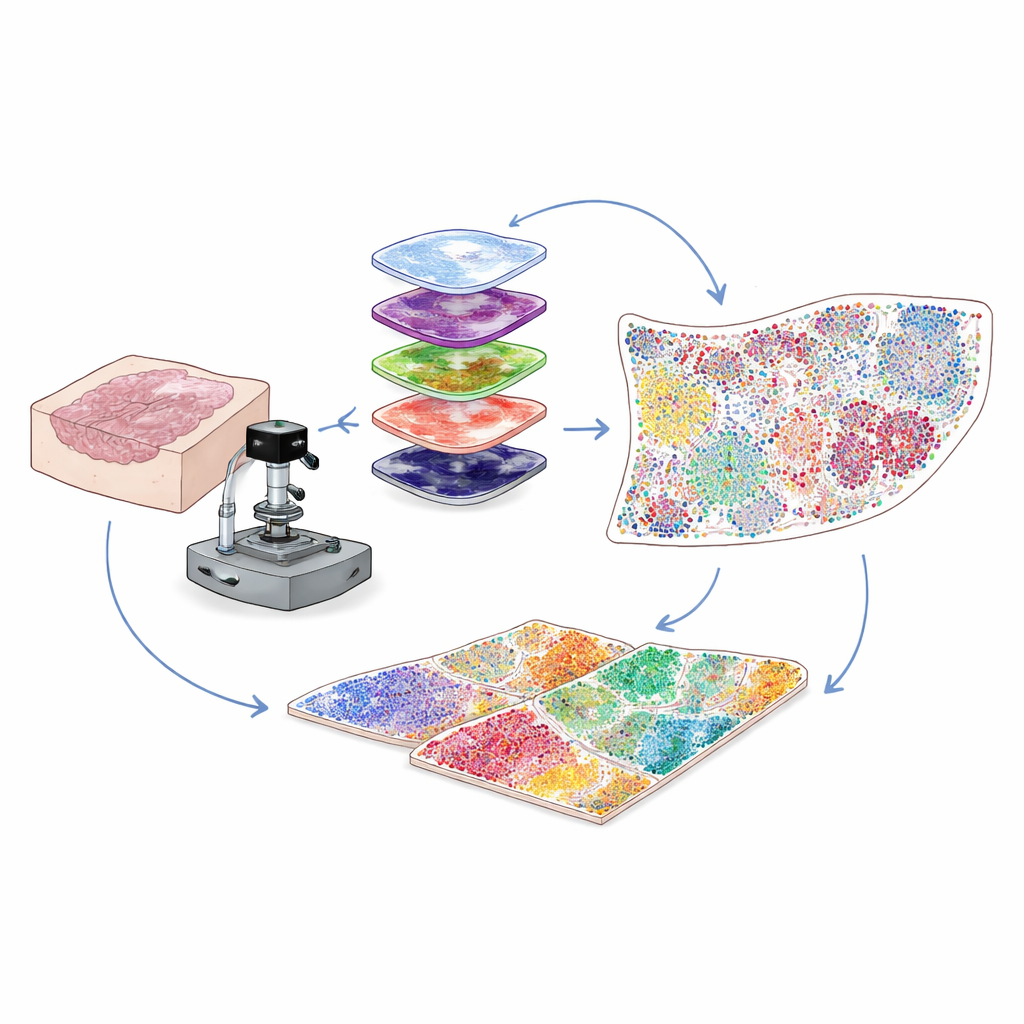
Meer zien in alledaagse ziekenhuismonsters
De meeste klinische kankermonsters worden bewaard als dunne plakjes paraffine-ingebed weefsel, bekend als FFPE-blokken, die jaren kunnen worden opgeslagen. Deze vormen een goudmijn voor onderzoek, maar een technisch probleem hield wetenschappers tegen: zulke monsters stralen natuurlijke achtergrondfluorescentie uit die de zwakke signalen van veel belangrijke eiwitten overstemt. De auteurs losten dit op door intens, zorgvuldig afgestemd licht te combineren met een milde chemische behandeling om die achtergrondgloed selectief uit te wissen zonder het weefsel of de eiwitdoelen te beschadigen. Deze hybride optische en chemische “bleaching”-stap verbetert de beeldhelderheid aanzienlijk, waardoor onderzoekers zwakke eiwitsignalen kunnen detecteren die anders verloren zouden gaan.
Dozijnsgewijs eiwitmarkers op dezelfde plak schilderen
Om te begrijpen welke cellen aanwezig zijn en wat ze doen, kleuren wetenschappers weefsels met antilichamen die zich aan specifieke eiwitten hechten. Traditionele multiplexmethoden hebben ofwel moeite met een zwak signaal voor zeldzame eiwitten of kunnen slechts een beperkt aantal markers tegelijk volgen. Hier gebruikt het team een aanpak genaamd cyclische tyramide signaalversterking. In elke ronde wordt een kleine set markers gekleurd en enzymatisch “ontwikkeld” tot heldere, permanent gebonden fluorescerende vlekken. De antilichamen worden vervolgens voorzichtig verwijderd terwijl het signaal blijft, de achtergrond wordt opnieuw gebleacht, en de volgende set markers wordt toegevoegd. Door deze cyclus vele malen te herhalen en de beelden uit te lijnen met behulp van het constante signaal van celkernen, kunnen ze betrouwbaar 30 tot 60 verschillende eiwitten op één weefselplak visualiseren, over een hele objectglaas, op single-cell resolutie.
Kleurige beelden omzetten in een cel-voor-cel atlas
High-plex beelden bevatten miljoenen pixels, veel meer dan een mens met het blote oog kan analyseren. De auteurs bouwen daarom een computerzichtworkflow die eerst elke celkern vindt en omlijnt met behulp van deep-learningtools die oorspronkelijk ontwikkeld zijn voor algemene celsegmentatie. Vervolgens wordt, op basis van waar de fluorescentie van elk eiwit verschijnt — op het membraan, in het cytoplasma of in de kern — en op een set logische regels, elke cel toegewezen aan een type of subtype, zoals tumorcel, helper-T-cel, killer-T-cel, B-cel, fibroblast of andere. De output is een digitale tabel die voor elke cel op het objectglaasje haar identiteit en exacte coördinaten vermeldt. Dit verandert een complex beeld in een kwantitatieve kaart van wie waar zit binnen de tumormicroomgeving.
Het onthullen van cellulaire buurten die de uitkomst bepalen
Cellen handelen zelden alleen; van belang is welke buren ze hebben. Om dit vast te leggen testen de onderzoekers verschillende manieren om lokale buurten rond elke cel te definiëren en kiezen uiteindelijk voor een radius-gebaseerde netwerkbenadering. Stel je voor dat je rond elke cel een kleine cirkel tekent — ongeveer zo dik als een mensenhaar — en opschrijft wie erin woont. Door cellen te groeperen waarvan de omliggende cirkels vergelijkbare mengsels van buren bevatten, identificeert de methode terugkerende “functionele niches”, zoals immuunrijke zones, door fibroblasten gedomineerde barrières of tumorgedomineerde regio’s. Toegepast op colonweefsel blijkt dat radius-gebaseerde buurten beter overeenkomen met bekende anatomische structuren dan alternatieve methoden. In cervixkankermonsters van patiënten met een goede versus slechte uitkomst, vindt het team dat immuuncelrijke niches zich bij patiënten met een gunstige prognose nabij de tumorrand clusteren, terwijl patiënten met slechtere uitkomst dikke, fibroblast-rijke zones tonen die tumorcellen omsluiten en aanvallende immuuncellen lijken af te sluiten.
Van ruimtelijke kaarten naar gerichte behandeling
Door hoogwaardige, betaalbare kleuring van vele eiwitten te combineren met robuuste beeldanalyse levert dit werk een end-to-end workflow die op grote aantallen standaard ziekenhuismonsters kan worden toegepast. De methode verandert bewaard weefsel in gedetailleerde kaarten van hoe tumor-, immuun- en stromale cellen zich ordenen en met elkaar interageren. Voor niet-specialisten is de kernboodschap dat niet alleen het type cellen, maar ook hun precieze buurtpatronen van invloed zijn op het gedrag van een kanker. Dit platform kan onderzoekers helpen beschermende immuun-hotspots te identificeren, onderdrukkende cellulaire barrières aan te wijzen en uiteindelijk nauwkeuriger prognoses en fijn afgestemde immunotherapiestrategieën te ondersteunen.
Bronvermelding: Xiao, C., Zhou, R., Chen, Q. et al. Integrative spatial profiling pipeline for determining TME architectures in archival clinical specimens using CmTSA superplex technology. Cell Discov 12, 16 (2026). https://doi.org/10.1038/s41421-026-00874-9
Trefwoorden: tumormicroomgeving, ruimtelijke proteomica, multiplexbeeldvorming, kankerimmunologie, single-cell-analyse