Clear Sky Science · nl
Chronobiologie van neurotrope virussen: ritmische virale ingang en aritmische gastheerklokken
Waarom timing belangrijk is bij herseninfecties
Veel gevaarlijke virussen, waaronder hondsdolheid en herpes, hebben de neiging het brein en de zenuwen binnen te dringen. Deze studie stelt een verrassend eenvoudige vraag met grote consequenties: verandert het tijdstip van de dag hoe gemakkelijk deze “neurotrope” virussen ons zenuwstelsel kunnen binnendringen, en kunnen de virussen op hun beurt onze interne klokken uit balans brengen? Inzicht in dit tweerichtingsgesprek tussen lichaamsklokken en virussen kan nieuwe mogelijkheden openen om vaccins, antivirale middelen en zelfs ploegendiensten te timen om risico’s te verkleinen.
Dagelijkse lichaamsklokken en virale deuropeningen
Bijna elke cel in het lichaam heeft een ingebouwd 24-uurs tijdsysteem, vaak de circadiaanse klok genoemd. Dat systeem wordt aangedreven door een stel kernklokeiwitten, waaronder BMAL1 en REV-ERBα, die duizenden genen ritmisch aan- en uitzetten. De auteurs richtten zich op de “deurknoppen” die virussen gebruiken om cellen binnen te komen – receptorproteïnen aan het celoppervlak – voor tientallen virussen die het brein als doelwit hebben of erin binnendringen. Door hersenachtige organoïden uit stamcellen, zenuwafgeleide cellijnen en muwweefsels te onderzoeken, vonden ze dat de meeste van deze virale receptoren gedurende de dag in hoeveelheid stijgen en dalen. Deze ritmes volgden nauwgezet de activiteit van klokcomponenten, wat suggereert dat ons dagelijkse tijdssysteem stilletjes bepaalt hoeveel virale toegangsplaatsen op een bepaald uur beschikbaar zijn.
Een celdelingsfactor wordt een klokboodschapper
Dieper gravend vroegen de onderzoekers hoe een eiwit dat gewoonlijk bekendstaat om het regelen van celdeling, E2F8 genoemd, past in dit tijdsnetwerk. Ze ontdekten dat E2F8 zelf onder circadiaanse controle staat en fungeert als relais tussen de klok en ten minste één belangrijk hondsdolheidsreceptor, p75NTR. Wanneer het klokeiwit REV-ERBα actief is, onderdrukt het E2F8. Daardoor verminderd E2F8 de rem op het p75NTR-gen niet meer, waardoor meer van deze receptor kan worden geproduceerd en cellen gastvrijer worden voor het hondsdolheidsvirus. Opmerkelijk is dat E2F8 ook terugkoppeling op de klok uitoefent: het kan rechtstreeks binden aan controlegebieden van kernklokgenen zoals REV-ERBα en PER2 en hun activiteit dempen. Dit creëert een feedbacklus waarin een celdelingsregelaar helpt de dagelijkse ritmes te vormen en daardoor de kwetsbaarheid van zenuwcellen voor infectie beïnvloedt.
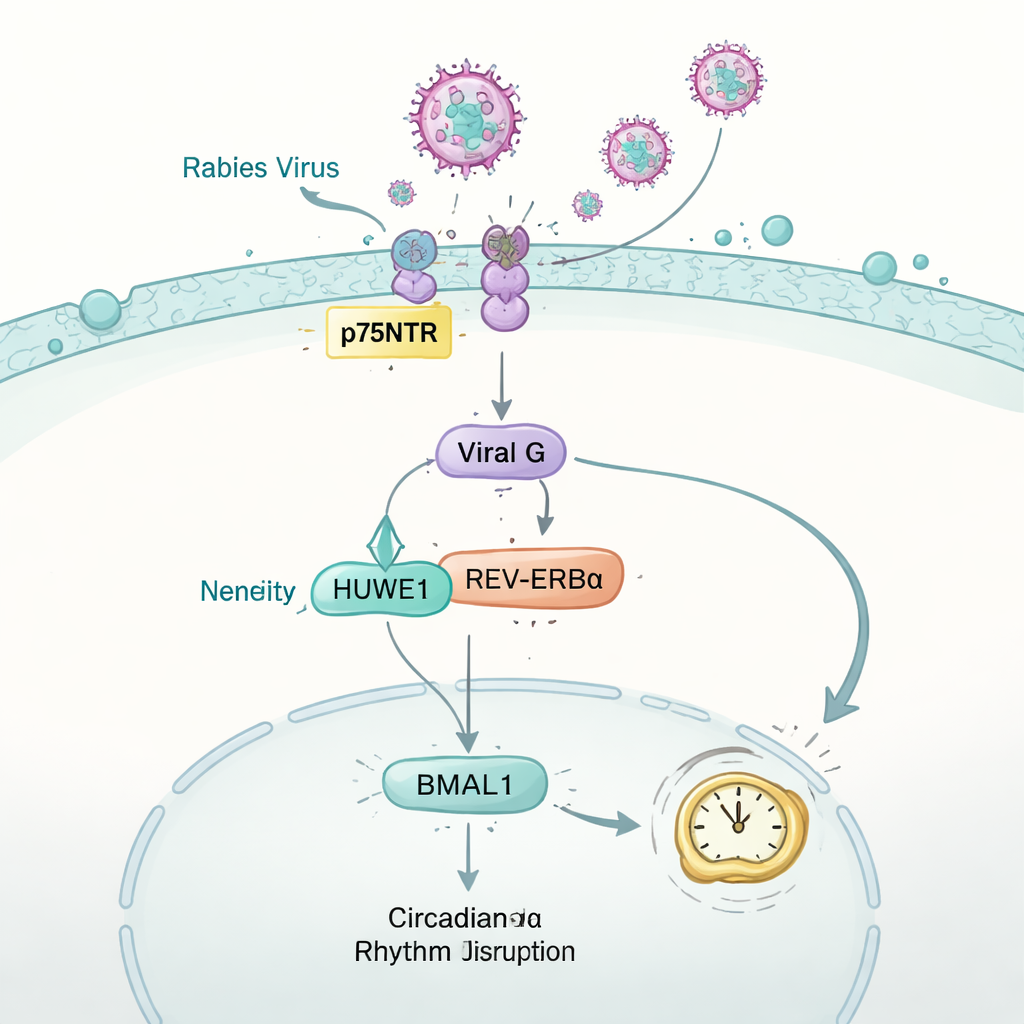
Hoe het hondsdolheidsvirus de klok uit het lood slaat
De studie draaide de vraag vervolgens om: kan een virus de klok terug geweld inzetten? Met muizen geïnfecteerd met het hondsdolheidsvirus hield het team loopactiviteit, stofwisseling en ademhalingschemie bij. Ondanks normale voedselinname vroeg in de infectie, verloren de dieren geleidelijk de normale dag-nachtpatronen die gezonde muizen laten zien. In de hersenen en verschillende andere organen daalden de niveaus van het cruciale klokeiwit BMAL1 scherp. In zenuwachtige cellen kon dit effect worden teruggevoerd op het hondsdolheidsglycoproteïne “G”, een oppervlakte-eiwit dat normaal het virus helpt fuseren met cellen. G kaapte een gastheerenzym genaamd HUWE1, dat gewoonlijk helpt een ander klokeiwit, REV-ERBα, te taggen voor afbraak. Door te concurreren om HUWE1 stabiliseerde het virale G-eiwit REV-ERBα, wat leidde tot extra onderdrukking van BMAL1 en uiteindelijk tot verstoring van het uurwerk dat de fysiologie op een 24-uursschema houdt.
Timing, jetlag en ernst van infectie
Om te testen of deze moleculaire veranderingen van belang zijn voor het hele organisme, infecteerde het team muizen met hondsdolheid op verschillende tijdstippen van de dag, onder normale licht-donkercycli, onder chronische “jetlag”-omstandigheden en in dieren die genetisch geen REV-ERBα hebben. Muizen die aan het begin van hun actieve (nacht)fase werden geïnfecteerd, wanneer de hondsdolheidsreceptor p75NTR een piek bereikt, verloren sneller gewicht, hadden hogere virale ladingen in meerdere hersengebieden, meer hersenontsteking en stierven eerder dan muizen die aan het begin van hun rustfase werden geïnfecteerd. Muizen die herhaalde faseverschuivingen ondergingen die roterend ploegendienst nabootsen, verloren normale klokritmes in de hersenen, toonden aanhoudend hogere p75NTR-niveaus, hadden zwakkere basis antivirale signalen en leden ernstiger ziekte. Daarentegen drukten muizen zonder REV-ERBα minder p75NTR uit, droegen lagere virale ladingen en overleefden langer na infectie, wat aangeeft dat deze klokcomponent een cruciale poortwachter is voor de ernst van hondsdolheid.
Wat dit voor mensen betekent
In gewone woorden toont de studie aan dat onze interne klokken niet alleen slaaptijden bepalen; ze openen en sluiten ook moleculaire deuropeningen die virussen die het brein binnendringen gebruiken, en diezelfde virussen kunnen terugslaan door de klok te verwarren. Eén factor, REV-ERBα, zit op een sleutelkruispunt: samen met E2F8 vormt het zowel receptorhoeveelheden als dagelijkse timing, terwijl het hondsdolheidsvirus het manipuleert in zijn eigen voordeel. Deze inzichten wijzen op praktische wegen vooruit. Vaccins of antivirale middelen kunnen op bepaalde tijden van de dag effectiever zijn, wanneer receptoren laag zijn of immuunresponsen sterk. Mensen met chronisch verstoorde ritmes — zoals ploegarbeiders of frequente reizigers — kunnen hogere risico’s lopen bij sommige neurotrope infecties. Het richten op REV-ERBα of aanverwante routes kan helpen het evenwicht in het voordeel van de gastheer te kantelen, waardoor infecties minder ernstig worden en uitkomsten verbeteren.
Bronvermelding: Zeng, S., Zhang, Q., Yang, X. et al. Chronobiology of neurotropic viruses: rhythmic viral entry and arrhythmic host clocks. Cell Discov 12, 11 (2026). https://doi.org/10.1038/s41421-026-00867-8
Trefwoorden: circadiaanse klok, neurotrope virussen, hondsdolheid, virale receptoren, chronotherapie