Clear Sky Science · nl
Dynamische veranderingen in het immuuromliggende milieu bij eierstokkanker na neoadjuvante chemotherapie
Waarom dit onderzoek belangrijk is voor vrouwen met eierstokkanker
Gevorderde eierstokkanker wordt vaak behandeld met krachtige chemotherapie voor of na een operatie, maar veel vrouwen krijgen toch terugval en verliezen gevoeligheid voor medicijnen. Deze studie behandelt een urgente vraag: hoe hervormt chemotherapie stilletjes de eigen afweer rond de tumor, en kunnen we die reactie bijsturen om de behandeling langer effectief te houden? Door individuele cellen in kaart te brengen en nieuwe medicijncombinaties in muismodellen te testen, onthullen de onderzoekers een verborgen rol voor vetachtige hormoonachtige moleculen—prostaglandinen—in het helpen van tumoren om na chemotherapie aan het immuunsysteem te ontsnappen.
Een veranderend slagveld rond de tumor
Eierstokkankers groeien niet geïsoleerd: ze bevinden zich in een drukke “buurt” van immuuncellen, bindweefsel en buikvocht. Voor de behandeling is deze omgeving vaak al in het voordeel van de kanker, met weinig agressieve killer‑T‑cellen en veel cellen die immuunaanvallen dempen. Het team analyseerde eerder gepubliceerde single‑cell RNA‑sequencingdata van vrouwen met hooggradig serieuze eierstokkanker en vergeleek monsters vóór en na neoadjuvante chemotherapie (chemotherapie gegeven vóór de operatie). Ze vonden dat chemotherapie niet alleen tumorcellen doodde; het wakkerde ook tijdelijk immuunactiviteit aan, met verhoogde signalen voor T‑celstimulatie en ontsteking en een afname van sommige regulerende T‑cellen die normaal remmen.
Wanneer nuttige veranderingen schadelijk worden
Ondanks deze korte opleving krijgen de meeste patiënten toch relapse en worden ze resistent tegen platinummedicijnen zoals cisplatine. Om te begrijpen waarom, onderzochten de onderzoekers dieper hoe verschillende celtypen na behandeling met elkaar communiceren. Ze ontdekten dat chemotherapie genen die betrokken zijn bij de productie van prostaglandinen sterk verhoogde in tumor‑geassocieerde macrofagen en fibroblasten, en de communicatie tussen deze cellen en T‑cellen versterkte. Met geavanceerde wiskundige analyse lieten ze zien dat de algemene omgeving verschoof naar een pro‑inflammatoir maar uiteindelijk onderdrukkend stadium, met toenemende chemokinen die myeloïde cellen aantrekken en versterkte routes die T‑cellen na verloop van tijd kunnen uitputten. Dit suggereert dat prostaglandinen kunnen fungeren als een moleculaire schakelaar die een aanvankelijk nuttige immuurgolf omzet in een langdurige rem op antitumorimmuniteit.
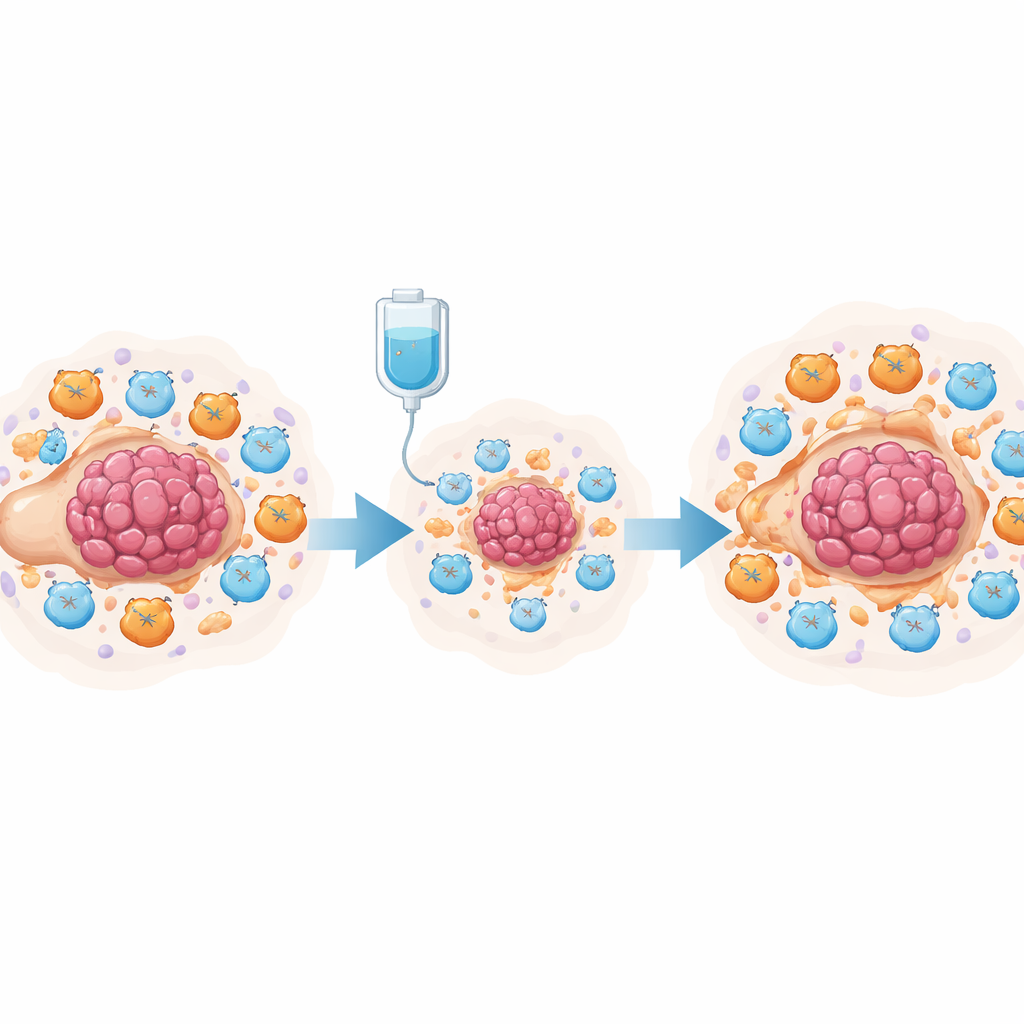
Chemotherapie, prostaglandinen en gesupprimeerde T‑cellen
Om dit experimenteel te toetsen, gebruikte het team een muismodel van eierstokkanker behandeld met cisplatine. Single‑cell analyse van tienduizenden cellen uit de buikholte toonde dat cisplatine het aantal tumorcellen verminderde en het totale aantal T‑cellen verhoogde, maar ook duidelijk myeloïde‑afgeleide suppressorcellen (MDSC’s) en uitgeputte killer‑T‑cellen uitbreidde. Zowel tumorcellen als deze suppressorcellen produceerden hoge niveaus van enzymen die prostaglandinen maken. In kweekexperimenten dreven cisplatine‑behandelde tumorcellen beenmergcellen naar een MDSC‑achtig toestand en verzwakten ze de activiteit en proliferatie van CD8+ killer‑T‑cellen. De onderzoekers traceerden dit effect naar het NF‑κB‑signaleringspad in tumorcellen, dat het PTGES‑gen inschakelde—een cruciale stap bij de productie van prostaglandine E2. Het blokkeren van dit pad verminderde PTGES‑niveaus en prostaglandineproductie.
De omslag maken met combinatietherapie
De meest praktische vraag was of het blokkeren van prostaglandinen chemotherapie effectiever kan maken. Bij muizen gebruikten de wetenschappers genetische verwijdering van Ptges in tumorcellen, antilichamen die prostaglandine E2 neutraliseren, of kleine moleculaire remmers van prostaglandine E‑synthase. Al deze benaderingen verlaagden prostaglandinespiegels, verminderden de ophoping van MDSC’s en herstelden het doden en de stam‑achtige veerkracht van CD8+ T‑cellen. Gecombineerd met cisplatine, of met het standaard cisplatine‑paclitaxelregime, vertraagden prostaglandineremmers de tumorgroei en -verspreiding effectiever dan chemotherapie alleen. De gegevens wijzen erop dat door prostaglandinen gedreven immuunsuppressie geen bijzaak is, maar een centrale reden waarom tumoren na een initiële respons ontsnappen.
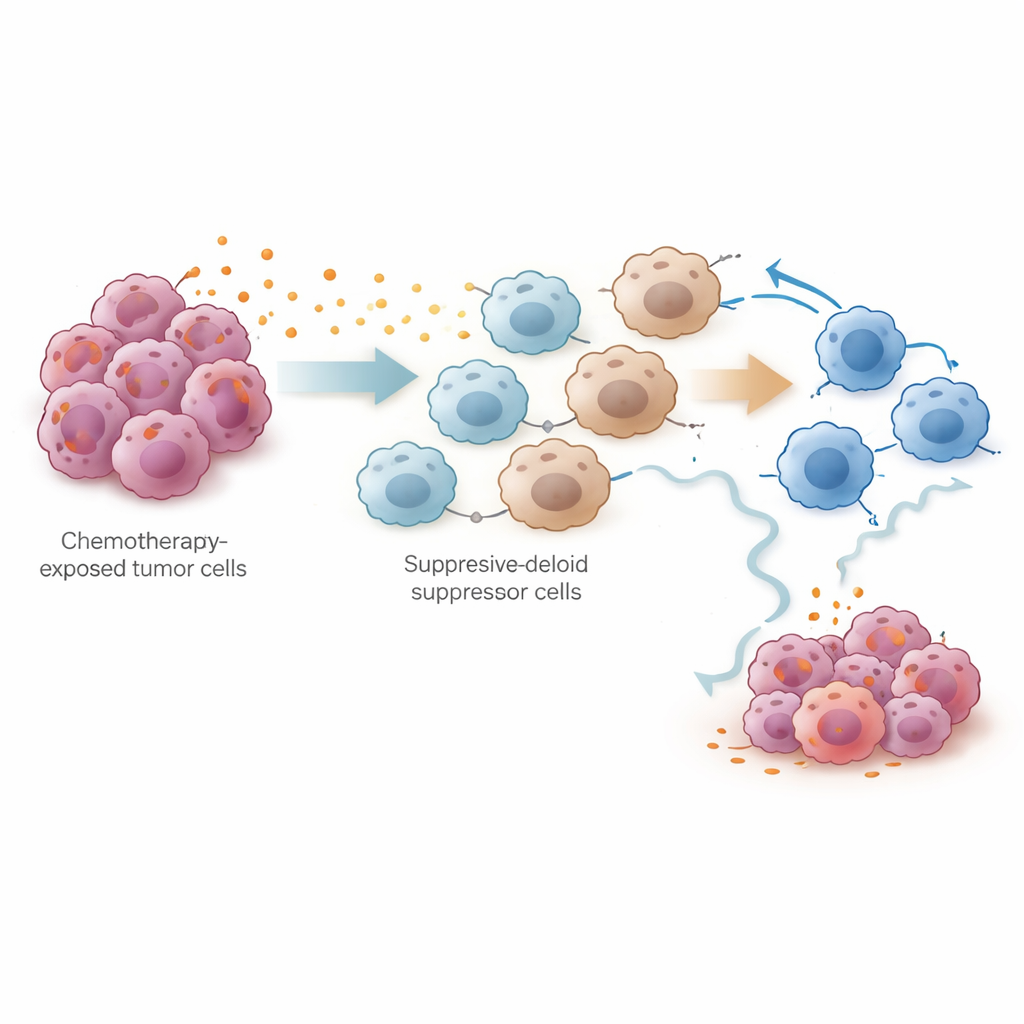
Een nieuw perspectief om behandeling effectief te houden
In gewone bewoordingen suggereert dit werk dat chemotherapie de omgeving van de tumor in twee fasen verandert: eerst verzwakt het de kanker en mobiliseert het kort het immuunsysteem, maar daarna veroorzaakt het een golf van prostaglandinen die suppressorcellen aantrekt en de natuurlijke tumor‑doderkrachten van het lichaam vermoeit. Door PTGES‑gedreven prostaglandineproductie als hoofdschuldige te identificeren, wijst de studie op een concrete strategie: het combineren van standaard platinachemotherapie met middelen die prostaglandinepaden blokkeren kan helpen een sterke immuunaanval te behouden en terugval bij eierstokkanker uit te stellen of te voorkomen. Hoewel klinische onderzoeken nog nodig zijn, biedt deze gecombineerde aanpak een veelbelovende nieuwe richting om het voordeel van bestaande behandelingen te verlengen.
Bronvermelding: Wu, M., Lv, F., Jin, Y. et al. Dynamic changes of the immune microenvironment in ovarian cancer following neoadjuvant chemotherapy. Cell Death Discov. 12, 130 (2026). https://doi.org/10.1038/s41420-026-03070-6
Trefwoorden: eierstokkanker, tumormicro‑omgeving, chemotherapie‑resistentie, prostaglandinen, immunotherapie