Clear Sky Science · nl
Epigenetische context bepaalt de transcriptieactiviteit van canonische en niet-canonische NF-κB-signaalroutes bij pancreaskanker
Waarom deze studie belangrijk is voor patiënten
Pancreaskanker behoort tot de dodelijkste vormen van kanker, deels omdat kankercellen bedreven zijn in het waarnemen en reageren op alarmsignalen in hun omgeving. Deze studie onderzoekt twee van die signalen, TNFα en TWEAK, en laat zien hoe ze verschillende „leesmodi” in het DNA van kankercellen activeren. Inzicht in deze modi kan nieuwe wegen openen om tumorgroei te vertragen, uitzaaiing te beperken en behandelingen effectiever te maken.
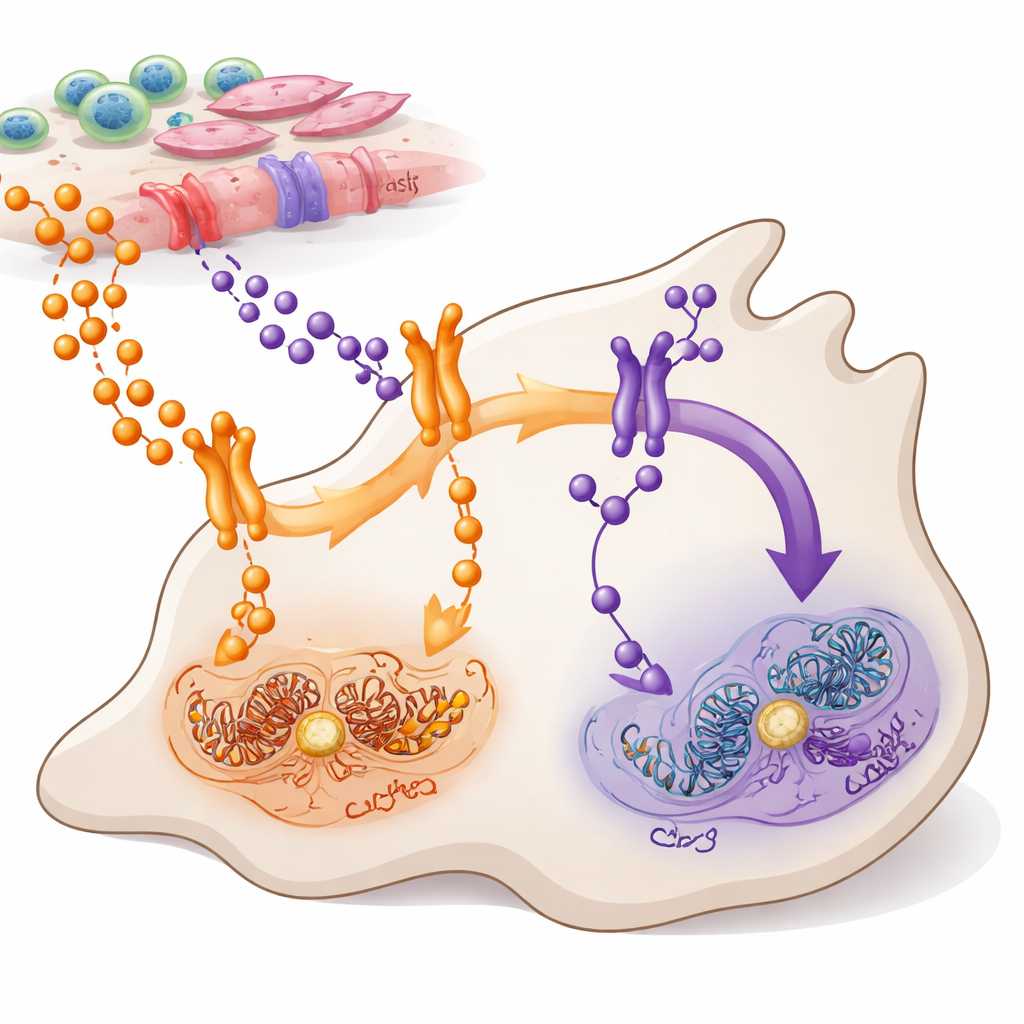
Twee berichtenroutes naar kankercellen
TNFα en TWEAK zijn kleine eiwitachtige boodschappers die door cellen in en rond een tumor worden afgegeven. Beide communiceren met een belangrijk regelsysteem binnen cellen, bekend als NF-κB, dat meehelpt bepalen of cellen groeien, bewegen of afsterven. De auteurs richtten zich op pancreatische ductale adenokarcinomen, de meest voorkomende en agressieve vorm van pancreaskanker, waarin NF-κB in de meeste tumoren abnormaal actief is. Ze brachten in kaart welke cellen TNFα en TWEAK produceren, welke cellen hun receptoren dragen, en hoe deze signalen door twee verwante NF-κB-takken stromen—vaak aangeduid als de canonische (via RELA) en niet-canonische (via RELB) routes.
Wie zendt de signalen in de tumoromgeving
Door single-cell RNA-sequencing van duizenden cellen uit patiëntentumoren te combineren met geavanceerde microscopie, vonden de onderzoekers dat TNFα vooral afkomstig is van immuuncellen, met name macrofagen en bepaalde T- en B-cellen. TWEAK daarentegen wordt geproduceerd door een breder scala aan cellen: macrofagen, fibroblasten, endotheelcellen en stellaatcellen. Ook hun receptoren verschillen. Tumorcellen en nabije fibroblasten drukken sterk de belangrijkste TNFα-receptor en de sleutelreceptor voor TWEAK uit. Netwerkanalyse suggereerde dat TWEAK-gebaseerde signalering een ruimer en complexer communicatienetwerk vormt tussen tumor- en ondersteunende cellen, terwijl TNFα-signaaloverdracht meer gefocust is binnen immuunrijke gebieden.
Verschillende diepten van respons binnen tumorcellen
In pancreaskankercellijnen behandelden de onderzoekers cellen met TNFα of TWEAK en maten welke genen in de tijd werden geactiveerd. TNFα veroorzaakte een snelle en brede golf van genactiviteit die verband houdt met ontsteking, celbeweging, weefselremodellering en overleving. TWEAK induceerde een kleinere, langzamere reeks veranderingen die grotendeels overlappen met de doelwitten van TNFα in plaats van een uniek programma te starten. Beide signalen konden celmigratie bevorderen en onder bepaalde omstandigheden celdood induceren, maar TNFα had het sterkere effect op beweging. Bij onderzoek van patiëntrdata uit The Cancer Genome Atlas zagen de onderzoekers dat tumoren met hoge TNFα- of hoge TWEAK-niveaus veel gedeelde geactiveerde genen vertoonden, wat deze patronen bevestigt in echte menselijke kankers.
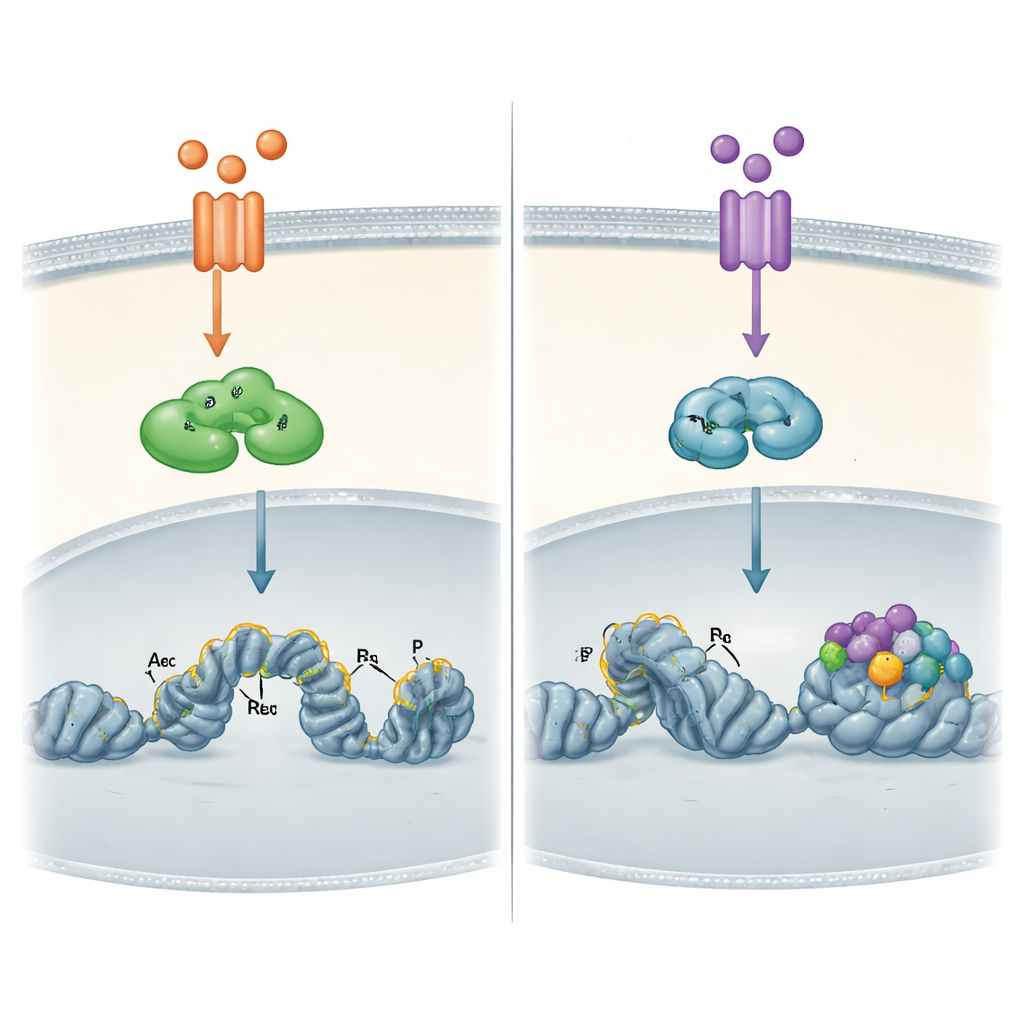
Hoe het DNA-landschap elke route vormt
De meest opvallende verschillen kwamen naar voren toen de auteurs direct naar het chromatine van de kankercellen keken—de compacte vorm van DNA en de eraan gebonden eiwitten. Met genoomwijde bindingkaarten toonden ze aan dat door TNFα geactiveerde RELA niet alleen aan reeds open DNA-regio’s kan binden, maar ook aan dichter verpakte regio’s en deze vervolgens kan helpen „openen” door chemische markeringen toe te voegen die geassocieerd zijn met actieve schakelaars. RELB, later geactiveerd door TWEAK, bond vrijwel uitsluitend aan locaties die al toegankelijk waren en voorzien van zulke actieve markeringen. Deze RELB-locaties waren bijzonder rijk aan dockingmotieven voor een andere factorfamilie, AP-1, wat suggereert dat RELB afhankelijk is van andere eiwitten die het terrein voorbereiden voordat het kan werken.
Wat dit betekent voor toekomstige behandelingen
Voor niet-specialisten is de belangrijkste conclusie dat TNFα en TWEAK hetzelfde NF-κB-gereedschap op wezenlijk verschillende manieren gebruiken. TNFα, via RELA, gedraagt zich als een hoofdschakelaar die gesloten delen van het DNA van kankercellen kan openwrikken en een breed scala aan genen kan activeren die betrokken zijn bij groei, overleving en verspreiding. TWEAK, via RELB, is meer een specialist die alleen kan opereren waar het DNA al open is en waar cofactoren zoals AP-1 aanwezig zijn. Deze taakverdeling suggereert dat geneesmiddelen die chromatinhermodellering, AP-1 of specifieke NF-κB-takken targeten, schadelijke genprogramma’s in pancreaskanker selectief zouden kunnen verzwakken terwijl andere functies meer intact blijven.
Bronvermelding: Aggrey-Fynn, J.E., Busch, J., Saul, D. et al. Epigenetic context defines the transcriptional activity of canonical and noncanonical NF-κB signaling in pancreatic cancer. Cell Death Discov. 12, 152 (2026). https://doi.org/10.1038/s41420-026-03019-9
Trefwoorden: pancreaskanker, NF-kappaB-signalisatie, tumormicro-omgeving, epigenetische regulatie, TNF en TWEAK