Clear Sky Science · nl
Pyroptose benutten in de behandeling van borstkanker: immunologische mechanismen en opkomende biomaterialenstrategieën
Celsterfte als nieuw wapen tegen borstkanker
Borstkanker blijft een van de meest voorkomende en hardnekkige vormen van kanker wereldwijd. Veel tumoren ontwijken na verloop van tijd chirurgie, chemotherapie en zelfs moderne immuuntherapieën. Deze review onderzoekt een opkomend idee: het opzettelijk opwekken van een ‘vurige’ vorm van celdood, pyroptose, binnen borstumoren. Door kankercellen gecontroleerd en ontstekingsbevorderend te laten openbarsten, hopen wetenschappers de tumor zowel direct te doden als het immuunsysteem te activeren om mee te vechten.
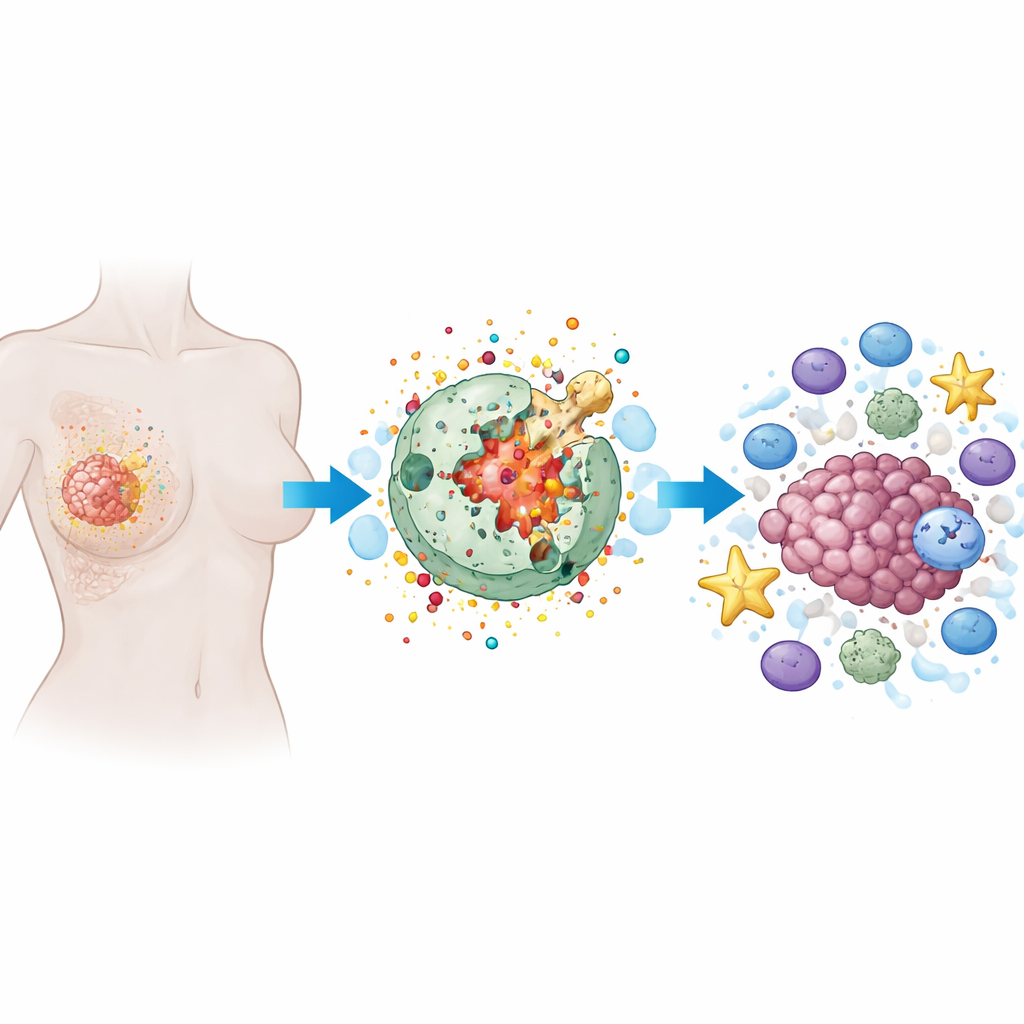
Hoe een vurige vorm van celdood werkt
Pyroptose is een geprogrammeerde vorm van celdood waarbij een cel opzwelt, het buitenmembraan vol gaten komt te zitten en uiteindelijk scheurt, waarbij de inhoud vrijkomt. In tegenstelling tot de stille, nette celdood die bij veel therapieën wordt gezien, is pyroptose luidruchtig en ontstekingsbevorderend. Gespecialiseerde eiwitten, vooral een familie genaamd gasderminen, werken als kleine springladingen. Zodra ze worden doorgesneden door intracellulaire enzymen, slaan gasderminen gaten in het celmembraan. Dit vernietigt niet alleen de kankercel maar geeft ook alarmstoffen en ontstekingsmoleculen vrij die immuuncellen kunnen aantrekken en activeren.
Waarom borsttumoren een bijzondere uitdaging zijn
Borstkanker is geen eenduidige ziekte maar een verzameling subtypes met verschillend gedrag. Sommige, zoals triple-negatieve borstkanker, missen gangbare medicatiedoelen en zijn vaak resistent tegen behandeling. Veel borstumoren worden beschouwd als ‘immunologisch koud’, wat betekent dat ze weinig actieve immuuncellen bevatten. De review legt uit hoe kenmerken van de tumoromgeving in de borst — waaronder stromale cellen, immuunsuppressieve cellen en lokale zuurstoftekorten — zowel het podium voor pyroptose kunnen vormen als, bij slechte beheersing, de ontsteking kunnen omzetten in brandstof voor tumorgroei en verspreiding. Deze dubbelzinnige aard maakt precisie bijzonder belangrijk.
De gasdermine-schakelaars binnen tumorcellen
Een centraal thema van het artikel is hoe verschillende gasdermine-eiwitten functioneren als moleculaire schakelaars binnen borstkankercellen. Varianten zoals GSDMD en GSDME kunnen signalen van chemotherapie, bestraling of aanvallen door immuuncellen omzetten in volle pyroptose. Andere, zoals GSDMC en sommige vormen van GSDMB, komen vaak hoger tot expressie in agressieve tumoren en kunnen de ziekte zowel bevorderen als remmen, afhankelijk van hoe ze geactiveerd worden. Veel borstkankers schakelen GSDME chemisch uit, waardoor pyroptose en immuunactivatie worden afgeremd. Het herstellen of selectief activeren van de juiste gasderminen kan bepalen of een therapie slechts enkele cellen doodt of de hele tumor in een in-situ vaccin verandert dat het immuunsysteem waarschuwt.
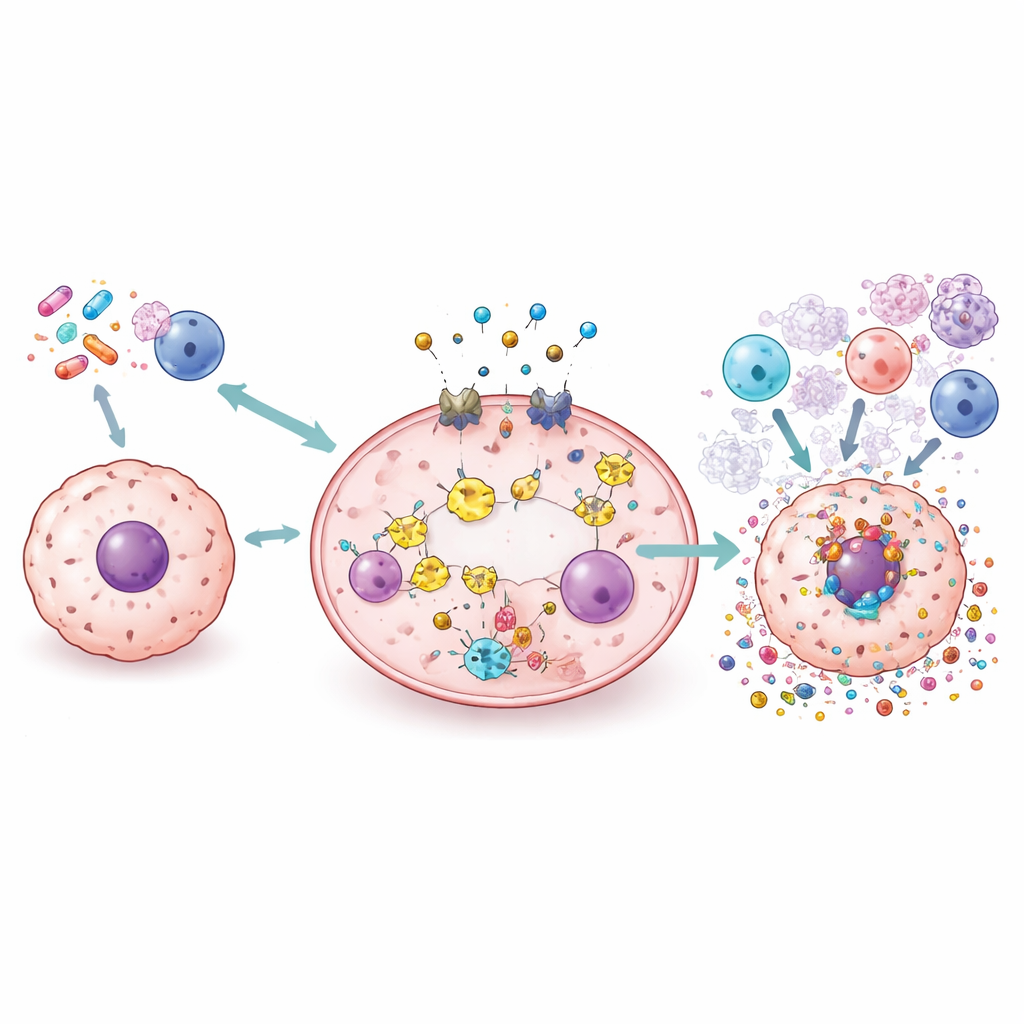
Nieuwe instrumenten: geneesmiddelen, nanodeeltjes, virussen en bestraling
De review inventariseert een breed scala aan strategieën in onderzoek om pyroptose veilig te benutten. Standaardmiddelen zoals cisplatine en doxorubicine kunnen worden hergebruikt of opnieuw geformuleerd om kankercellen richting gasdermine-gedreven openbarsten te duwen in plaats van stille celdood. Kleine moleculen kunnen delen van het pad versterken of blokkeren om de ontsteking fijn af te stemmen. Nanodeeltjes en biomimetische dragers worden ontworpen om chemotherapie, koperionen of licht-geactiveerde moleculen rechtstreeks in tumoren af te leveren, waar ze pyroptose veroorzaken terwijl gezonde weefsels worden gespaard. Oncolytische virussen en radiotherapie kunnen ook worden aangepast of gecombineerd met andere middelen om pyroptose uit te lokken en het immuunlandschap van de tumor te herstructureren, wat immuuncheckpointmiddelen mogelijk effectiever maakt.
Het afwegen van krachtige voordelen tegen reële risico’s
Omdat pyroptose zo ontstekingsbevorderend is, kunnen dezelfde reacties die het immuunsysteem helpen kanker te bestrijden ook gezond weefsel beschadigen of zelfs tumorgroei bevorderen als ze chronisch worden. De auteurs belichten vroege biomarkers — zoals genhandtekeningen, methyleringspatronen, fragmenten van gasdermine-eiwitten in het bloed en cytokineprofielen — die kunnen helpen bepalen welke patiënten het meest waarschijnlijk profiteren en wie een hoger risico loopt op gevaarlijke ‘cytokinestormen’. Geavanceerde nanomedicine-ontwerpen, zorgvuldig gekozen medicijncombinaties en realtime monitoring van ontstekingsmarkers worden allemaal onderzocht om de respons scherp maar gecontroleerd te houden.
Wat dit voor toekomstige patiënten kan betekenen
Simpel gezegd betoogt deze review dat het ‘luid laten sterven’ van kankercellen de borstkankerzorg kan transformeren. Door pyroptose in een nauwkeurig subgroepje tumorcellen teweeg te brengen, kunnen artsen zowel de tumor verkleinen als een krachtige, blijvende immuunrespons activeren, waardoor koude tumoren heet worden en beter reageren op moderne immuuntherapieën. Pyroptose is echter een veranderlijke bondgenoot: als ze te breed of te lang wordt ontketend, kan ze ontsteking verergeren of resistente cellen in de kaart spelen. Toekomstig onderzoek zal zich richten op het in kaart brengen wie baat heeft, het perfectioneren van gerichte afleversystemen en het uitvoeren van klinische trials die pyroptose-inducerende benaderingen combineren met immuunmiddelen. Als deze uitdagingen kunnen worden opgelost, kan het benutten van pyroptose een krachtige nieuwe dimensie toevoegen aan de behandeling van borstkanker.
Bronvermelding: Asiedu, R.K.F., Souley Abdou, M., Wei, R. et al. Harnessing pyroptosis in breast cancer therapy: immunological mechanisms and emerging biomaterial strategies. Cell Death Discov. 12, 157 (2026). https://doi.org/10.1038/s41420-026-02996-1
Trefwoorden: pyroptose, borstkanker, gasdermine, tumormicro-omgeving, nanomedicijn