Clear Sky Science · nl
Absolute dynamisch en relatief statisch: de relatie tussen glycolyse en OXPHOS in de ontwikkeling van kanker
Waarom de energiekeuzes van kanker ertoe doen
Kankercellen lijken op extreem gedisciplineerde duursporters: ze moeten zich voortdurend van brandstof voorzien om te groeien, zich te verspreiden en behandelingen te ontlopen. Deze review legt uit hoe tumorcellen twee hoofdenergiesystemen benutten — één snel en één efficiënt — en vooral hoe ze die systemen mengen en ertussen schakelen. Begrijpen hoe die energiestrategieën wisselen biedt een nieuw perspectief op diagnose en behandeling van kanker tijdens het hele ziekteverloop.
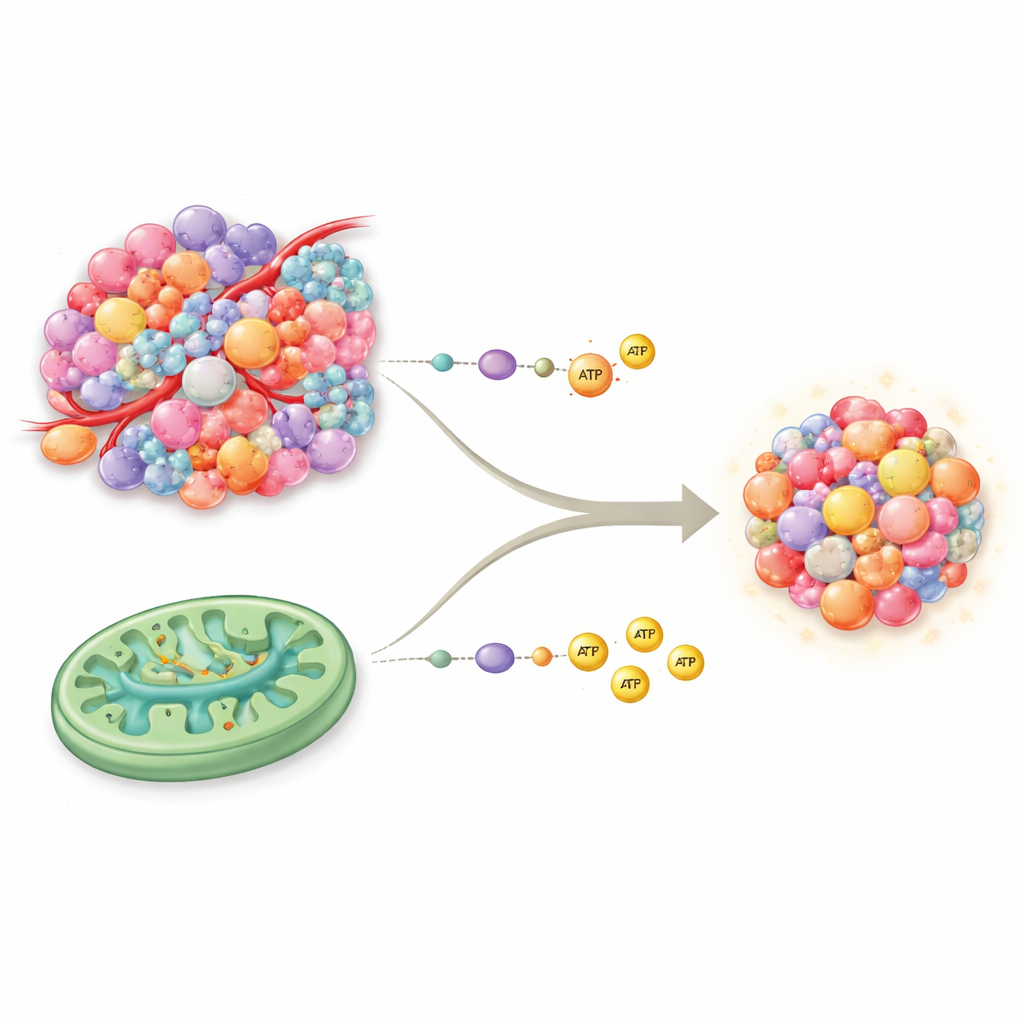
Twee hoofdwegen voor celbrandstof
Onze cellen produceren doorgaans energie via twee kernroutes. Glycolyse is het snelle, “klaar-kas”-systeem dat suiker snel afbreekt maar relatief weinig energie per eenheid oplevert. Oxidatieve fosforylering, of OXPHOS, vindt plaats in de mitochondriën en werkt meer als een hoogrendement energiecentrale: het levert veel meer energie maar vereist een goede zuurstof- en voedingsaanvoer. Decennialang werd gedacht dat kanker bijna uitsluitend op glycolyse vertrouwde, zelfs als er zuurstof aanwezig was — een patroon dat bekendstaat als het Warburg-effect. Nieuw bewijs kantelt dit simpele beeld: veel tumoren hebben volledig functionele mitochondriën en kunnen OXPHOS en de tricarbonzuurcyclus (TCA) naast glycolyse gebruiken, wat hen een rijkere en flexibeler energietoolbox geeft dan eerder werd aangenomen.
Verschillende celtypen, verschillende brandstofkeuzes
Een tumor is geen uniforme massa. Het is een klein ecosysteem met kankercellen, steuncellen, bloedvaten en immuuncellen, elk met specifieke brandstofbehoeften. Sommige kankercellen leven dicht bij bloedvaten en hebben volop zuurstof en voedingsstoffen; andere liggen diep in slecht bevoorraden gebieden. Daardoor kunnen cellen binnen dezelfde tumor glycolyse bevoordelen, vooral op OXPHOS vertrouwen of beide systemen tegelijk gebruiken. Deze metabole verscheidenheid — heterogeniteit genoemd — ontstaat door verschillen in bloedtoevoer, nutriëntniveaus, celtype en signalen uit de omgeving. Bovendien vertonen tumoren vaak metabole symbiose: glycolytische cellen exporteren lactaat als een ‘afval’product, dat naburige OXPHOS-afhankelijke cellen importeren en verbranden als waardevolle brandstof. Vergelijkbare lactaatuitwisseling vindt plaats tussen kankercellen en steuncellen zoals fibroblasten, endotheelcellen en immuunsuppressieve cellen, wat gezamenlijk de tumor helpt te gedijen en therapieresistentie bevordert.
Altijd in beweging: hoe tumorenergie in de tijd verschuift
Tumormetabolisme is niet alleen divers op elk willekeurig moment; het is ook sterk dynamisch. Naarmate tumoren groeien, ondervinden ze veranderende omstandigheden zoals lage zuurstof, verzuring, nutriënttekorten en variaties in weefselstijfheid. Onder harde, zuurstofarme omstandigheden schakelen veel kankercellen naar glycolyse. Bij zuurstofverzadiging, bij ophoping van zuren of bij suikertekort kunnen ze weer meer op OXPHOS vertrouwen. Dezelfde flexibiliteit verschijnt tijdens belangrijke biologische fases. Snel delende cellen leunen op glycolyse om bouwstenen te leveren voor nieuw DNA, vetten en membranen. Rustende cellen of cellen die in de bloedbaan circuleren, vertrouwen vaak meer op OXPHOS. Tijdens invasie en metastasering passen kankercellen hun brandstofkeuze herhaaldelijk aan: sommige stappen bevorderen glycolyse, andere OXPHOS, en metastatische cellen die nieuwe organen koloniseren stemmen hun metabolisme af op de ‘bodem’ van het doelweefsel.
Genen, enzymen en energiecentrales achter de schakeling
Diep in het cellulaire apparaat sturen genen en enzymen deze energiekeuzes. Oncogenen en tumorsuppressoren kunnen cellen richting glycolyse of OXPHOS duwen, of hen in staat stellen beide routes op te voeren. Mutaties of veranderingen in sleutelenzymen van de TCA, zoals die betrokken bij citraat, succinaat of isocitraat, kunnen het evenwicht verschuiven en soms kankerverwekkende signalen stimuleren zoals bloedvatvorming en invasie. Enzymen die op cruciale kruispunten zitten — bijvoorbeeld pyruvaatkinase M2, dat helpt beslissen of koolstof uit suiker energie of bouwmateriaal wordt — koppelen glycolyse aan mitochondriale functies. Ondertussen vergroten verschillen in aantal, structuur en prestatie van mitochondriën tussen tumorregio’s het spectrum van mogelijke energietoestanden verder.
Behandeling herdenken via een bewegend energiedoel
Aangezien tumorcellen tussen glycolyse en OXPHOS kunnen schakelen, is het blokkeren van slechts één pad vaak onvoldoende; de kanker kan dan haar brandstofverbruik omleiden en overleven. De auteurs betogen dat energiemetabolisme in kanker slechts kortstondig stabiel is en fundamenteel en voortdurend verandert. Zij stellen voor om tumoren te bekijken via een “energiemetabolismespectrum” dat in de tijd moet worden gemeten, niet slechts één keer. In de praktijk kan dit betekenen dat men de brandstofvoorkeuren van een tumor volgt in verschillende ziektestadia en remmers van glycolyse en OXPHOS in op maat gemaakte combinaties inzet. Dergelijke dynamische, door metabolisme geleide behandelstrategieën zouden de energievoorziening van de tumor beter kunnen afsnijden, zijn aanpassingsvermogen beperken en de langetermijnbeheersing van de ziekte verbeteren.
Bronvermelding: Bao, X., Hou, B., Guo, Z. et al. Absolute dynamic and relative static: the relationship of glycolysis and OXPHOS in cancer development. Cell Death Discov. 12, 136 (2026). https://doi.org/10.1038/s41420-026-02992-5
Trefwoorden: kankermetabolisme, glycolyse, oxidatieve fosforylering, tumormicro-omgeving, metabole plasticiteit