Clear Sky Science · nl
APOA2-gemedieerde endotheel-mesenchymale transitie en herschikking van lipidenmetabolisme in kanker veroorzaken resistentie tegen anti-angiogene geneesmiddelen via TGF-β
Waarom deze ontdekking belangrijk is voor patiënten
Artsen gebruiken steeds vaker middelen die levertumoren uithongeren door hun bloedtoevoer af te sluiten, maar veel patiënten zien na een aanvankelijk effect dat hun kanker niet meer reageert. Deze studie stelt een urgente vraag: waarom worden sommige levertumoren resistent tegen deze vaat-afsluitende behandelingen, en hoe kunnen we ze te slim af zijn? De onderzoekers onthullen een verborgen samenwerking tussen een bloedvet-eiwit en een krachtig groeisignaal die tumoren in staat stelt zowel hun bloedvaten als hun energiegebruik te herprogrammeren, wat wijst op een alternatieve benadering om een moeilijk te behandelen kanker aan te pakken.
Een tumor die leert te leven zonder zijn gebruikelijke levenslijn
Hepatocellulair carcinoom, de meest voorkomende vorm van leverkanker, is sterk afhankelijk van nieuwe bloedvaten om te groeien. Standaardmiddelen voor gevorderde ziekte zijn ontworpen om een belangrijke vaatgroeiplaat, gecentreerd rond VEGF en zijn receptor VEGFR2, te blokkeren. Toch blijven tumoren bij veel patiënten doorgroeien ondanks deze geneesmiddelen. Door tumormonsters te vergelijken van patiënten die wel of niet reageerden op het anti-angiogene middel apatinib, vonden de auteurs dat één gen, APOA2, opviel. Tumoren van resistente patiënten vertoonden duidelijk hogere niveaus van APOA2, een eiwit dat vooral bekend is vanwege zijn rol in het transport van vetten in het bloed. Dit deed de mogelijkheid rijzen dat APOA2 tumoren helpt te ontsnappen aan vaatgerichte medicatie.
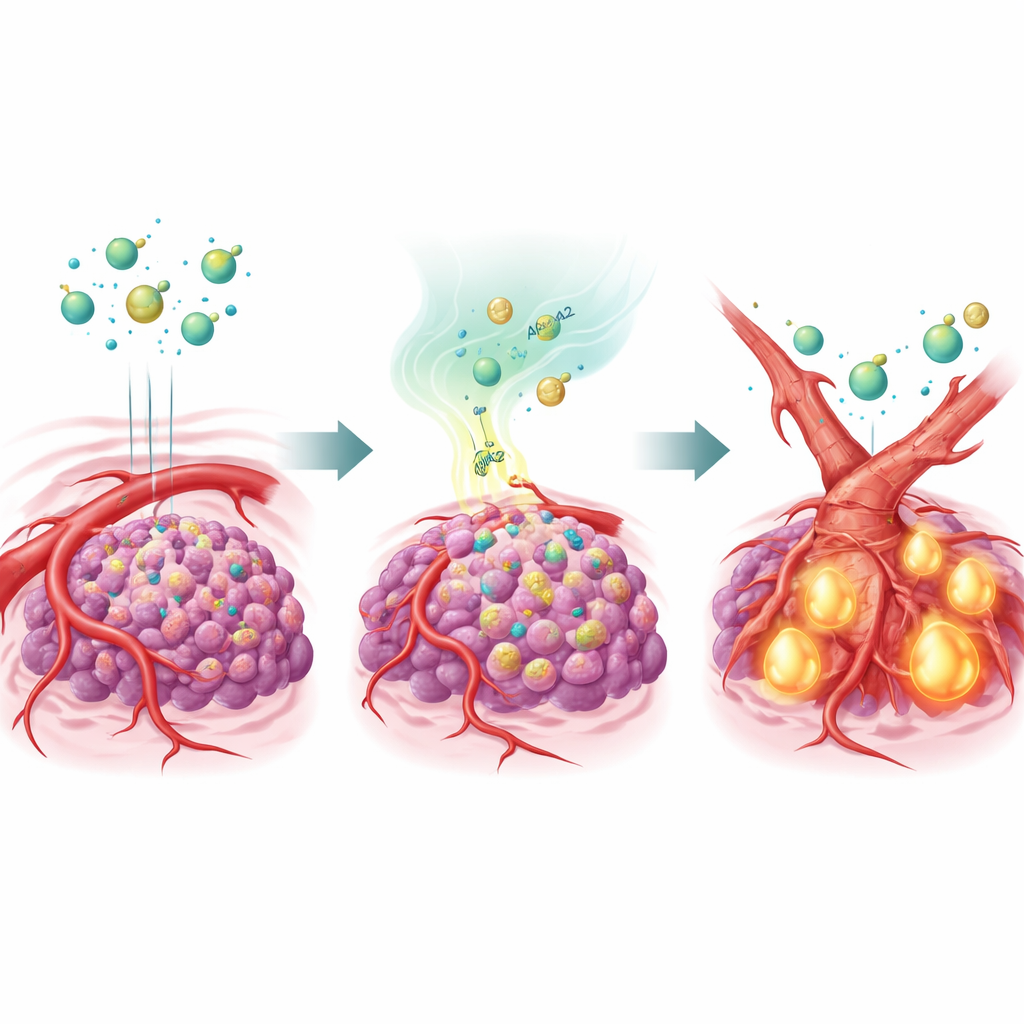
Een vettransporteiwit dat bloedvaten hervormt
Om dit idee te testen, produceerde het team leverkankercellen die te veel APOA2 aanmaakten en implanterde deze in muizen. Bij behandeling met verschillende anti-angiogene geneesmiddelen negeerden deze APOA2-rijke tumoren grotendeels de therapie: hun bloedvaten bleven aanwezig en de kankers bleven groeien. Gedetailleerde analyses toonden aan dat een meesterlijk signaal, TGF-β, sterk geactiveerd was in deze tumoren en dat de niveaus verhoogd waren zowel in de tumoromgeving als in het bloed van de dieren. TGF-β werkte op de cellen die bloedvaten bekleden en dreef hen tot identiteitsverandering in een proces dat endotheel-naar-mesenchymale transitie wordt genoemd. Terwijl ze veranderden naar een meer littekenachtige, mesenchymale staat, verloren deze cellen veel van hun VEGFR2, het zeer receptor-eiwit waar anti-angiogene middelen op mikken. In feite remodelden de vaten zichzelf naar een vorm die de geneesmiddelen niet langer konden bereiken.
Een metabole omweg die kankercellen van brandstof voorziet
Het verhaal eindigde niet bij de vaatwand. Hetzelfde door APOA2 aangedreven TGF-β-signaal herschreef ook hoe kankercellen zich van energie voorzien. In plaats van hoofdzakelijk afhankelijk te zijn van suikerafbraak, begonnen APOA2-rijke cellen meer vrije vetzuren uit hun omgeving op te nemen en deze in hun mitochondriën te verbranden via vetzuuroxidatie. Experimenten die voedingsstofgebruik en zuurstofconsumptie maten, lieten zien dat deze cellen meer afhankelijk werden van vetten als energiebron en meer cellulaire brandstof (ATP) produceerden. Deze verschuiving stelde tumorcellen in staat zich snel te blijven delen en celdood te vermijden, zelfs wanneer de bloedtoevoer onder druk stond door anti-angiogene behandeling.
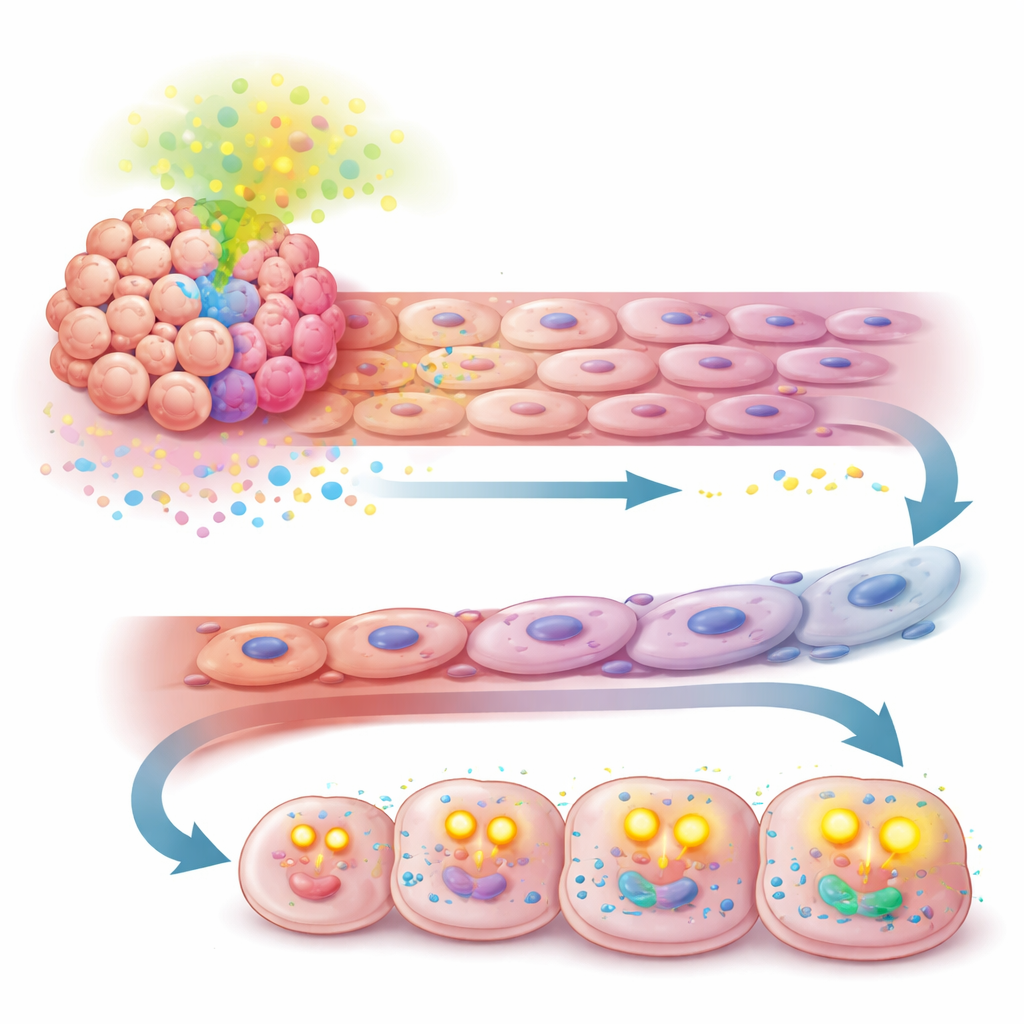
Een zwakke plek omzetten in een nieuw behandeldoel
Cruciaal is dat wanneer de onderzoekers TGF-β blokkeerden, de voordelen die APOA2 gaf verdwenen. Remmen van dit signaal in muismodellen verminderde de abnormale vaatveranderingen, herstelde de gevoeligheid voor therapie en vertraagde de tumorgroei. Nog veelbelovender was dat een dubbele antilichaamtherapie die zowel TGF-β als de immuunremmer PD-1 tegelijk blokkeert, beter werkte dan één van de twee benaderingen alleen in APOA2-rijke tumoren. Deze resultaten suggereren dat, in een subset van levertumoren met hoge APOA2, de ziekte stilletjes haar afhankelijkheid van het gebruikelijke VEGF-pad heeft verlegd naar een TGF-β-gericht traject dat zowel bloedvaten als tumormetabolisme ondersteunt.
Wat dit betekent voor de toekomstige zorg bij leverkanker
Voor een niet-specialist is de kernboodschap dat sommige levertumoren aan huidige vaatgerichte middelen ontkomen door zowel hun leidingsysteem als hun energievoorziening te herbedraden. Een vetgerelateerd eiwit, APOA2, zet het TGF-β-signaal aan, dat op zijn beurt bloedvaten camoufleert zodat bestaande middelen ze niet meer kunnen zien en kankercellen leert van vetten in plaats van suikers te leven. De studie suggereert dat het testen van tumoren op APOA2 patiënten kan aanwijzen die waarschijnlijk niet zullen profiteren van standaard anti-angiogene therapie maar mogelijk wel reageren op middelen die TGF-β blokkeren, vooral in combinatie met moderne immunotherapie. Samengevat: door bloot te leggen hoe tumoren zich aanpassen, wijst dit werk op een meer gerichte strategie die zowel de vaten als de energiebron van deze veerkrachtige kankers aanvalt.
Bronvermelding: Zhang, S., Fu, Z., Zhu, F. et al. APOA2-mediated endothelial mesenchymal transition and cancer lipid metabolism reprogramming confers antiangiogenic drug resistance through TGF-β. Cell Death Discov. 12, 119 (2026). https://doi.org/10.1038/s41420-026-02984-5
Trefwoorden: hepatocellulair carcinoom, resistentie tegen anti-angiogene therapie, APOA2, TGF-beta signalering, lipidenmetabolisme van kanker