Clear Sky Science · nl
Door botulinumtoxine veroorzaakte atrofie van de masseter spier is geassocieerd met verstoorde autofagische flux zonder tekenen van apoptose bij muizen
Waarom injecties in de kaakspier ertoe doen
Injecties met botulinumtoxine in de kauwspier van de kaak, de masseter, zijn tegenwoordig gebruikelijk in zowel geneeskundige als cosmetische klinieken. Ze kunnen kaakpijn verlichten en een vierkante kaaklijn versmallen, maar veel patiënten merken dat de spier maandenlang dunner en zwakker wordt. Deze studie bij muizen stelt een eenvoudige maar belangrijke vraag: wat gebeurt er binnen die spiercellen, en schaadt de behandeling de natuurlijke schoonmaak- en herstelmechanismen van de spier?
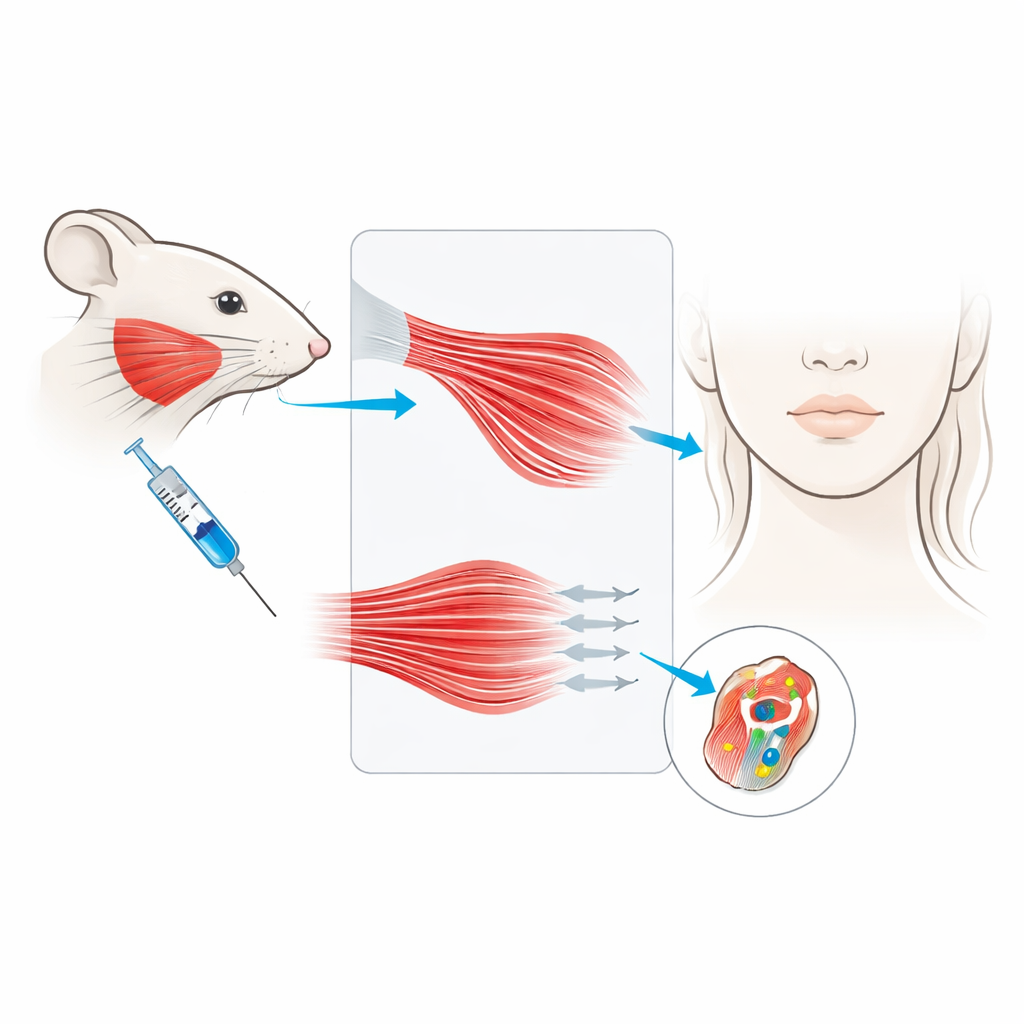
Kaakontspanners en krimpende spieren
De masseter helpt ons sterk te bijten en te kauwen. Wanneer deze spier overactief of vergroot raakt, kan dat bijdragen aan kaakgewrichtspijn en hoofdpijn, en sommige mensen laten de spier verkleinen voor een slankere onderkaak. Botulinumtoxine type A werkt door de zenuwsignalen die de spier tot samentrekking aanzetten te blokkeren, waardoor de spier tijdelijk verlamd raakt. Eerder onderzoek toonde aan dat deze zenuwblokkade leidt tot een meetbaar verlies van spiermassa en vezelgrootte bij dieren, wat wijst op echte atrofie in plaats van alleen ontspanning. Het was echter onduidelijk of deze krimp voortkomt uit celdood of uit veranderingen in de manier waarop de spier zijn componenten afbreekt en recyclet.
Controleren op celdood in de kaak
Een mogelijkheid was dat het toxine apoptose zou uitlokken, een vorm van geprogrammeerde celdood die vaak omschreven wordt als cellulair zelfmoord. Om dit te testen injecteerden de onderzoekers botulinumtoxine in één masseter bij volwassen muizen en saline in de tegenoverliggende zijde als controle. Ze keken vervolgens naar verschillende bekende moleculaire tekenen van apoptose en naar gebroken DNA in de kernen van spiercellen. Gedurende meerdere tijdpunten in de eerste week vonden ze geen toename van enige van deze doodsmarkers. Het aantal cellen met gefragmenteerd DNA bleef extreem laag, in tegenstelling tot positieve-controlemonsters waarin DNA-schade opzettelijk was geïnduceerd. Deze resultaten wijzen erop dat de spiervezels in de kaak na behandeling niet verloren gingen door een golf van klassieke celdood.
Het opruimsysteem van de spier raakt vast
Het team richtte zich vervolgens op autofagie, het interne recyclingsysteem van de cel. Autofagie verpakt versleten eiwitten en beschadigde structuren in kleine zakjes die fuseren met verteringscompartimenten, waardoor hun inhoud kan worden afgebroken en hergebruikt. In gezonde spier helpt dit proces de vezels sterk en functioneel te houden. Na injectie met botulinumtoxine zagen de onderzoekers een substantiële ophoping van meerdere eiwitten die deze recyclingzakjes markeren, samen met veel meer heldere puncta binnen de vezels onder het microscoop. Op het eerste gezicht lijkt dit op activatie van autofagie. Maar toen ze chloroquine gebruikten, een geneesmiddel dat de laatste stappen van autofagie blokkeert, stegen de niveaus van deze markers niet verder. Samen met de ongewijzigde verhouding van verschillende vormen van een sleutel-eiwit voor autofagie wijst dit patroon op een vastgelopen assemblagelijn: recyclingpakketjes worden gevormd maar niet afgeleverd of opgeruimd.
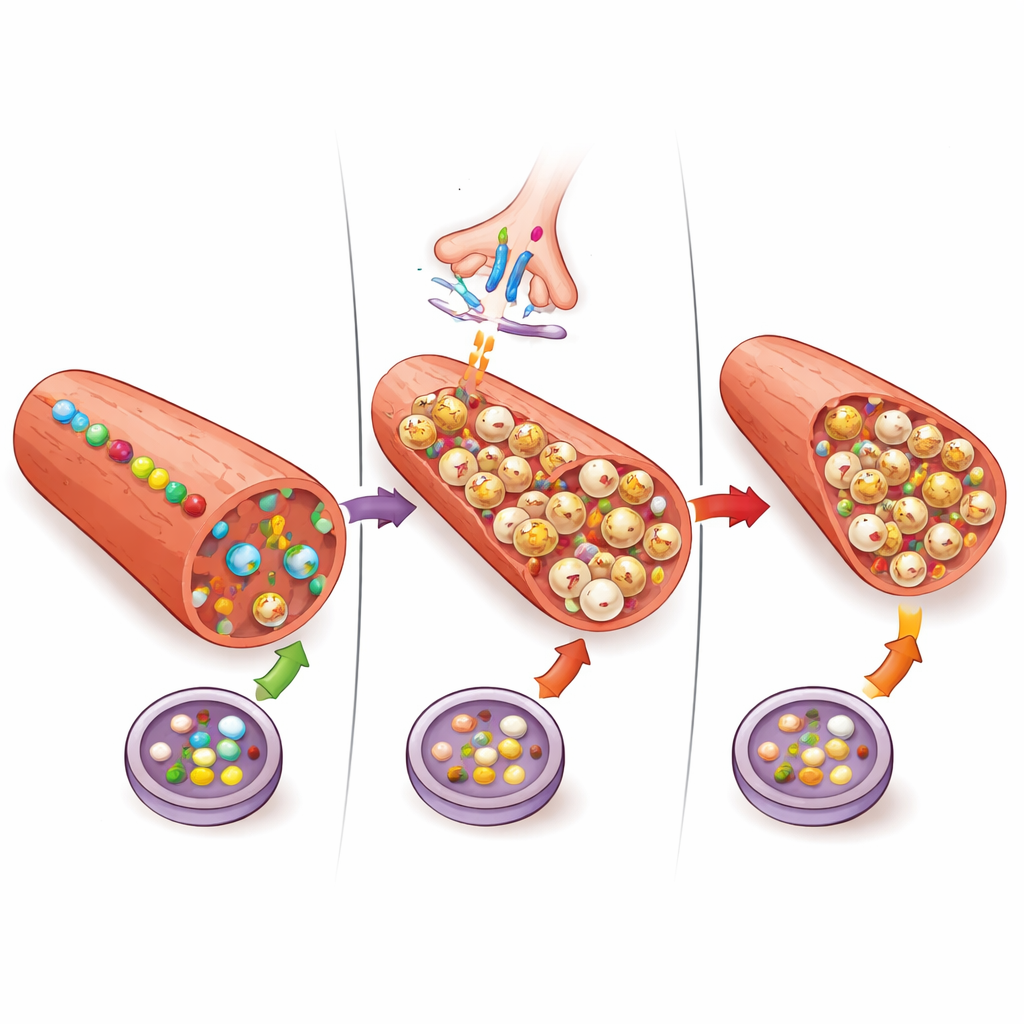
Van vastgelopen schoonmaak naar dunner wordende spier
De onderzoekers vroegen zich vervolgens af hoe deze moleculaire veranderingen zich verhouden tot daadwerkelijk spierverlies. Ze maten het spiergewicht en de diameter van individuele vezels en bevestigden dat de botulinum-behandelde masseter lichter was en uit dunner wordende vezels bestond. Belangrijk is dat de hoeveelheid ophoping van één recyclingmarker, LC3 genoemd, samenhing met hoeveel spiermassa elk dier verloor. Toen ze autofagie alleen blokkeerden met chloroquine, krimpten de vezels niet significant. Het toevoegen van chloroquine bovenop botulinumtoxine maakte de atrofie echter niet erger, wat suggereert dat beide ingrepen samenkomen op dezelfde geblokkeerde recyclingstap en dat deze blokkade op zichzelf niet direct de hoofdmechaniek van eiwitafbraak aandrijft. Andere systemen die eiwitten afbreken, zoals het ubiquitine–proteasoompad dat in eerder werk is aangetoond, doen waarschijnlijk het grootste deel van de afbraak.
Wat dit betekent voor patiënten en toekomstige zorg
In eenvoudige termen laat de studie zien dat gebruikelijke botulinuminjecties in de kaak in dit muismodel niet lijken te leiden tot het doden van spiercellen, maar wel het interne huishoudsysteem van de spier verstoren door de recyclingmachinerie te verstoppen. Deze verstopte toestand hangt samen met verlies van spieromvang, hoewel het waarschijnlijk niet de belangrijkste motor is van eiwitafbraak. Omdat de experimenten slechts enkele doseringen bij jonge mannelijke muizen omvatten, kunnen behandelingen in de echte wereld met herhaalde injecties, andere leeftijden of vrouwen andere langetermijneffecten hebben. Desondanks benadrukt het werk dat spieratrofie na botulinumtoxine biologisch complex is en dat het beschermen of herstellen van het recyclingmechanisme van de cel mogelijk op termijn kan helpen om ongewenst, blijvend spierverlies te verminderen bij mensen die op deze injecties vertrouwen voor medische of cosmetische redenen.
Bronvermelding: Quezada, E.R., Blanco, N., Llanos, P. et al. Botulinum toxin-induced masseter muscle atrophy is associated with impaired autophagic flux without signs of apoptosis in mice. Cell Death Discov. 12, 121 (2026). https://doi.org/10.1038/s41420-026-02982-7
Trefwoorden: botulinumtoxine, masseterspier, spieratrofie, autofagie, kaakstoornissen