Clear Sky Science · nl
KCTD1 stabiliseert c-Myc om PD-L1 te verhogen en antitumorimmuniteit te onderdrukken bij hepatocellulair carcinoom
Waarom dit ertoe doet voor toekomstige kankerzorg
Veel mensen met leverkanker profiteren niet van de meest veelbelovende immunotherapieën van vandaag, die erop gericht zijn de eigen T-cellen van het lichaam tegen tumoren los te laten. Deze studie onderzoekt waarom een belangrijke vorm van leverkanker, hepatocellulair carcinoom, zich nog steeds aan immuunaanvallen kan onttrekken, zelfs tijdens behandeling — en identificeert een nieuwe moleculaire schakelaar, KCTD1, die bestaande immunotherapie geneesmiddelen effectiever zou kunnen maken.
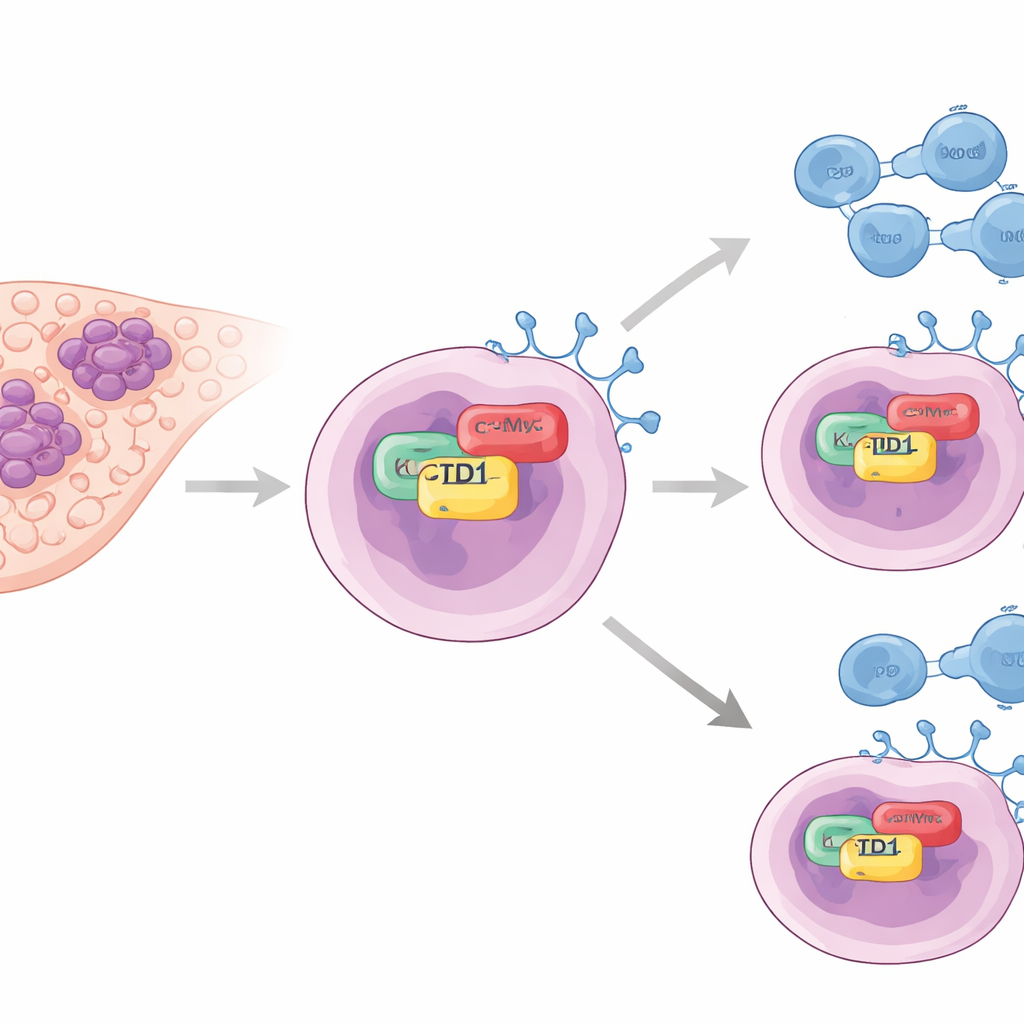
Een verborgen helper van de „uit”-schakelaars van tumoren
De auteurs richtten zich op een eiwit met de naam KCTD1, eerder in verband gebracht met groei van levertumoren maar nauwelijks bestudeerd in immuunontwijking. In tumormonsters van patiënten vonden ze dat de KCTD1-niveaus veel hoger waren in kankergezwelweefsel dan in normaal leverweefsel. Belangrijk is dat tumoren met veel KCTD1 ook hoge niveaus van PD-L1 hadden, een eiwit op het oppervlak van kankecellen dat zich bindt aan PD-1 op T-cellen en het immuunsysteem effectief het signaal geeft zich terug te trekken. Patiënten van wie de tumoren minder KCTD1 hadden, leefden doorgaans langer, wat suggereert dat dit eiwit samenhangt met zowel de ernst van de ziekte als de sterkte van het immuun schild van de tumor.
De moleculaire verbindingen in kankercellen leggen
Om te begrijpen hoe KCTD1 PD-L1 versterkt, werkte het team met leverkankercellijnen gekweekt in het laboratorium. Wanneer ze KCTD1 verminderden, daalden de PD-L1-eiwitniveaus en werd het resterende PD-L1 sneller afgebroken, wat aangeeft dat KCTD1 PD-L1 helpt stabiliseren in plaats van alleen het gen aan te zetten. Met biochemische pull-downexperimenten en fluorescentiemicroscopie lieten ze zien dat KCTD1 fysiek bindt aan een andere belangrijke kankerdrijver, het oncoproteïne c-Myc, in de celkern. Deze interactie vindt plaats via specifieke contactgebieden op beide eiwitten en leidt tot stabieler c-Myc, wat op zijn beurt de productie van PD-L1 verhoogt. Wanneer c-Myc op zichzelf werd gereduceerd, viel PD-L1 omlaag, zelfs als KCTD1 overvloedig aanwezig was, waarmee c-Myc de cruciale tussenliggende schakel in een KCTD1–c-Myc–PD-L1-keten wordt geplaatst.
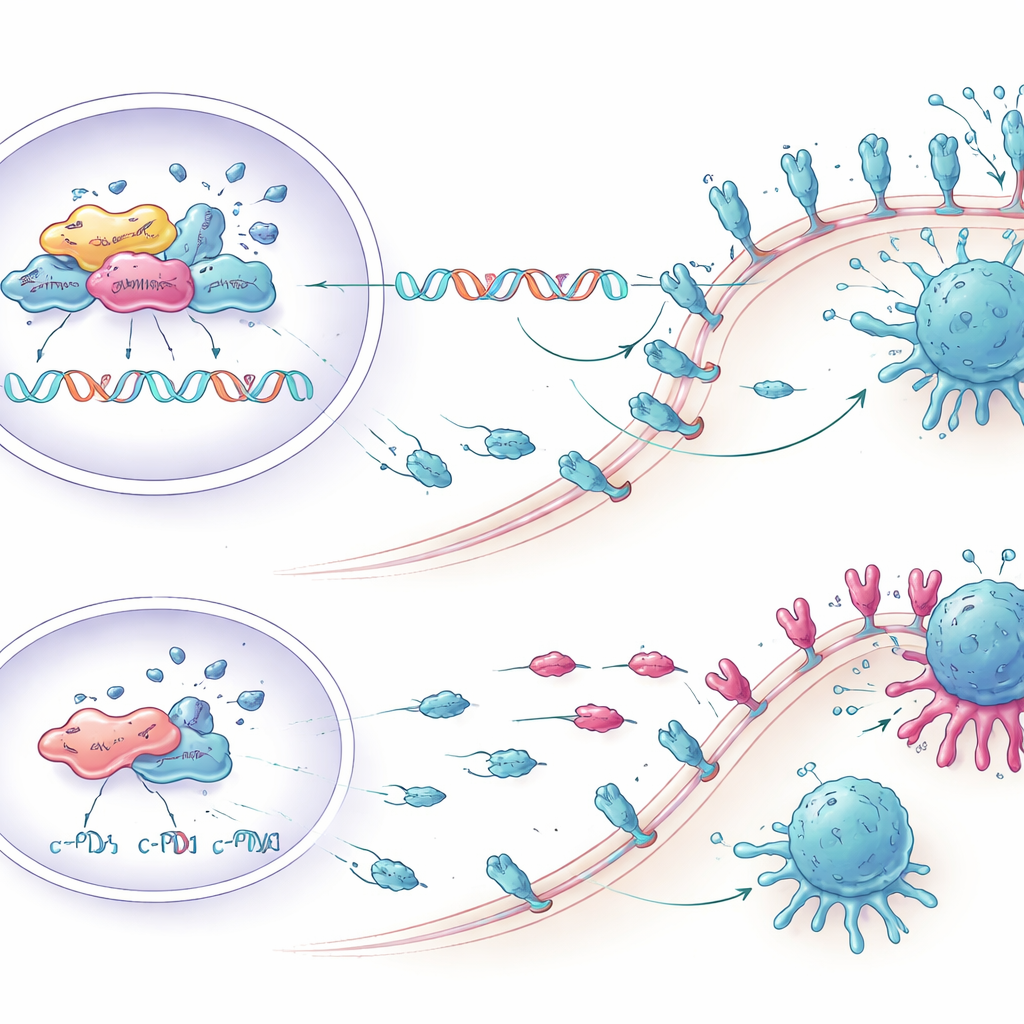
T-cellen in het laboratorium weer activeren
Vervolgens vroegen de onderzoekers of het verlagen van KCTD1 de immuunaanval daadwerkelijk kon versterken. Ze co-kweekten humane leverkankercellen met immuuncellen afkomstig van bloeddonoren. Tumorcellen die zo waren geconstrueerd dat ze minder KCTD1 en daardoor minder PD-L1 hadden, veroorzaakten sterkere reacties van CD8-T-cellen — de belangrijkste moordenaars van kankercellen in het immuunsysteem. Meer van deze T-cellen produceerden inflammatoire moleculen zoals TNF-α en interferon-gamma, vertoonden hogere markers van groei en activatie en toonden minder tekenen van uitputting. Hierdoor ondergingen meer tumorcellen geprogrammeerde celdood toen KCTD1 werd onderdrukt, wat aantoonde dat de moleculaire veranderingen zich vertaalden in echte verbeteringen in immuun-gemedieerde killing.
Het mechanisme in muizen testen
Om te zien of hetzelfde patroon in levende organismen geldt, implanterende het team muisleverkankercellen zonder KCTD1 direct in de lever van muizen. Tumoren met verminderde KCTD1 vormden minder en kleinere knobbels, toonden langzamere celdeling en hadden meer kankercellen die celdood ondergingen. Deze tumoren uitten ook minder c-Myc en PD-L1. Het verwijderen van CD8-T-cellen uit de muizen maakte een groot deel van dit voordeel ongedaan, wat aangeeft dat de vertraging van de tumor sterk afhankelijk was van T-celactiviteit. Ten slotte, toen de onderzoekers KCTD1-knockdown combineerden met een anti–PD-1-antistof — een bestaand immuuncheckpointmiddel — hadden de muizen de laagste tumorlast en de hoogste niveaus van CD4- en CD8-T-cellen die hun tumoren infiltreerden.
Wat dit voor patiënten zou kunnen betekenen
Samengevat onthult het werk KCTD1 als een centrale coördinator die c-Myc stabiliseert, PD-L1 op leverkankercellen verhoogt en de aanval van CD8-T-cellen afzwakt. Het verstoren van deze route maakt tumoren zowel kwetsbaarder voor het immuunsysteem als gevoeliger voor PD-1-blokkerende geneesmiddelen in muizen. Voor patiënten suggereert dit dat geneesmiddelen gericht tegen KCTD1 of het contactoppervlak met c-Myc in de toekomst gecombineerd zouden kunnen worden met huidige immunotherapieën om meer mensen met leverkanker te helpen profiteren van duurzame immuuncontrole van hun ziekte.
Bronvermelding: Zhong, D., Long, S., Dai, Y. et al. KCTD1 stabilizes c-Myc to upregulate PD-L1 and suppress anti-tumor immunity in hepatocellular carcinoma. Cell Death Discov. 12, 129 (2026). https://doi.org/10.1038/s41420-026-02975-6
Trefwoorden: hepatocellulair carcinoom, tumorimmunotherapie, PD-1 PD-L1-route, c-Myc-signaaltransductie, T-cel antitumorimmuniteit