Clear Sky Science · nl
Moleculaire inzichten in de antikankereffecten van Silodosine: een veelbelovende herbestemmingsstrategie voor borstkanker
Waarom een oud middel nieuwe aandacht krijgt
Borstkanker blijft een van de meest voorkomende en dodelijke vormen van kanker bij vrouwen, en veel patiënten raken uiteindelijk zonder effectieve behandelingsopties. Deze studie onderzoekt of silodosine, een pil die al veilig wordt gebruikt voor urinaire problemen bij mannen, kan worden herbestemd om borstkanker te bestrijden. Omdat het een goedgekeurd, betaalbaar geneesmiddel is met een bekend veiligheidsprofiel, zou aantonen dat het de groei van borstkankercellen kan vertragen of deze kan doden het traject naar nieuwe therapieën kunnen versnellen, vooral voor mensen met een agressieve ziekte.
Een bekend geneesmiddel in een nieuwe rol
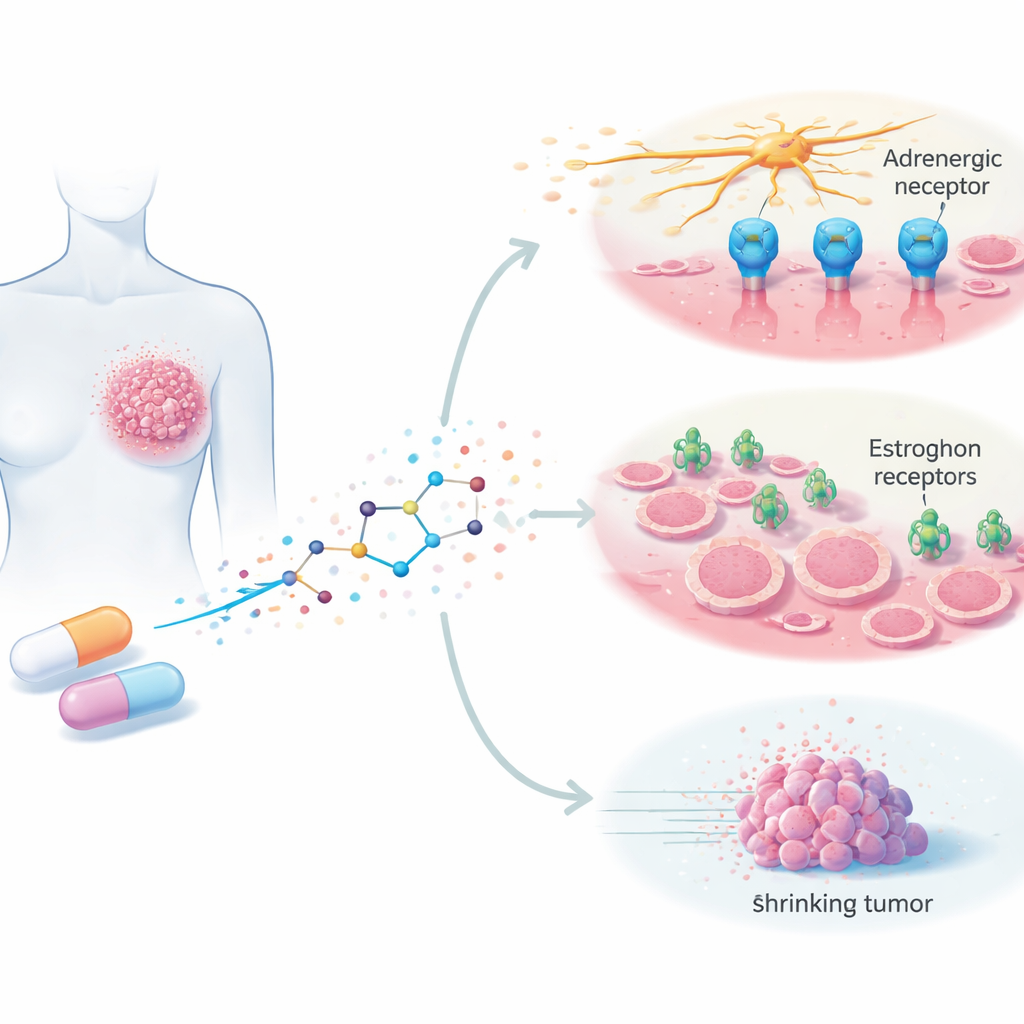
Silodosine wordt momenteel voorgeschreven om urinesymptomen door een vergrote prostaat te verlichten door bepaalde zenuwsignalen, de adrenerge signalen, te blokkeren. Deze signalen regelen meer dan spieren; groeiend bewijs suggereert dat ze ook tumoren kunnen helpen groeien, zich verspreiden en nieuwe bloedvaten vormen. De onderzoekers vroegen zich af of silodosine deze schadelijke signalen in borstkankercellen kan verstoren. Ze testten het geneesmiddel op verschillende menselijke borstkankercellijnen die in het laboratorium werden gekweekt, representatief voor zowel hormoongevoelige tumoren als moeilijk te behandelen triple-negatieve tumoren, en vergeleken de effecten met die op gezonde borstcellen.
Groeivertraging en het opwekken van celdood
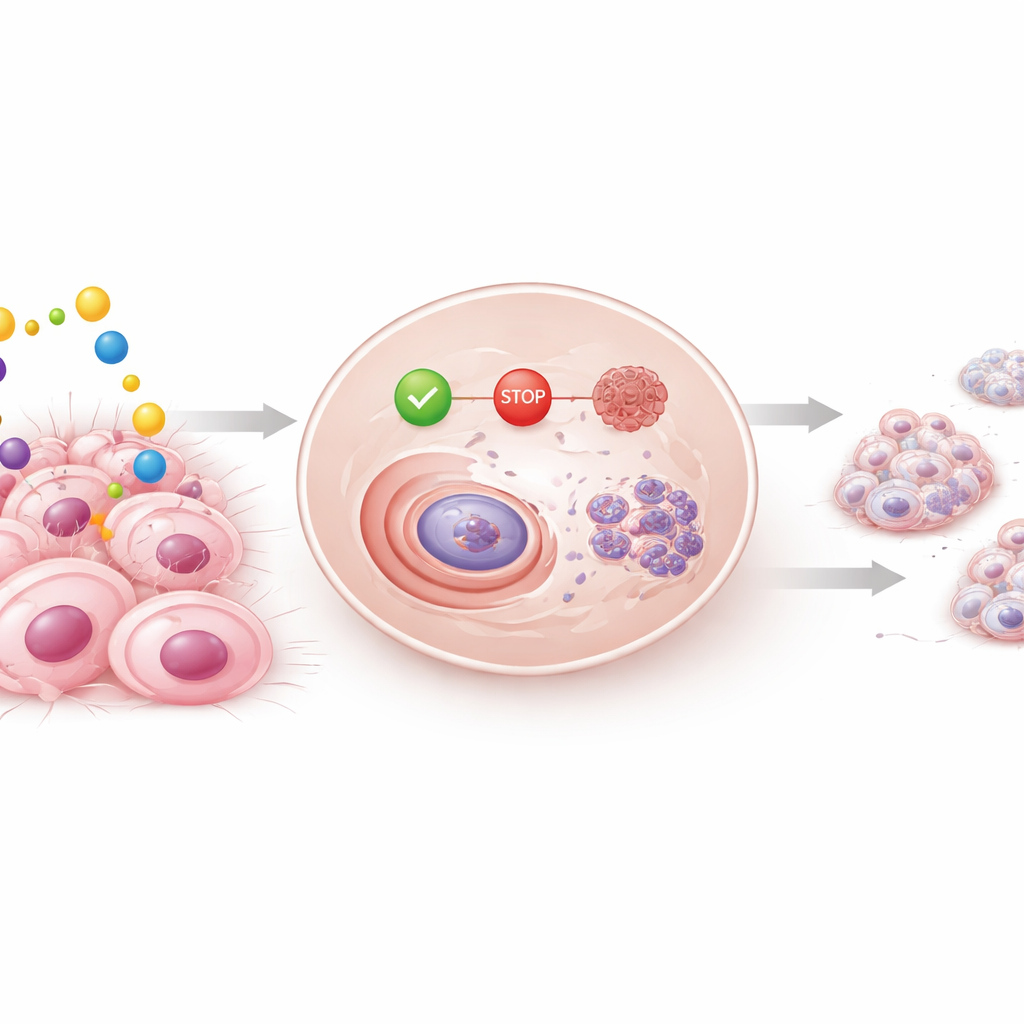
Wanneer borstkankercellen werden blootgesteld aan silodosine, vertraagde hun groei op een tijd- en dosisafhankelijke manier. Hormoongevoelige cellen werden vooral getroffen, maar zelfs agressieve triple-negatieve cellen toonden verminderde overlevingskansen en een gereduceerde mogelijkheid om kolonies te vormen na verloop van tijd, terwijl normale borstcellen grotendeels gespaard bleven. Verdere experimenten toonden aan wat binnenin de cellen gebeurde: silodosine hield ze vast in een vroege fase van de celcyclus, de reeks stappen die cellen moeten voltooien om zich te delen. Belangrijke ‘ga’-eiwitten die cellen naar deling duwen, namen af, terwijl ‘stop’-eiwitten en het bekende bewakerseiwit p53 toenamen. Het middel duwde de kankercellen ook richting geprogrammeerde celdood, zoals bleek uit het toenemend aantal cellen met gefragmenteerd DNA.
Belemmering van beweging en driedimensionale tumorachtige groei
Kanker wordt levensbedreigend wanneer cellen migreren en elders nieuwe tumoren vestigen. Met een krasachtige wond in een cellenlaag vonden de onderzoekers dat silodosine vertraagde hoe snel zowel hormoongevoelige als triple-negatieve borstkankercellen de kloof konden sluiten. Het team maakte ook gebruik van driedimensionale sferoïden, kleine bolvormige celclusters die echte tumoren beter nabootsen dan platte cellagen. Silodosine verminderde opvallend de vorming en grootte van deze sferoïden. Tegelijkertijd verlaagde het de niveaus van E-cadherine, een molecuul dat cellen helpt samen te houden en ook betrokken is bij groeisignalen en overlevingsroutes, wat suggereert dat het verstoren van cel-celcontacten een manier kan zijn waarop het geneesmiddel de organisatie en verspreiding van tumoren verstoort.
Een verrassend tweede doelwit binnen kankercellen
Silodosine is ontworpen om adrenerge receptoren te blokkeren, maar de gegevens pasten niet bij een eenvoudig verhaal van slechts één doelwit. Sommige borstkankercellen die sterk op het middel reageerden, hadden weinig of geen detecteerbare adrenerge receptor van het type waarop silodosine verondersteld wordt in te werken, en cellen met meer van deze receptor waren niet altijd gevoeliger. Om naar andere doelen te zoeken gebruikten de auteurs computermodellering om te onderzoeken of silodosine ook in oestrogeenreceptoren zou kunnen passen, de moleculaire schakelaars die veel borstkankers aansturen en die de belangrijkste doelwitten zijn van geneesmiddelen zoals tamoxifen. Hun simulaties toonden aan dat silodosine zich met betekenisvolle sterkte aan beide hoofdvormen van de oestrogeenreceptor kan binden, en interacteert met dezelfde sleutelcontactpunten als tamoxifen. Dit suggereert dat silodosine naast het blokkeren van zenuwgerelateerde signalen mogelijk ook als een modulator van de oestrogeenreceptor kan optreden.
Wat dit voor patiënten zou kunnen betekenen
Samengevoegd wijzen de experimenten op silodosine als een veelzijdige aanvaller van borstkankercellen: het vertraagt hun groei, duwt ze richting zelfdestructie, belemmert hun beweging en voorkomt dat ze zich organiseren tot tumorachtige sferoïden, terwijl het waarschijnlijk zowel adrenerge als oestrogeengerelateerde paden beïnvloedt. De effectieve doseringen in petrischaaltjes liggen hoger dan die bij patiënten worden bereikt met standaard urologische doseringen, dus er is meer werk in diermodellen en met combinatietherapieën nodig om het potentieel in de praktijk te beoordelen. Toch, omdat silodosine al is goedgekeurd en over het algemeen goed wordt verdragen, legt deze studie de basis voor herbestemming als onderdeel van nieuwe behandelstrategieën, met name voor patiënten met weinig opties zoals mensen met triple-negatieve borstkanker.
Bronvermelding: Pellegrino, M., Occhiuzzi, M.A., Marra, M. et al. Molecular insights into Silodosin’s anti-cancer effects: a promising repurposing strategy for breast cancer. Cell Death Discov. 12, 128 (2026). https://doi.org/10.1038/s41420-026-02973-8
Trefwoorden: borstkanker, herbestemming van geneesmiddelen, silodosine, oestrogeenreceptor, triple-negatieve borstkanker