Clear Sky Science · nl
De beschermende opregulatie van metallothioneïne-2A bij tussenwervelschijfdegeneratie remt ferroptose van nucleus pulposus-cellen via activatie van de PI3K/AKT/mTOR-route
Waarom dit rugprobleem ertoe doet
Laag rugpijn treft wereldwijd honderden miljoenen mensen en is een belangrijke oorzaak van beperkingen. Een belangrijke boosdoener is het geleidelijke verval van de schokdempende kussentjes tussen onze wervels, de tussenwervelschijven. Deze studie stelt een hoopvolle vraag: kunnen de beschermende moleculen van het lichaam deze schijven helpen beschermen tegen schade, en zou het versterken daarvan kunnen wijzen op nieuwe behandelingen voor chronische rugpijn? 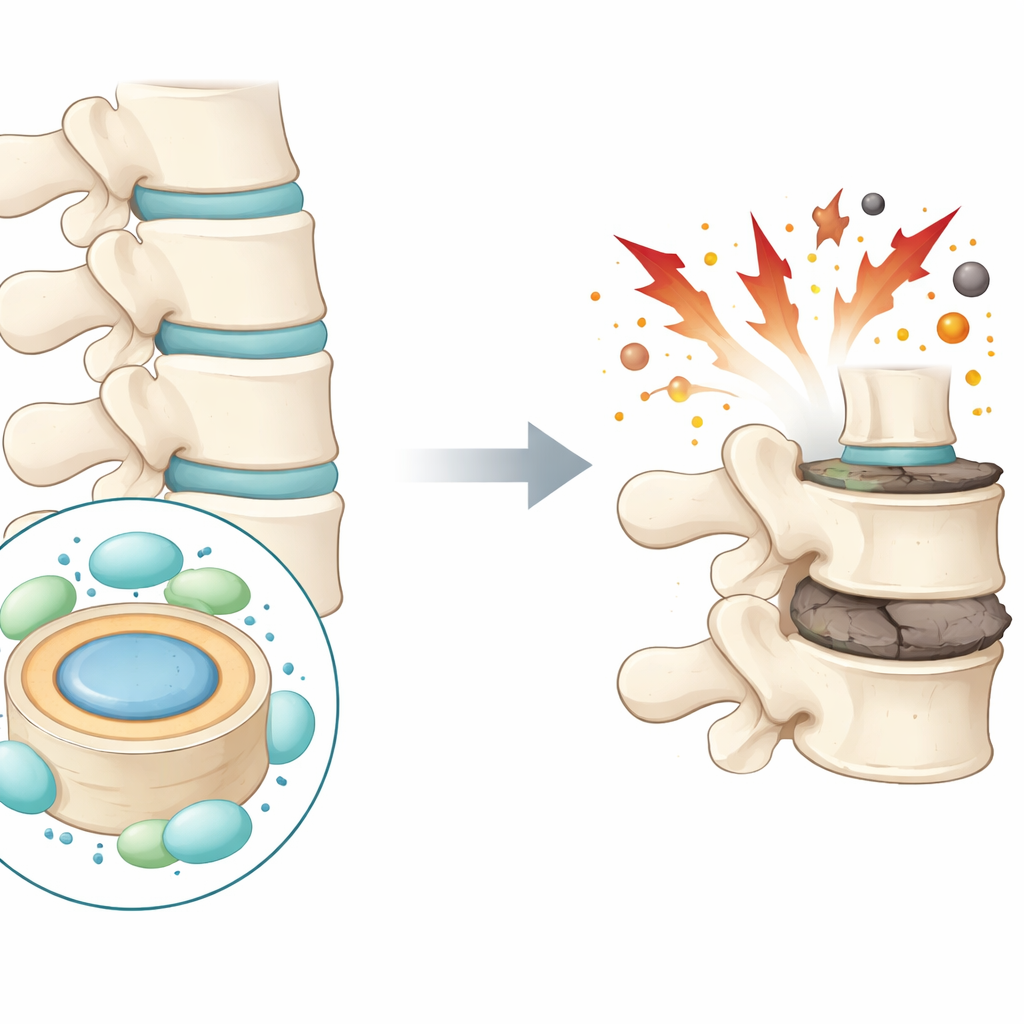
De kussens in de wervelkolom
Elke tussenwervelschijf heeft een zachte, gelachtige kern genaamd nucleus pulposus, omgeven door een steviger ring. Deze structuren werken als schokdempers voor de wervelkolom. Wanneer schijven degenereren, sterven de cellen in het centrale deel af en slijt de ondersteunende matrix van eiwitten en water. De schijf wordt platter en scheurt, wat kan leiden tot pijn en beperkte beweging. De auteurs richten zich op een specifiek type celdood dat pas recent aandacht kreeg in veel aandoeningen: ijzer-gedreven, oxidatie-gerelateerde celdood, bekend als ferroptose. Zij vermoeden dat dit proces een sleutelrol speelt bij het afbraakproces van de schijf.
Wanneer ijzer en oxidatie misgaan
Ferroptose wordt geactiveerd wanneer vrij ijzer en reactieve zuurstofmoleculen zich ophopen in cellen, waardoor vetten in celmembranen en met name de kleine energiecentrales, de mitochondriën, beschadigd raken. Het team analyseerde single-cell genetische data van menselijk schijfweefsel en vond duidelijke aanwijzingen dat ferroptose-gerelateerde genen veranderd zijn in degenererende schijven. Met name markers die normaal cellen beschermen tegen dit soort schade, zoals het enzym GPX4, waren verminderd in versleten schijven van zowel patiënten als ratten. Tegelijkertijd waren markers die schade en ontsteking bevorderen verhoogd, wat een beeld schetst van cellen onder oxidatieve aanval tijdens schijfdegeneratie.
Een ingebouwde metaalbindende beschermer
Onder de vele genen die veranderden in zieke schijven, stak er één bovenuit: metallothioneïne‑2A (MT2A), een klein eiwit dat metalen zoals zink bindt en schadelijke reactieve moleculen kan wegvangen. MT2A-niveaus waren opvallend hoger in ernstiger gedegenereerde menselijke schijven en in een ratmodel van schijfletsel. Op het eerste gezicht lijkt dit paradoxaal—waarom zou een beschermend molecuul stijgen in beschadigd weefsel? De onderzoekers stelden de hypothese op dat het lichaam een compenserende respons inzet om de toename van ijzer-gedreven stress tegen te gaan. In kweekschalen, wanneer schijfcellen werden blootgesteld aan een chemische stof die oxidatieve stress nabootst, stegen MT2A-niveaus terwijl de celgezondheid achteruitging, wat de gedachte versterkt dat het wordt aangezet als verdediging.
Bescherming omlaag en omhoog draaien
Om te testen of MT2A daadwerkelijk beschermend is in plaats van schadelijk, stelden de onderzoekers de niveaus ervan zorgvuldig bij in menselijke schijfcellen. Wanneer zij de productie van MT2A blokkeerden, veroorzaakte oxidatieve stress veel meer celdood, meer ijzerophoping, sterkere lipided Schade en ernstig beschadigde mitochondriën. Wanneer ze MT2A juist verhoogden, of de cellen behandelden met een bekende remmer van ferroptose, werden veel van deze problemen verlicht: ijzer en reactieve moleculen daalden, beschermende antioxidanten herstelden zich en mitochondriën zagen er gezonder uit. Deze veranderingen weerspiegelden zich ook in een betere instandhouding van de ondersteunende matrixeiwitten van de cellen, die cruciaal zijn om schijven vol en functioneel te houden. 
Een sleutelsignaleringsroute binnen de cel
Dieper gravend onderzochten de wetenschappers hoe MT2A beschermende signalen binnen cellen afgeeft. Gensequencing en eiwitmetingen wezen op de PI3K/AKT/mTOR-route, een bekend intern controlesysteem dat groei, stofwisseling en overleving beïnvloedt. Het verlagen van MT2A dempte de activiteit van deze route, terwijl het verhogen van MT2A deze activeerde. Wanneer de onderzoekers geneesmiddelen gebruikten om verschillende stappen in deze route te blokkeren, verdwenen de voordelen van MT2A-overexpressie: markers van ferroptose stegen opnieuw, oxidatieve schade keerde terug en schijfcellen verloren meer van hun structurele eiwitten. Dit suggereert dat MT2A schijfcellen grotendeels beschermt door deze pro-overlevingssignaalroute te activeren, die op zijn beurt ferroptose onderdrukt.
Proof of concept in dieren
Ten slotte vroegen de onderzoekers of het verhogen van MT2A daadwerkelijk de schijfdegeneratie in een levend organisme kon vertragen. Bij ratten veroorzaakten zij schijfletsel met een naaldprik en brachten daarna een virus in dat ontworpen was om MT2A rechtstreeks in de schijf te verhogen. Weken later toonden beeldvorming en weefselanalyse aan dat schijven met extra MT2A meer van hun hoogte behielden, een duidelijkere interne structuur hadden en minder verlies van belangrijke matrixeiwitten vertoonden vergeleken met onbehandelde beschadigde schijven. Markers van ferroptose waren ook verminderd, wat de gedachte ondersteunt dat MT2A helpt het schijfkussen te beschermen tegen instorting door oxidatieve en ijzerstress.
Wat dit betekent voor toekomstige zorg bij rugpijn
Samenvattend suggereert het werk dat MT2A niet slechts een bijstander is maar een ingebouwd veiligheidsmechanisme dat omhoogschakelt wanneer schijven beginnen te falen, in een poging cellen te verdedigen tegen schadelijke ijzer-gedreven oxidatie. Door een intern overlevingspad te activeren beperkt MT2A een specifieke vorm van celdood, behoudt het de structuur van de schijf en vertraagt het degeneratie—althans in diermodellen en celkweken. Voor patiënten duidt dit op MT2A en zijn signaalpartners als veelbelovende doelwitten voor geneesmiddelen of gen-gebaseerde therapieën gericht op het beschermen of verjongen van tussenwervelschijven, mogelijk met meer opties dan alleen pijnbestrijding en chirurgie op de lange termijn.
Bronvermelding: Cai, H., Zheng, Hl., Chen, Qz. et al. The protective up-regulation of metallothionein-2A in intervertebral disc degeneration inhibits nucleus pulposus cell ferroptosis through activation of the PI3K/AKT/mTOR pathway. Cell Death Discov. 12, 111 (2026). https://doi.org/10.1038/s41420-026-02972-9
Trefwoorden: lage rugpijn, tussenwervelschijfdegeneratie, ferroptose, metallothioneïne-2A, PI3K AKT mTOR-route