Clear Sky Science · nl
Multi-omics onthult heterogeniteit en functionele populaties van oligodendrocytvoorlopercellen geïnduceerd door humane neurale stamcellen
Waarom bescherming van de isolatie van de hersenen belangrijk is
De bedrading van onze hersenen is afhankelijk van een vette laag genaamd myeline, die zenuwvezels omsluit als isolatie rondom elektrische kabels. Wanneer myeline beschadigd raakt, zoals bij multiple sclerose en andere aandoeningen, vertragen of falen signalen, wat problemen veroorzaakt met beweging, gezichtsvermogen en denken. Deze studie onderzoekt een speciale groep menselijke cellen die myeline kunnen herbouwen en stelt een praktische vraag: welke cellen zijn het meest geschikt voor toekomstige celtherapieën om deze cruciale isolatie te herstellen?
Van startcellen naar myelinebouwers
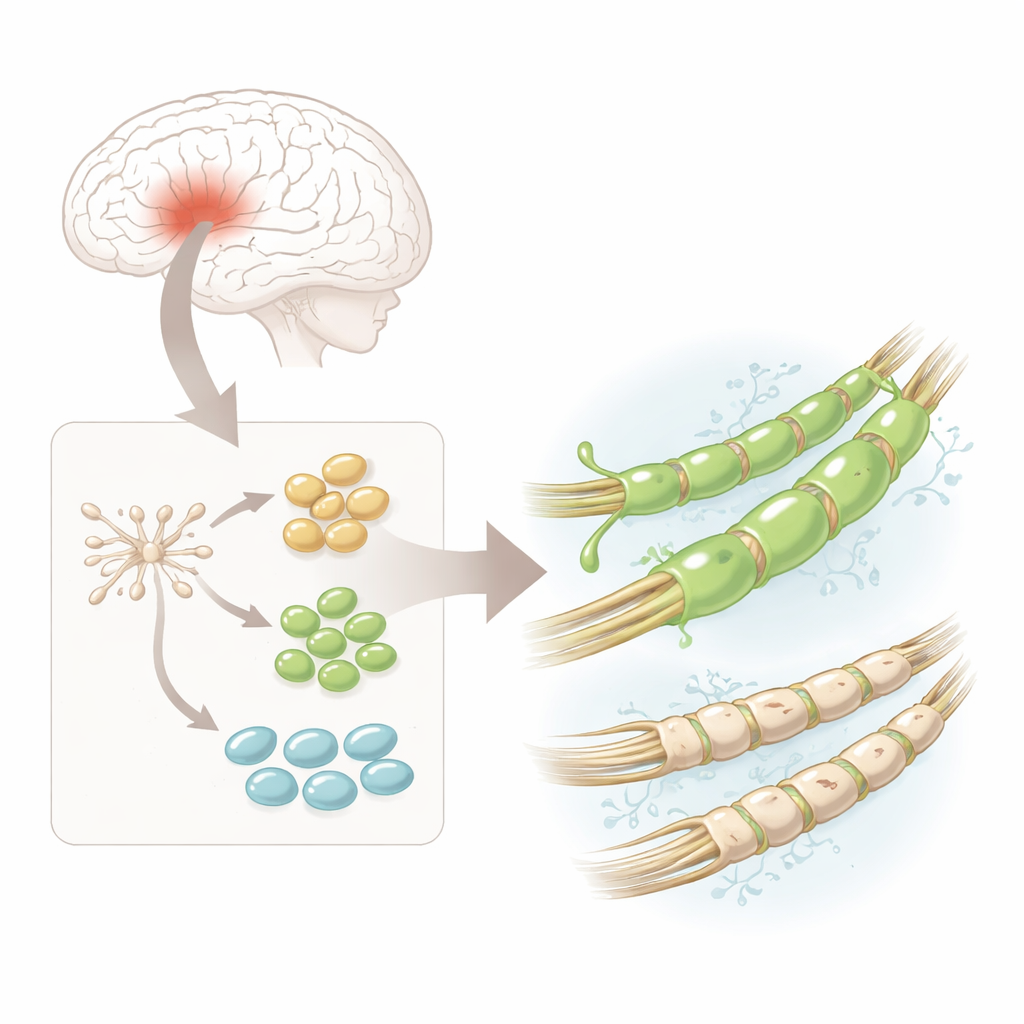
De onderzoekers begonnen met humane neurale stamcellen—veelzijdige startcellen verkregen uit foetaal hersenweefsel die al gericht zijn op het worden van cellen van het zenuwstelsel. In het laboratorium zetten ze deze stamcellen aan tot differentiatie naar oligodendrocytvoorlopercellen, of hOPC’s, die directe voorlopers zijn van de myelinevormende cellen. Onder de microscoop veranderden de cellen van eenvoudige ronde vormen naar complexere vormen met meerdere vertakkingen, en schakelden ze kenmerkende eiwitten aan die stappen markeren op weg naar rijpe myelineproducerende cellen. Dit leverde een betrouwbare, relatief veilige bron van menselijke myelinebouwende voorlopercellen voor gedetailleerde analyse.
Eén celtype, veel verborgen varianten
Met behulp van single-cell RNA-sequencing—een methode die afleest welke genen actief zijn in duizenden individuele cellen—ontdekte het team dat de hOPC’s niet allemaal hetzelfde waren. In plaats daarvan groepeerden ze in drie hoofdfasen: vroege “pre-voorlopers”, meer gecommitteerde voorlopercellen en cellen die een volledige oligodendrocytidentiteit naderden. Door alle stadia heen stak één gen erbovenuit: PDGFRA, dat codeert voor een receptoreiwit in het celmembraan. Een zeer gevoelige beeldvormingstechniek genaamd RNA-Scope bevestigde dat PDGFRA’s bericht en eiwit in elke fase overvloediger waren dan andere sleutelmarkeerders, wat suggereert dat deze receptor bijzonder capabele myelinebouwende cellen kan definiëren.
Het uitsorteren van de krachtigste herstelcellen
Om dit idee te testen, splitsten de wetenschappers hOPC’s in twee groepen op basis van de aanwezigheid van de PDGFR-α-receptor aan het celoppervlak. Ze vergeleken vervolgens PDGFR-α–positieve cellen, PDGFR-α–negatieve cellen en ongesorteerde cellen in een reeks functionele testen. Wanneer getransplanteerd in “shiverer”-muizen—die geen normale myeline kunnen vormen—produceerden de PDGFR-α–positieve cellen dichtere, compactere myeline rondom zenuwvezels dan de andere groepen. Deze cellen migreerden ook verder en deelden zich sneller in laboratoriumassays. Met andere woorden: de PDGFR-α–positieve populatie was het meest vitaal in verplaatsen naar plaatsen waar ze nodig waren, in aantal vergroten en isolatie herbouwen.
Interne signalen die groei en herstel aansturen
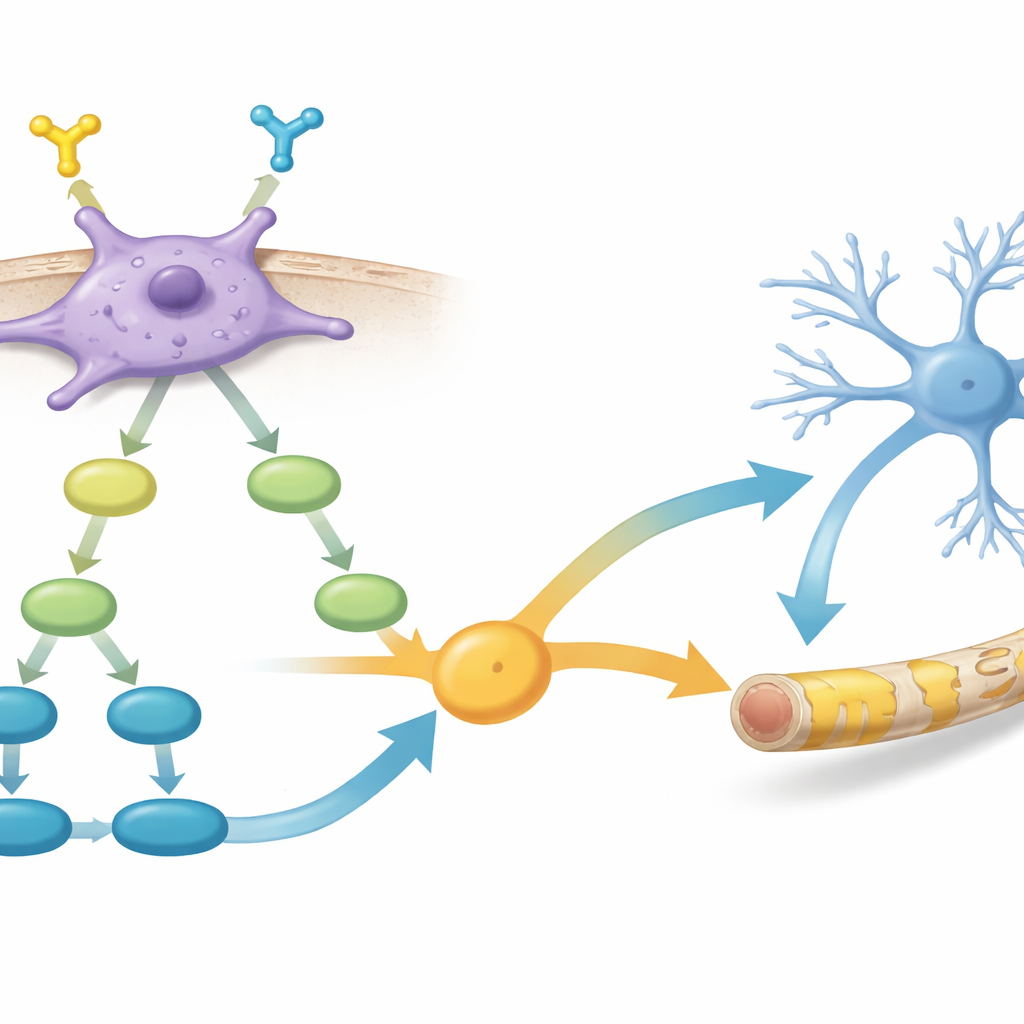
Dieper gravend vergeleek het team de genactiviteit tussen PDGFR-α–positieve en –negatieve cellen. Ze ontdekten dat de positieve cellen netwerken van genen activeerden die betrokken zijn bij gliacelgroei en myelinevorming, evenals meerdere sleutelroutes van intracellulaire signalering. Twee paden sprongen er met name uit: PI3K–AKT–mTOR, lang in verband gebracht met celgroei en myelineproductie, en TGF-β-signaaltransductie, die beïnvloedt hoe jonge hersencellen hun lotsbestemmingen kiezen. De gegevens suggereerden dat activering van PDGFR-α inschakelt naar PI3K–AKT–mTOR, wat op zijn beurt TGF-β–gerelateerde signalen versterkt, en samen duwen deze routes cellen in de richting van effectieve myelinebouwers.
Myelineherstel versterken met een chemische hulp
De onderzoekers vroegen zich vervolgens af of ze deze veelbelovende cellen nog verder konden verbeteren. Ze behandelden PDGFR-α–positieve hOPC’s met een klein molecuul dat het TGF-β-pad activeert en onderzochten zowel genactiviteit als gedrag. Na behandeling vertoonden deze cellen hogere niveaus van meerdere myelinegerelateerde genen en produceerden ze dikkere, meer volledige myelinescheden wanneer ze in shiverer-muizen werden getransplanteerd, vergeleken met onbehandelde PDGFR-α–positieve cellen. Dit ondersteunt het idee dat het zorgvuldig bijsturen van interne signaalroutes in al goed geselecteerde voorlopercellen hun prestaties als levende myelineherstelmiddelen verder kan verbeteren.
Wat dit betekent voor toekomstige behandelingen
Voor niet-specialisten is de kernboodschap dat niet alle myelinebouwende voorlopercellen gelijk zijn. Door krachtige genlezende en beeldvormingstools te combineren, identificeert deze studie een opvallende subgroep—PDGFR-α–positieve hOPC’s—die beter migreren, zich meer delen en myeline effectiever herbouwen dan hun leeftijdsgenoten. Het benadrukt ook interne signaleringsroutes die chemisch bijgestuurd kunnen worden om deze cellen nog krachtiger te maken. Gezamenlijk bieden deze inzichten een routekaart voor het ontwerpen van veiligere, efficiëntere celtherapieën om de isolatie van de hersenen te herstellen bij aandoeningen waarbij myeline verloren gaat.
Bronvermelding: Ye, D., Zhou, H., Qu, S. et al. Multi-omics reveals heterogeneity and functional populations of oligodendrocyte progenitor cells induced by human neural stem cells. Cell Death Discov. 12, 112 (2026). https://doi.org/10.1038/s41420-026-02971-w
Trefwoorden: myelineherstel, oligodendrocytvoorlopercellen, neurale stamcellen, celtherapie, single-cell RNA-sequencing