Clear Sky Science · nl
Mitochondriale bio-energetica–SASP kruisbestuiving bepaalt senolytische werkzaamheid bij therapie-geïnduceerde senescentie
Waarom het uitschakelen van “zombie”-kankercellen zo lastig is
Veel moderne kankergeneesmiddelen doden niet elke tumorcel direct. In plaats daarvan belanden sommige cellen in een limbo-achtige toestand die senescentie wordt genoemd: ze stoppen met delen maar blijven leven, een beetje als “zombie”-cellen. Deze therapie-geïnduceerde senescentie kan aanvankelijk nuttig zijn, maar als ze blijven hangen kunnen ze herval, resistentie en bijwerkingen aanwakkeren. Wetenschappers testen daarom senolytische middelen die selectief senescentie cellen doden. Dit artikel stelt een ogenschijnlijk simpele vraag: waarom sterven sommige senescentie kankercellen wanneer ze aan senolytica worden blootgesteld, terwijl andere hardnekkig overleven?
Stroomcentrales die hun verleden onthouden
In het hart van de studie staan mitochondriën, de kleine stroomcentrales in cellen. De auteurs onderzochten of de manier waarop mitochondriën verschillende brandstoffen verbranden — zoals suikers, vetten en aminozuren — beïnvloedt hoe gevoelig senescentie kankercellen zijn voor senolytica die een overlevingsproteïne genaamd BCL‑xL targeten. Met een hoogdoorvoertest (MitoPlate S‑1) maakten ze functionele “vingerafdrukken” van mitochondriale activiteit in meerdere kankercellijnen voor en na het aanzetten van senescentie door verschillende behandelingen (DNA‑beschadigende middelen, mitotische blokkeringen, oxidatieve stress of celcyclusremmers). Ze ontdekten dat therapie-geïnduceerde senescentie geen eenduidige mitochondriale toestand produceerde. In plaats daarvan liet elk middel een distinctief “bio-energetisch stempel” achter, waardoor veranderde hoe breed en intensief mitochondriën verschillende energiebronnen konden aanspreken. Cruciaal was dat deze flexibiliteit bovenop een bestaande basislijn lag: de oorspronkelijke mitochondriale configuratie van de ouderlijke kankercellen bepaalde een bovengrens — het “plafond” — voor hoe sterk een latere senolytische respons kon zijn.
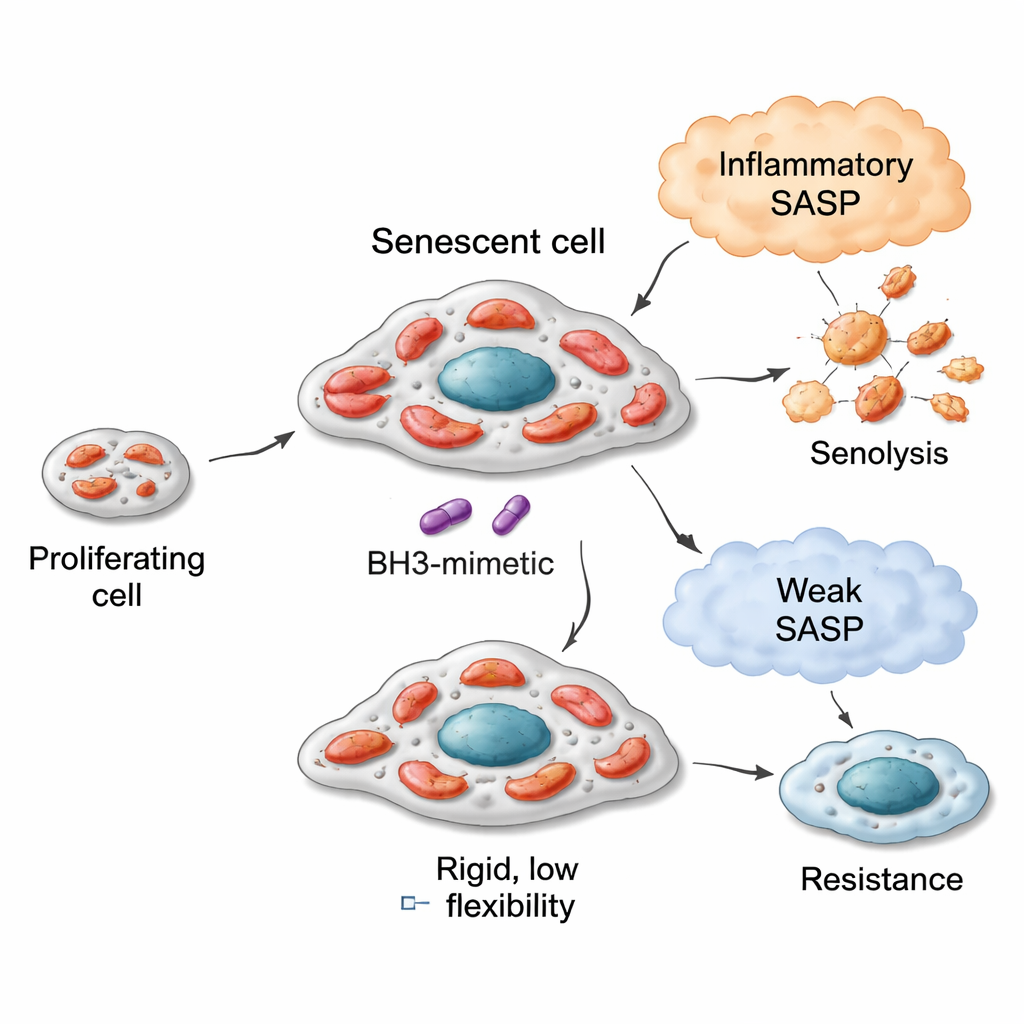
Flexibele motoren, verschillende brandstoffen en senolytische gevoeligheid
In long-, borst- en darmkankermodellen bleken senescentie cellen met meer flexibele mitochondriën — in staat om een breder scala aan brandstoffen te oxideren — doorgaans kwetsbaarder voor BCL‑xL–gerichte senolytica zoals navitoclax (ABT‑263) en A1331852. Bijvoorbeeld, longkankercellen die door het middel bleomycine in senescentie werden gedreven ontwikkelden mitochondriën die krachtig vele substraten gebruikten, vooral die gekoppeld aan vetzuurafbraak en bepaalde aminozuurroutes. Deze cellen waren zeer gevoelig voor senolytica. Ter contrast lieten cellen die door een CDK4/6‑remmer (palbociclib) in senescentie waren gebracht een smaller metabool repertoire zien en reageerden slecht op dezelfde senolytische middelen. Toch kende deze relatie grenzen: borstkankercellen konden na senescentie ook metabolisch flexibel worden, maar omdat hun beginnende mitochondriën minder ‘geprimed’ waren voor apoptose, bleef hun maximale senolytische respons bescheiden. Darmkankercellen met defecte apoptotische mechanismen bleven resistent ongeacht hoe hun metabolisme verschoven. Een enkele maat — hoe goed cellen de brandstof succinaat bij de basislijn verbrandden — diende als een eenvoudige indicator van deze geërfde mitochondriale capaciteit.
Wanneer metabolisme met ontsteking spreekt
Senescentie cellen staan bekend om de SASP, een cocktail van uitgescheiden inflammatoire en groeifactoren die omliggende weefsels beïnvloeden. Het team onderzocht hoe mitochondriaal metabolisme verbonden is met dit secretiegedrag met behulp van cellen die waren uitgerust met een reporter voor miR‑146a, een microRNA dat wordt aangezet door de belangrijkste inflammatoire schakelaar NF‑κB. Ze vonden dat hoewel algemene SASP‑profielen grotendeels werden bepaald door het celtype, alleen bepaalde senescentiestaten deze NF‑κB/miR‑146a‑as activeerden. Dat waren dezelfde staten die goed reageerden op BCL‑xL senolytica. Belangrijk is dat deze “inflammatoire SASP‑positieve” senescentie cellen ook een versterkt gebruik van vetzuuroxidatie vertoonden en een transcriptionele opwaartse verschuiving in genen die langeketenvetten naar mitochondriën transporteren. Het blokkeren van vetzuurtoegang met het middel etomoxir dempte miR‑146a‑activatie zonder senescentie volledig terug te draaien, wat suggereert dat de keuze van mitochondriale brandstof helpt bij het toestaan van een inflammatoire, senolytisch‑toegankelijke SASP.
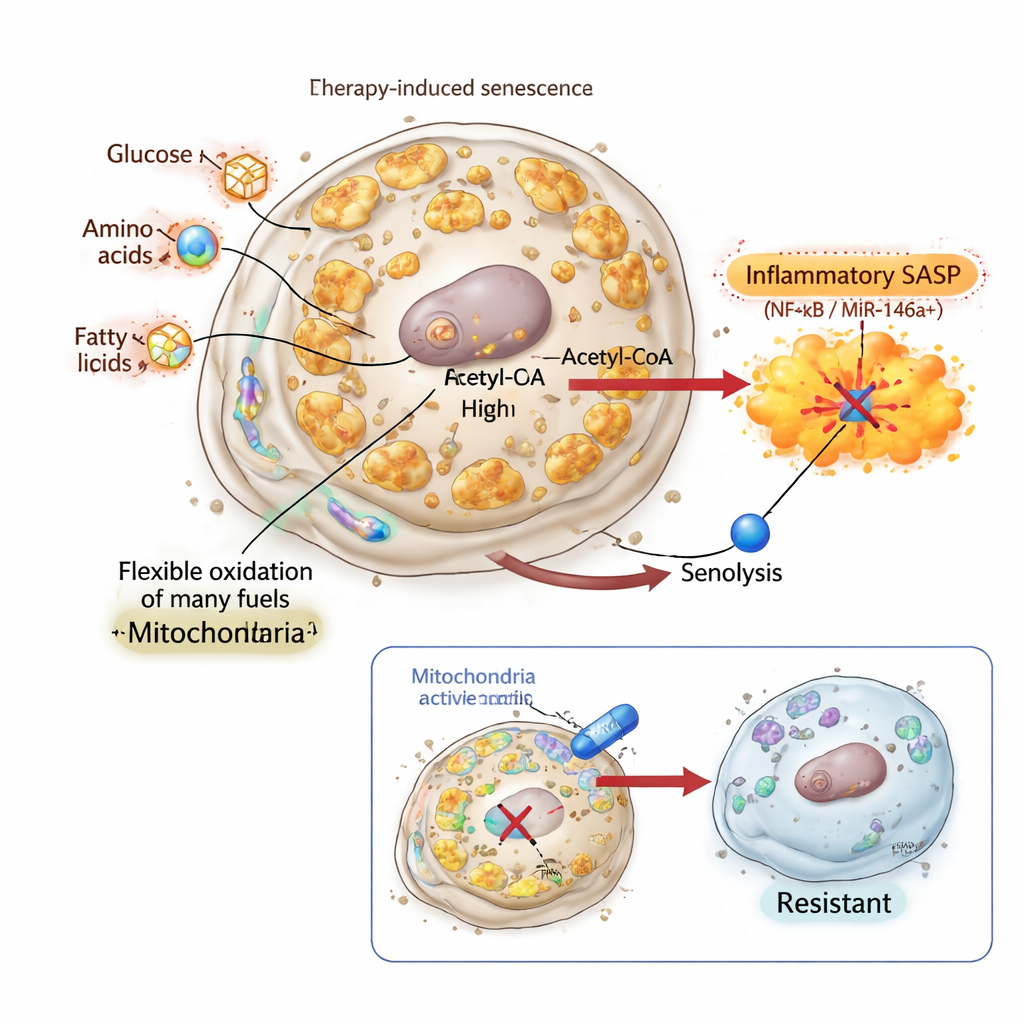
Het signaal dempen en ondoodbare senescentie cellen creëren
Om te testen of de inflammatoire SASP werkelijk vereist is voor senolytische killing, gebruikten de onderzoekers inflachromene, een verbinding die chromatine‑eiwitten HMGB1 en HMGB2 bindt en hun rol in het activeren van SASP‑genen blokkeert. In long‑ en borstkankercellen induceerde inflachromene een schoolvoorbeeld van een senescentiefenotype: cellen werden groot, stopten met delen en stapelden senescentiemarkers op. Hun mitochondriale massa en bio-energetische activiteit namen aanzienlijk toe, en hun brandstofgebruik werd duidelijk heringericht. Toch was hun SASP verzwakt en bleef de miR‑146a‑reporter grotendeels stil. Opvallend genoeg waren deze SASP‑loze senescentie cellen volledig resistent tegen BCL‑xL–gerichte senolytica, ondanks bio‑energetisch actieve, geherprogrammeerde mitochondriën en verminderde expressie van het klassieke anti‑apoptotische gen BCL2. Dit toonde aan dat mitochondriale veranderingen alleen niet voldoende zijn; zonder een mitochondrion‑gestuurde inflammatoire output faalt de senolytische “tweede klap”.
Wat dit betekent voor toekomstige kankerbehandelingen
Voor de niet‑specialist komt de conclusie van de studie neer op het volgende: het doden van therapie‑geïnduceerde “zombie” kankercellen wordt beheerst door een gelaagde schakeling. Ten eerste bepaalt de oorspronkelijke gezondheid en bedrading van de mitochondriën in een tumorcel hoe ver senolytica ooit kunnen reiken. Ten tweede kan de specifieke behandeling die senescentie veroorzaakt het mitochondriale metabolisme richting meer of minder flexibiliteit duwen, en zo cellen dichter bij of verder van de rand van apoptose brengen. Ten derde — en het doorslaggevendste — werken senolytica alleen goed als metabole herprogrammering succesvol een inflammatoir SASP‑programma activeert dat terugpraat met de kern. Zonder die inflammatoire kruiscommunicatie kunnen senescentie cellen een doodlopende, medicijnresistente toestand worden. In de praktijk suggereert dit dat toekomstige therapieën geoptimaliseerd kunnen worden door zowel mitochondriale flexibiliteit als SASP‑ontsteking functioneel in tumoren te testen en vervolgens senescentie‑inducerende middelen en senolytica in combinaties te kiezen die ervoor zorgen dat de “zombie” cellen niet alleen bevroren zijn, maar ook klaar zijn om te worden verwijderd.
Bronvermelding: Llop-Hernández, À., Verdura, S., López, J. et al. Mitochondrial bioenergetics-SASP crosstalk determines senolytic efficacy in therapy-induced senescence. Cell Death Discov. 12, 103 (2026). https://doi.org/10.1038/s41420-026-02967-6
Trefwoorden: cellulaire senescentie, mitochondriën, senolytica, kankermetabolisme, inflammatoire SASP