Clear Sky Science · nl
Caspase-activatie versterkt anti-Desmogleïne 3-geïnduceerde acantholyse in de menselijke epidermis
Wanneer het lichaam zijn eigen huidlijm aanvalt
Pemphigus vulgaris is een zeldzame maar gevaarlijke aandoening waarbij het immuunsysteem van het lichaam de “lijm” aanvalt die huidcellen bij elkaar houdt, wat pijnlijke blaren en open zweren veroorzaakt. Deze studie kijkt onder de microscoop om een cruciale vraag te beantwoorden: ontstaan deze blaren alleen omdat antilichamen die lijm blokkeren, of dragen extra signalen voor celdood bij aan het uit elkaar scheuren van huidcellen? Begrip hiervan kan leiden tot gerichtere en mildere behandelingen voor patiënten.
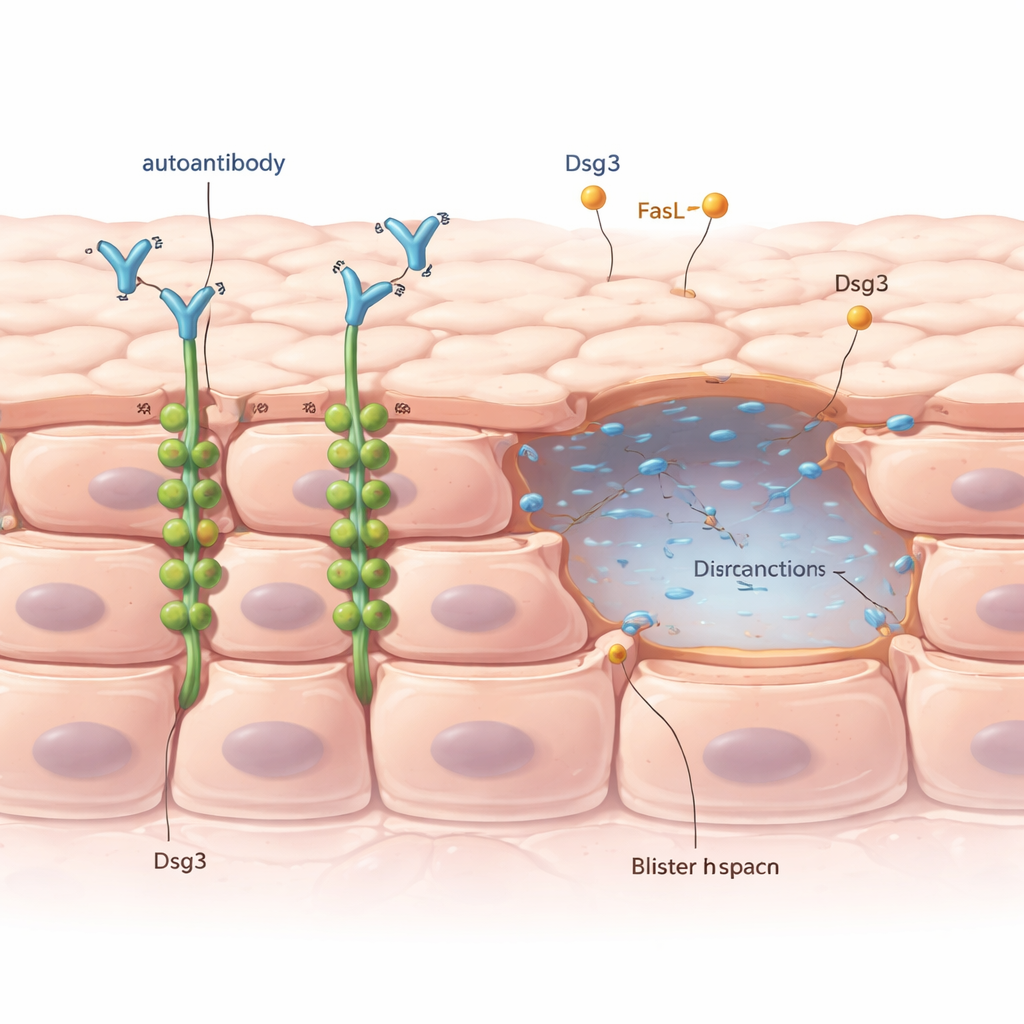
Hoe huidcellen normaal aan elkaar blijven zitten
De buitenste laag van onze huid bestaat uit dicht opeengepakte cellen die met kleine structuren, desmosomen genoemd, aan elkaar verbonden zijn; die functioneren als klinknagels tussen naburige cellen. Een belangrijk bestanddeel van deze klinknagels is een eiwit genaamd desmogleïne 3, of kortweg Dsg3. Bij pemphigus vulgaris maken patiënten antilichamen die per ongeluk binden aan Dsg3. Artsen weten al lang dat deze antilichaanaanval leidt tot een proces dat acantholyse heet, waarbij huidcellen contact verliezen en blaren ontstaan. Maar het is raadselachtig dat blaren alleen op bepaalde plaatsen en momenten verschijnen, ook al zijn de schadelijke antilichamen over de huid verspreid.
Antilichamen alleen kunnen de schade op gang brengen
Om te zien wat de antilichamen zelf doen, gebruikten de onderzoekers stukjes gezond menselijk huid en een in het laboratorium gekweekte huidcellijn. Ze brachten ze in contact met een goed bestudeerd anti-Dsg3-antilichaam. Ze ontdekten dat dit antilichaam de cel–cel-adhesie kon verzwakken en acantholyse kon veroorzaken, zelfs zonder het inschakelen van de gebruikelijke celdoodmachinerie in de cellen. De sleutelgebeurtenis was dat Dsg3 van het celoppervlak werd weggetrokken naar het celinterieur, vaak verpakt in kleine vesikels. Deze verwijdering van Dsg3 uit de “klinknagels” tussen cellen maakte de desmosomen korter en minder effectief, waardoor cellen begonnen te scheiden.
Wanneer celdoodsignalen meespelen, wordt het erger
Het team vroeg zich vervolgens af of een bekend celdoodsignaal bij pemphigus, een molecule genaamd Fas-ligand (FasL), dit beeld verandert. FasL kan enzymen activeren die caspases heten, vooral caspase-8, die normaal gesproken cellen richting geprogrammeerde celdood sturen. In huidmonsters van patiënten en in hun huidmodel zagen de onderzoekers actieve caspase-8 in beschadigde gebieden zonder klassieke tekenen van stervende cellen. Toen ze kleine, niet-dodelijke hoeveelheden FasL samen met het anti-Dsg3-antilichaam toevoegden, ontstonden er sneller en ernstiger blaren, met name in de diepere lagen van de epidermis. In kweekcellen verzwakte FasL op zichzelf de adhesie niet, maar in combinatie met het antilichaam nam het celuit elkaar vallen sterk toe — en deze versterking verdween toen caspase-8 werd geblokkeerd.
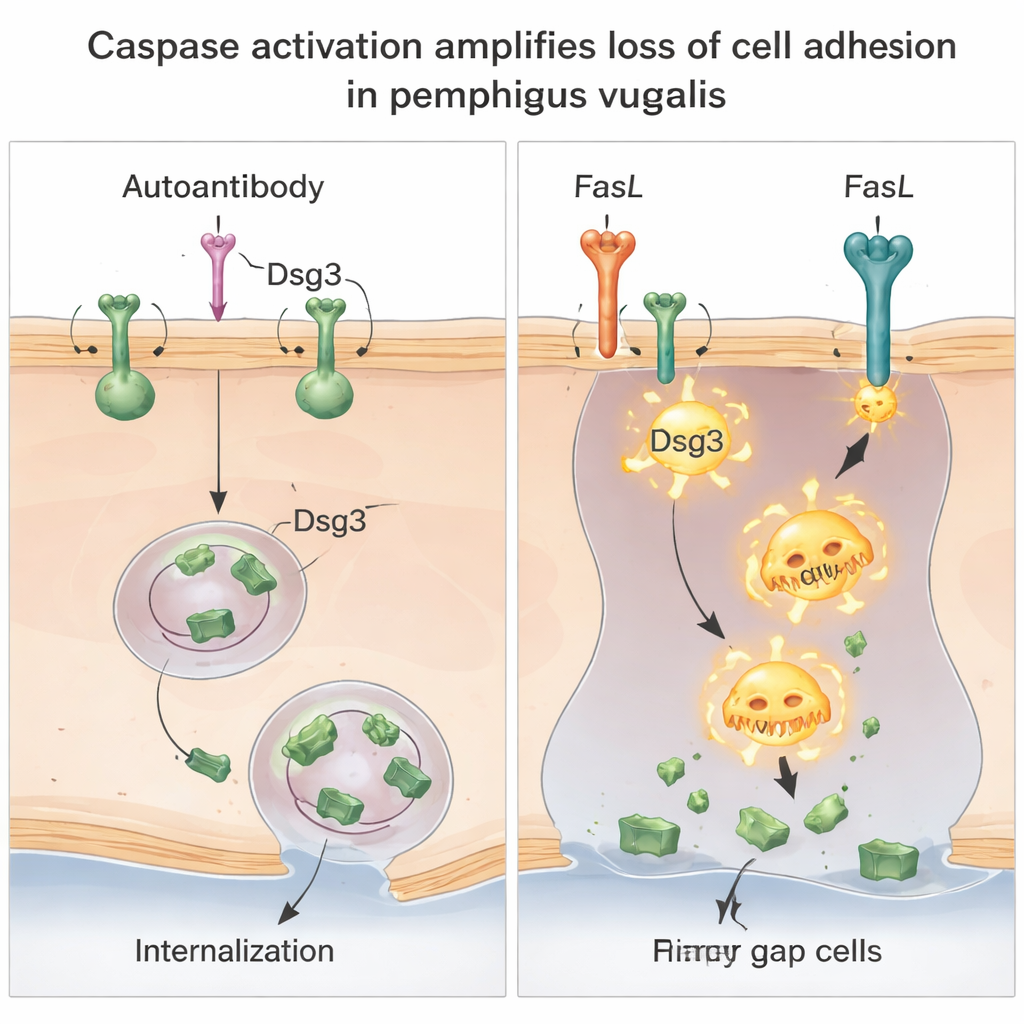
Twee manieren om hetzelfde verband te verbreken
Dieper gravend toonden de wetenschappers aan dat er eigenlijk twee verschillende maar samenwerkende manieren zijn waarop Dsg3 verloren gaat. Ten eerste bevordert het antilichaam de internalisatie van intacte Dsg3–antilichaamcomplexen van het celoppervlak in gespecialiseerde membraancompartimenten, waardoor de hoeveelheid Dsg3 bij celverbindingen afneemt. Deze stap was niet afhankelijk van caspases en werd niet gestopt door het blokkeren van gangbare routes voor eiwitafbraak, wat wijst op een specifieke herschikking van Dsg3 binnen de cel. Ten tweede, wanneer FasL aanwezig is, wordt caspase-8 actief en knipt het Dsg3 in kleinere fragmenten, vooral in de losser gebonden delen van het membraan. Deze caspase-gedreven knipping vermindert verder de hoeveelheid volledige, functionele Dsg3 en vergroot het verlies van adhesie dat door de antilichamen wordt veroorzaakt.
Wat dit betekent voor patiënten en toekomstige behandelingen
Samen genomen suggereren de resultaten dat bij pemphigus vulgaris antilichamen tegen Dsg3 het blaarproces op gang brengen door Dsg3 van het celoppervlak te strippen, terwijl FasL-gedreven caspase-activatie fungeert als een versterker die de schade veel erger maakt door het resterende Dsg3 te splijten. Belangrijk is dat veel van dit gebeurt voordat de huidcellen daadwerkelijk sterven. Voor patiënten betekent dit dat effectieve therapieën niet alleen schadelijke antilichamen moeten verminderen, maar mogelijk ook FasL of caspases moeten blokkeren om te voorkomen dat blaren ontstaan of zich verspreiden. Dit dubbele mechanisme kan helpen verklaren waarom de ziekte zo verschillend kan lijken en zich zo verschillend kan gedragen tussen personen — of tussen verschillende lichaamsplaatsen — en wijst op nieuwe, meer precieze manieren om de natuurlijke huidlijm intact te houden.
Bronvermelding: Schmidt, M.F., Feoktistova, M.A., Panayotova-Dimitrova, D. et al. Caspase-activation powers anti-Desmoglein 3-induced acantholysis in human epidermis. Cell Death Discov. 12, 102 (2026). https://doi.org/10.1038/s41420-026-02963-w
Trefwoorden: pemphigus vulgaris, auto-immuun blaarziekte, desmogleïne 3, caspase-8, Fas-ligand