Clear Sky Science · nl
Vergelijkende fenotypische en moleculaire profilering van replicatieve en chemisch-geïnduceerde veroudering in gewrichtskraakbeencellen
Waarom versleten gewrichtscellen ertoe doen
Pijnlijke, stijve gewrichten zijn een veelvoorkomend onderdeel van ouder worden, maar wetenschappers ontdekken dat een bepaald type “versleten” cel mogelijk een belangrijke aanjager is van artrose—de meest voorkomende gewrichtsaandoening wereldwijd. Deze cellen, senescente cellen genoemd, stoppen met delen en beginnen een mengsel van irriterende moleculen uit te scheiden dat nabijgelegen weefsel kan beschadigen. Deze studie stelt een bedrieglijk eenvoudige maar cruciale vraag: wanneer onderzoekers kraakcellen in het laboratorium kweken om artrose te bestuderen, welke methoden om die cellen “oud” te maken lijken eigenlijk op wat er in echte gewrichten gebeurt?
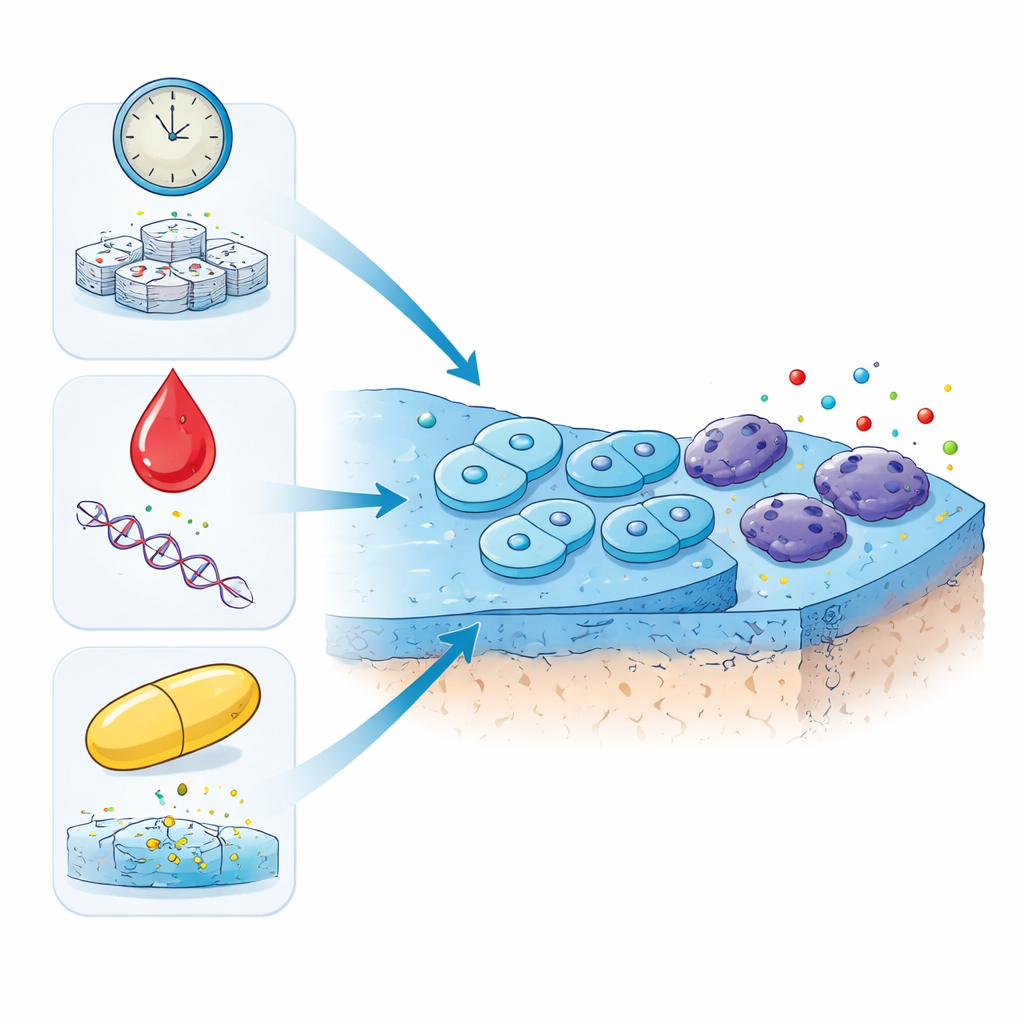
Drie verschillende wegen naar vermoeide cellen
De onderzoekers richtten zich op chondrocyten, de cellen die het gladde kraakbeenlaagje aan de uiteinden van botten onderhouden. Met cellen uit schapengewrichten duwden ze de cellen in senescentie op drie verschillende manieren. In de ene benadering lieten ze de cellen gewoon vele generaties blijven delen totdat ze een oud, versleten stadium bereikten, wat het verouderingsproces in de tijd nabootst. In de andere twee benaderingen blootstelden ze jonge cellen aan lage doses van twee in de geneeskunde gebruikte medicijnen: doxorubicine, een chemotherapiemiddel dat DNA beschadigt, en dexamethason, een sterk ontstekingsremmend steroid dat in pijnlijke gewrichten wordt geïnjecteerd. Alle drie de behandelingen werden afgesteld zodat de cellen lang genoeg overleefden om een stabiele, leeftijdsachtige staat te ontwikkelen.
Gemeenschappelijke tekenen van cellulaire ouderdom
Bij alle drie de methoden vertoonden de chondrocyten klassieke kenmerken van senescentie. Ze stopten met vermenigvuldigen, toonden veranderingen in hun celcyclus en ontwikkelden een hogere activiteit van een kenmerkend enzym dat vaak wordt gebruikt om senescente cellen op te sporen. De cellen veranderden ook hun interne structuur, met grotere, plattere vormen en veranderingen in de manier waarop hun DNA is verpakt. Diep vanbinnen werkten hun mitochondriën—de kleine energiecentrales die cellulaire brandstof maken—niet meer efficiënt. Met krachtige genetische en eiwitanalyses vond het team dat sleutelwegen voor energieproductie en systemen voor het opbouwen van nieuwe eiwitten in elk model naar beneden waren bijgesteld. Samen schetsen deze veranderingen een consistent beeld van kraakcellen die het werk hebben verlaten en vastzitten in een metabool trage maar aanhoudende staat.
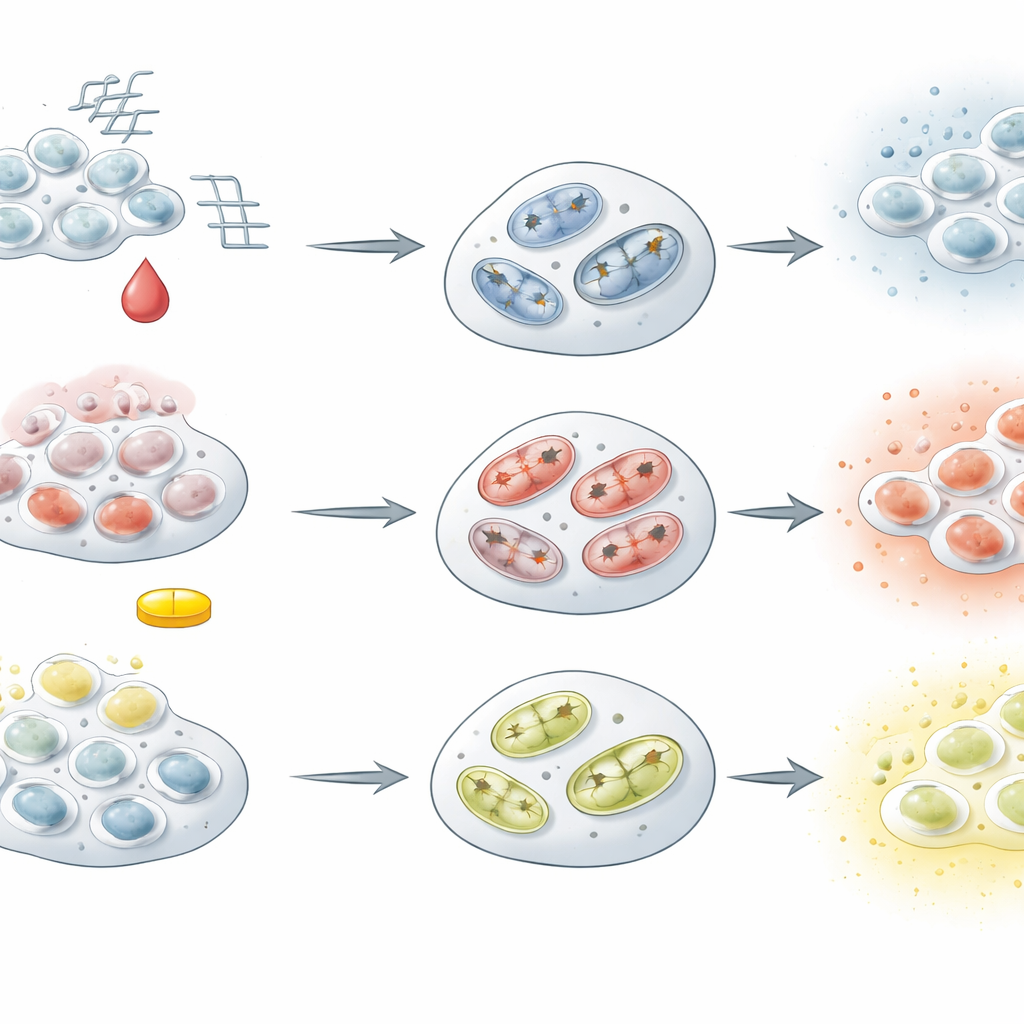
Zelfde bestemming, verschillende routes
Ondanks deze gedeelde kenmerken waren de drie modellen allesbehalve identiek. Cellen die waren verouderd door vele delingsrondes vertoonden verkorte uiteinden van chromosomen, bouwden schadelijke zuurstofbijproducten op, verloren energie en scheidden meer structurele kraakbeeneiwitten uit in hun omgeving—kenmerken die lijken op langzaam, leeftijdsgerelateerd kraakbeenslijtage. Daarentegen reageerden cellen die met doxorubicine waren gestrest met een sterke DNA-schaderespons, activeerden ze machinerie voor celdood en produceerden ze hoge niveaus van ontstekingssignalen, wat wijst op een hardere, meer letselachtige situatie. Dexamethason-behandelde cellen werden ook senescent, maar zonder dezelfde piek in schadelijke zuurstofmoleculen of apoptose. In plaats daarvan behielden of verhoogden ze hun energieopbrengst en produceerden ze een sterke mix van uitgescheiden factoren die samenhangen met ontsteking en weefselhermodellering, wat de complexe, dubbelzinnige effecten van steroidale medicijnen op anders gezond kraakbeen weerspiegelt.
Signalen die het gewricht bereikt
De stoffen die deze senescente cellen uitstootten—gezamenlijk bekend als het senescentie-geassocieerde secretorische fenotype—verschilden sterk tussen de modellen. De lang gedeelde cellen scheidden minder klassieke ontstekings- en stressgerelateerde eiwitten uit, maar werden rijker aan componenten van de kraakbeenmatrix. Daarentegen pompten beide medicijnbehandelde groepen, vooral de cellen blootgesteld aan steroid, veel moleculen uit die immuuncellen kunnen aantrekken, ontsteking kunnen bevorderen en het omliggende weefsel kunnen herschikken. Deze verschillende “secretiefingerafdrukken” zijn belangrijk omdat ze in een levend gewricht ofwel decennialang het kraakbeen geruisloos kunnen verzwakken of agressiever, opvlammingsachtig letsel kunnen veroorzaken na letsel, chemotherapie of herhaalde steroidinjecties.
Wat dit betekent voor het begrijpen en behandelen van gewrichtsaandoeningen
Voor niet-specialisten is de belangrijkste boodschap dat niet alle verouderde kraakcellen gelijk zijn. De studie toont aan dat hoewel verschillende laboratoriummethoden kraakcellen in een oude, senescente staat kunnen duwen, ze dat doen via verschillende soorten stress met verschillende consequenties. Cellen verouderd door de loop van de tijd en herhaalde deling lijken het meest op die gezien bij natuurlijke veroudering en langdurige artrose. Cellen die gestrest zijn door chemotherapie of steroïden modelleren beter situaties waarin medicijnen of acuut letsel de gewrichtsachteruitgang versnellen. Door het laboratoriummodel zorgvuldig af te stemmen op het scenario uit de echte wereld, kunnen onderzoekers geneesmiddelen die senescente cellen verwijderen of hun schadelijke uitscheiding verminderen beter testen. Het werk benadrukt ook falende mitochondriën en verstoorde energiebalans als een centrale zwakte die alle senescente kraakcellen gemeen hebben—een aantrekkelijk doelwit voor toekomstige therapieën die onze gewrichten langer gezonder moeten houden.
Bronvermelding: Arteaga, M.B., Tarasova, K., Kidtiwong, A. et al. Comparative phenotypic and molecular profiling of replicative and chemically-induced senescence in articular chondrocytes. Cell Death Discov. 12, 106 (2026). https://doi.org/10.1038/s41420-026-02961-y
Trefwoorden: artrose, cellulaire veroudering, chondrocyten, mitochondriale disfunctie, kraakbeenslijtage