Clear Sky Science · nl
PDHA1 verhoogt de weerstand tegen ferroptose bij anoikis-resistente prostaatkanker door AIFM2 op te drijven
Waarom sommige prostaatkankercellen weigeren te sterven
Wanneer kankercellen zich losmaken van een tumor en in de bloedbaan terechtkomen, zouden de meeste moeten sterven voordat ze een nieuw orgaan bereiken. Toch overleeft een gevaarlijke minderheid, reist ze mee en zaait ze metastasen die vaak dodelijk zijn. Deze studie stelt een centrale vraag: wat stelt bepaalde prostaatkankercellen in staat om weerstand te bieden tegen een vorm van celdood die normaal optreedt zodra ze het contact met hun weefsel verliezen? Door een verborgen overlevingscircuit in deze cellen bloot te leggen, wijst het onderzoek op nieuwe manieren om metastase bij de bron te blokkeren.
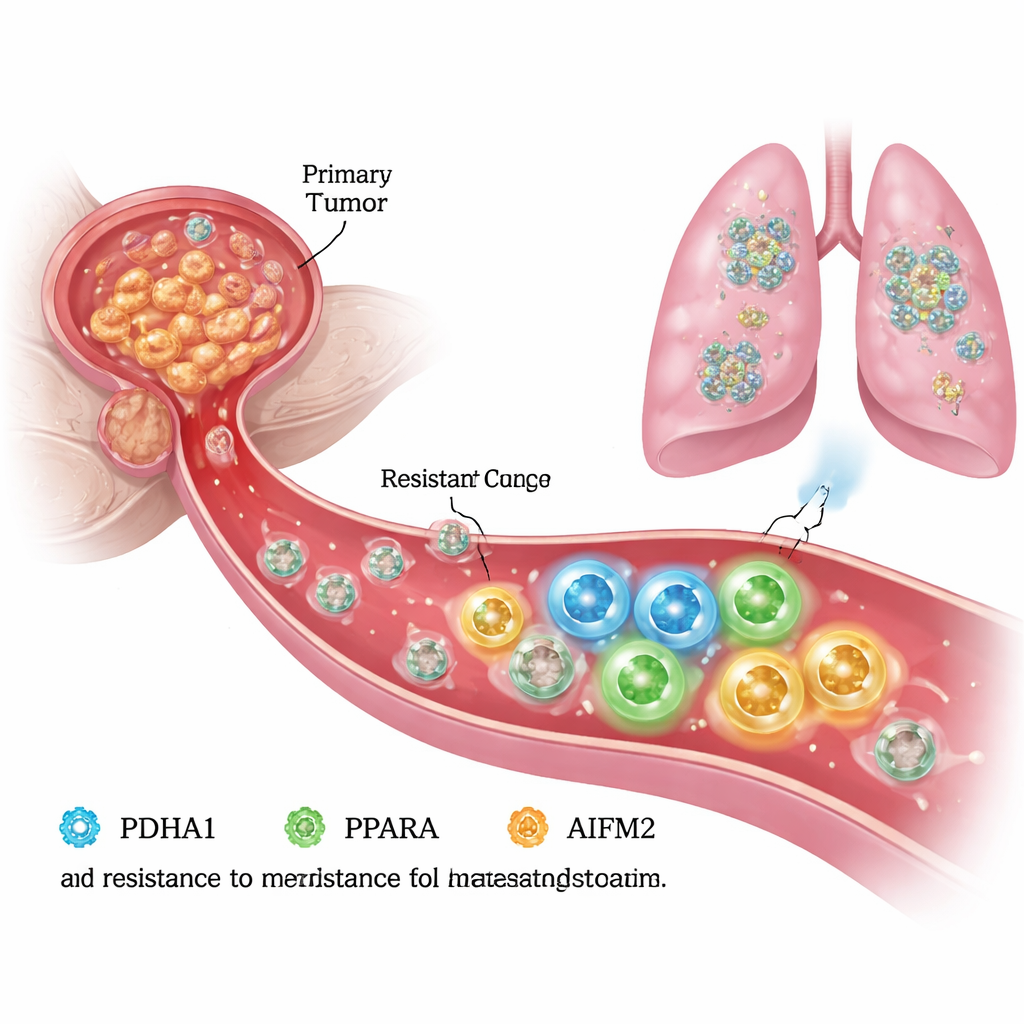
Ontsnappen aan de dood in de bloedbaan
Om zich te verspreiden moeten prostaatkankercellen het zonder de ondersteuning van het omringende weefsel, het extracellulaire matrix, uithouden. Onder deze “losgemaakte” omstandigheden ondergaan gezonde cellen een geprogrammeerde celdood die anoikis heet, en veel kankercellen zijn ook kwetsbaar voor een verwant, ijzerafhankelijk doodsproces dat ferroptose wordt genoemd. De auteurs maakten in het laboratorium anoikis-resistente prostaatkankercellen en vergeleken die met hun oorspronkelijke “ouderlijke” cellen. Ze ontdekten dat de resistente cellen niet alleen agressiever migreerden en invadeerden, maar ook beter overleefden onder detachering, wat suggereert dat ze hun interne machines hadden herbedraad om ferroptose te vermijden en te blijven groeien.
Een metabole schakelaar met een tweede taak
Nog dieper graven richtte het team zich op een metabool enzym genaamd PDHA1, vooral bekend om zijn rol bij het omzetten van pyruvaat uit suiker naar acetyl-CoA in de mitochondriën en zo de energieproductie te voeden. In de anoikis-resistente cellen waren PDHA1-niveaus en -activiteit duidelijk hoger, en patiëntmonsters lieten meer PDHA1 zien in primaire tumoren van mannen wiens prostaatkanker was uitgezaaid naar lymfeklieren of verre locaties. Toen de onderzoekers PDHA1 verminderden, verloren resistente cellen veel van hun vermogen om te bewegen, te infiltreren en te overleven. Verrassend genoeg was een aanzienlijk deel van PDHA1 in deze cellen niet langer beperkt tot de mitochondriën; het was naar de celkern verplaatst, waar DNA is verpakt met histonen die chemisch kunnen worden aangepast om genen aan of uit te zetten.
Herschrijven van genactiviteit om ferroptose te blokkeren
In de kern leek PDHA1 de lokale productie van acetyl-CoA te voeden, een sleutelbouwsteen voor histonacetylatie. De auteurs toonden aan dat kern-PDHA1 een specifieke markering, H3K9-acetylatie, verhoogde in het regelgebied van een gen dat PPARA heet. Deze verandering werkte als het losser maken van de chromatine "spoelen", waardoor het gemakkelijker werd om PPARA aan te zetten. PPARA fungeerde op zijn beurt als een hoofdschakelaar die de productie van een ander eiwit, AIFM2, verhoogde door aan zijn promotor te binden en de transcriptie te verhogen. In plaats van AIFM2 direct aan te passen werkte PDHA1 dus via PPARA, en legde een meerstapsroute bloot van veranderde stofwisseling naar veranderde genregulatie.
Een schild opbouwen tegen ijzergedreven schade
AIFM2 staat bekend als een intern remmiddel tegen ferroptose: het helpt vetten in celmembranen te beschermen tegen destructieve oxidatie. In de resistente prostaatkankercellen leidde opdrijven van PDHA1 tot hogere AIFM2-niveaus, terwijl het verminderen van PDHA1 deze niveaus verlaagde. Functionele tests toonden aan dat het terugbrengen van PDHA1 de kenmerken van ferroptose versterkte—meer reactieve zuurstofsoorten, meer lipidentergang, een lagere mitochondriale membraanpotentiaal en karakteristieke inkrimping van mitochondriën—vooral wanneer cellen werden blootgesteld aan het ferroptose-inducerende middel erastine. Overexpressie van AIFM2 keerde deze effecten om, redde celoverleving in kweek en herstelde longmetastasen in muismodellen, zelfs wanneer PDHA1 was onderdrukt. Dit bevestigde dat AIFM2 een cruciale downstream-effector is van PDHA1-gedreven ferroptose-resistentie.
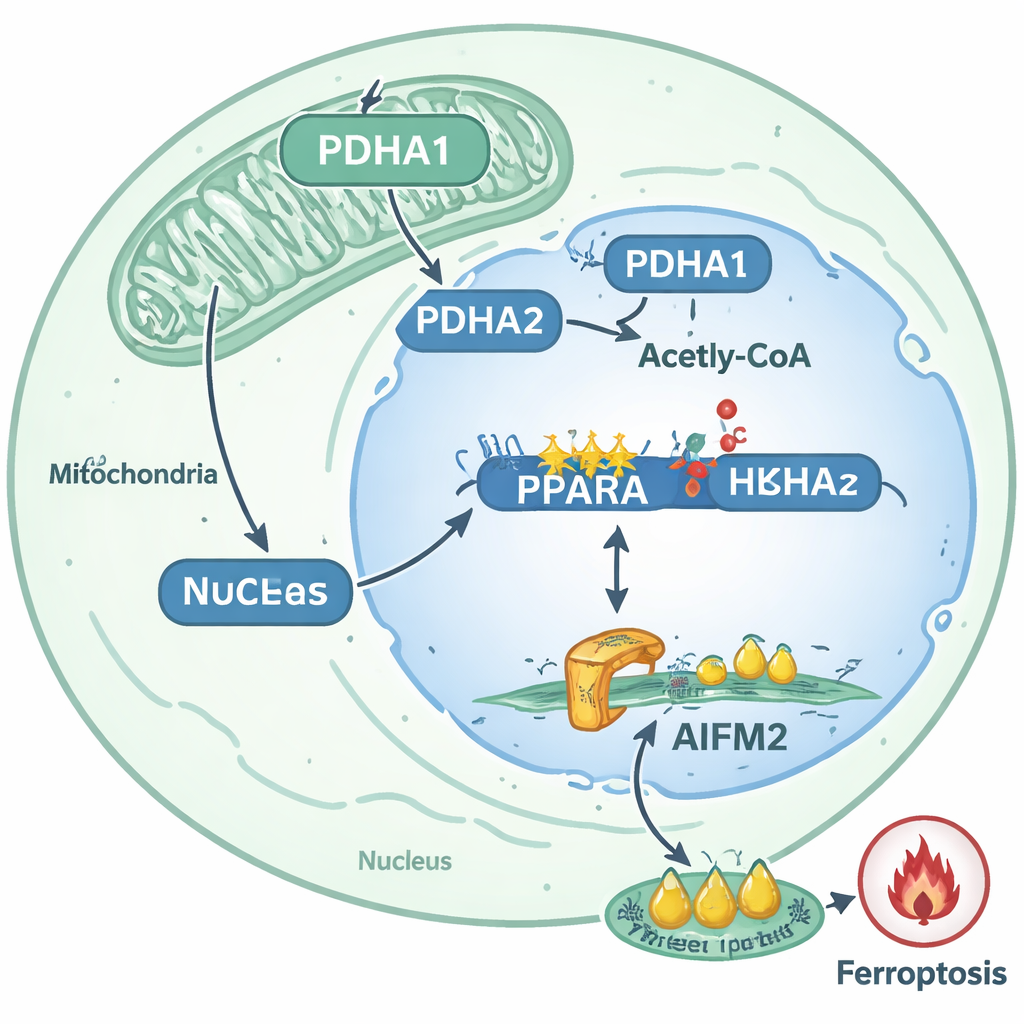
Van moleculair circuit naar behandelideeën
Door deze gebeurtenissen in kaart te brengen schetst de studie een duidelijk pad waardoor losgemaakte prostaatkankercellen moeilijker te doden worden: PDHA1 verhuist naar de kern, verhoogt histonacetylatie bij het PPARA-gen, stimuleert PPARA-activiteit en verhoogt daardoor AIFM2-niveaus om ferroptose te blokkeren. Deze route hangt sterk samen met metastatisch gedrag in patiënttumoren en in diermodellen. Voor niet-specialisten is de conclusie dat bepaalde kankercellen een standaard metabool enzym herbestemmen tot een epigenetisch instrument dat genactiviteit herschrijft en een biochemisch schild opbouwt tegen een krachtige vorm van celdood. De auteurs suggereren dat geneesmiddelen die PDHA1, PPARA of AIFM2 targeten—of therapieën die opzettelijk ferroptose opwekken—op een dag gecombineerd zouden kunnen worden om metastatische prostaatkankercellen dit overlevingsvoordeel te ontnemen en ze veel kwetsbaarder te maken tijdens hun meest risicovolle reis: de sprong van het ene orgaan naar het andere.
Bronvermelding: Cong, Y., Chen, K., Ju, Y. et al. PDHA1 enhances resistance to ferroptosis in anoikis-resistant prostate cancer by upregulating AIFM2. Cell Death Discov. 12, 105 (2026). https://doi.org/10.1038/s41420-026-02958-7
Trefwoorden: uitzaaiing van prostaatkanker, ferroptose, anoikis-resistentie, PDHA1, AIFM2