Clear Sky Science · nl
Metabole signaturen moduleren om cabozantinib‑resistentie te verminderen in FLT3‑ITD acute myeloïde leukemie‑celmodellen
Waarom dit belangrijk is voor kankerbehandeling
Veel moderne kankergeneesmiddelen zijn ontworpen om zich te richten op één defect eiwit in tumorcellen. Deze gerichte middelen kunnen dramatische remissies veroorzaken, maar kankers vinden vaak manieren om zich aan te passen en terug te groeien. Dit artikel onderzoekt hoe een vorm van bloedkanker, acute myeloïde leukemie (AML), resistent wordt tegen een dergelijk gericht middel, cabozantinib, en hoe het herbedraden van het energiegebruik van kankercellen artsen zou kunnen helpen die resistentie te omzeilen.
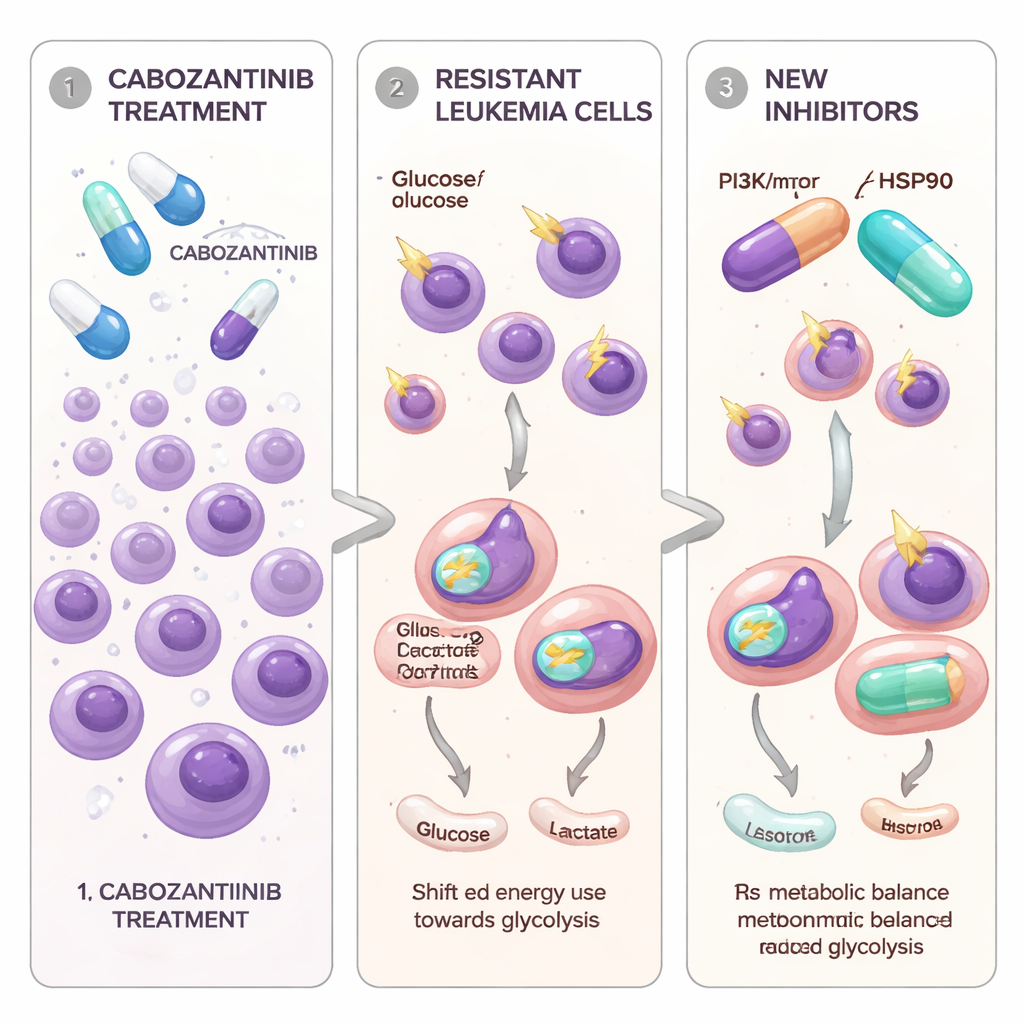
Leukemiecellen die leren een gericht geneesmiddel te ontwijken
De onderzoekers concentreerden zich op AML‑cellen die een mutatie dragen in een groeisignaal‑schakelaar genaamd FLT3‑ITD, waarvan bekend is dat die een bijzonder agressieve ziekte aandrijft. Cabozantinib, een pil die al wordt gebruikt voor verschillende solide tumoren, kan FLT3‑gedreven leukemiecellen in het laboratorium sterk remmen. Om te modelleren wat er bij patiënten in de loop van de tijd gebeurt, stelde het team twee FLT3‑gemuteerde AML‑cellijnen geleidelijk bloot aan oplopende doses cabozantinib totdat enkele cellen overleefden en weer begonnen te groeien. Deze nieuwe celpopulaties, Molm13‑XR en MV4‑11‑XR genoemd, konden cabozantinibconcentraties verdragen die veel hoger waren dan die van hun oorspronkelijke “ouder”cellen. Ze werden ook minder gevoelig voor twee andere goedgekeurde FLT3‑gerichte middelen, sorafenib en quizartinib, terwijl ze kwetsbaar bleven voor een andere remmer, gilteritinib.
Genetische aanpassingen die kanker helpen overleven
Bij nadere bestudering vonden de wetenschappers dat deze medicijnresistente leukemiecellen nieuwe veranderingen in hun FLT3‑gen droegen. Beide resistente lijnen hadden dezelfde puntmutatie verworven, D835Y genoemd, in een cruciale regio van FLT3’s kinase‑domein, een bekend hotspot voor resistentie tegen meerdere middelen. Één lijn, MV4‑11‑XR, had bovendien een ongebruikelijke deletie van 1,3 kilobase gekregen die een volledig exon van FLT3 verwijderde en een deel van het domein dat belangrijk is voor medicijnbinding uitveegde. Deze veranderingen lijken tijdens langdurige blootstelling aan cabozantinib geselecteerd te zijn: gemuteerde versies van FLT3 kwamen veel vaker voor in de resistente cellen dan in de beginnende populatie. Tegelijkertijd waren sleutelsignaleringstrajecten stroomafwaarts van FLT3 — zoals ERK, STAT5 en AKT — sterker geactiveerd, wat snellere groei en grotere kolonieformatie in de resistente cellen ondersteunde.
Kankercellen schakelen van brandstofsysteem
Het team vroeg zich vervolgens af of resistentie niet alleen aan genetica was gekoppeld, maar ook aan hoe de cellen zichzelf van brandstof voorzien. Met behulp van RNA‑sequencing en specifieke metabolische tests vonden ze een consistent patroon: cabozantinib‑resistente cellen vertrouwden veel sterker op glycolyse — de snelle afbraak van glucose in het celplasma — zelfs wanneer zuurstof volop aanwezig was. Deze cellen namen meer glucose op, produceerden meer lactaat, toonden een hogere activiteit van een sleutelenzym genaamd GAPDH en verhoogden de expressie van meerdere glycolyse‑gerelateerde genen. Daarentegen waren de mitochondriën — de structuren die efficiëntere energieproductie ondersteunen — minder actief en minder talrijk. Metingen van zuurstofverbruik lieten zien dat zowel basale als piek‑mitochondriale respiratie waren verminderd, en reactieve zuurstofsoorten binnen de cellen waren verhoogd, wat wijst op gestreste, onderpresterende mitochondriën.
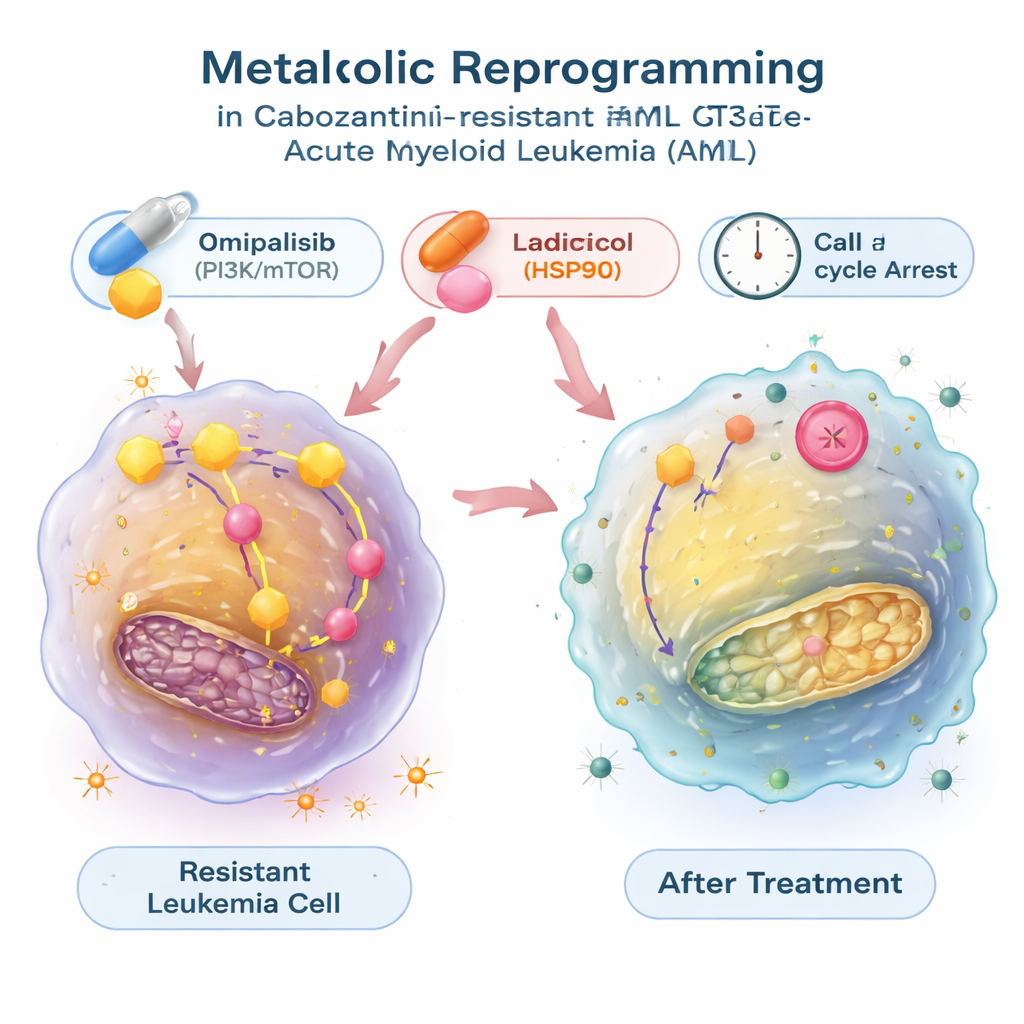
Geneesmiddelen vinden die de metabole schakel terugzetten
Om te onderzoeken of deze energiewijziging omkeerbaar was, gebruikten de onderzoekers een grote openbare database die gen‑expressiepatronen koppelt aan de effecten van duizenden verbindingen. Ze zochten naar middelen die naar verwachting het metabole signatuur van de resistente leukemiecellen zouden tegengaan en kwamen uit op twee middelen: radicicol, dat een eiwitchaperonne genaamd HSP90 blokkeert, en omipalisib, dat het PI3K/mTOR‑signaleringspad remt dat groei en metabolisme reguleert. In labtesten vertraagden beide moleculen niet alleen de groei van resistente cellen, maar verminderden ze ook de overactieve glycolyse, normaliseerden ze glucoseopname en lactaatafgifte en dempten ze de expressie van glycolyse‑gerelateerde genen. Deze verbindingen duwden leukemiecellen in een rustfase van de celcyclus, en in het geval van radicicol veroorzaakten ze ook aanzienlijke geprogrammeerde celdood. Gecombineerd met cabozantinib werkten omipalisib — en in één model ook radicicol — synergistisch, waardoor de medicijnresistente cellen gemakkelijker te doden waren.
Wat dit betekent voor toekomstige leukemiebehandelingen
Voor niet‑specialisten is de boodschap dat leukemiecellen een gericht geneesmiddel kunnen ontlopen niet alleen door het directe doelwit te muteren, maar ook door te veranderen hoe ze energie maken en gebruiken. De studie toont aan dat cabozantinib‑resistente AML‑cellen een “suikerverbrandings”strategie aannemen terwijl hun mitochondriën verwaarloosd raken. Door de paden aan te tikken die deze herbedrade stofwisseling ondersteunen — met middelen zoals omipalisib of HSP90‑remmers — kan het mogelijk zijn de gevoeligheid voor cabozantinib en vergelijkbare behandelingen te herstellen. Hoewel deze bevindingen uit celmodellen en niet uit patiënten komen, suggereren ze dat het combineren van gerichte kankergeneesmiddelen met metabolisme‑modulerende middelen een veelbelovende manier kan zijn om resistentie bij FLT3‑gemuteerde AML uit te stellen of te overwinnen.
Bronvermelding: Fu, YH., Ng, K.M., Tseng, CY. et al. Modulating metabolic signatures to mitigate cabozantinib resistance in FLT3-ITD acute myeloid leukemia cell models. Cell Death Discov. 12, 98 (2026). https://doi.org/10.1038/s41420-026-02957-8
Trefwoorden: acute myeloïde leukemie, medicatie‑resistentie, FLT3‑mutatie, kankermetabolisme, cabozantinib