Clear Sky Science · nl
DNA-polymerase kappa gestabiliseerd door Ptbp2 interageert met MRE11 en bevordert genomische instabiliteit bij leukemie
Hoe leukemiecellen gebroken DNA behouden en toch overleven
Ons DNA wordt voortdurend aangevallen, maar gezonde cellen zijn doorgaans zeer goed in het opsporen en herstellen van schade. Bij leukemie leren sommige cellen echter leven met gebroken, instabiel DNA — en zetten die instabiliteit soms zelfs om in een overlevingsvoordeel. Deze studie onthult een moleculair "team-up" tussen een splicing-eiwit (Ptbp2), een speciale DNA-kopieerenzym (DNA-polymerase kappa, of Polk) en een schadeherkennende factor (MRE11) die leukemiecellen helpt net genoeg schade te repareren om te overleven, terwijl ze tegelijkertijd de genetische chaos ophopen die kankervorderingen aandrijft.
Een verborgen helper in leukemiecellen
De onderzoekers concentreerden zich op chronische myeloïde leukemie (CML), een bloedkanker die vaak wordt aangedreven door het BCR::ABL1-fusiegen. Hoewel moderne geneesmiddelen die BCR::ABL1 blokkeren in de vroege ziekte goed werken, reageren veel patiënten in de agressieve "blast crisis"-fase slecht. Eerder werk toonde aan dat Ptbp2, een eiwit dat aan RNA bindt en beïnvloedt hoe boodschappers worden verwerkt, door BCR::ABL1 wordt opgevoerd en als oncogen functioneert in CML. Hier ontdekte het team dat Ptbp2 zich vasthecht aan het uiteinde (3′ UTR) van het Polk-messenger RNA en het beschermt tegen afbraak. Daardoor produceren leukemiecellen meer Polk-eiwit wanneer Ptbp2 verhoogd is.
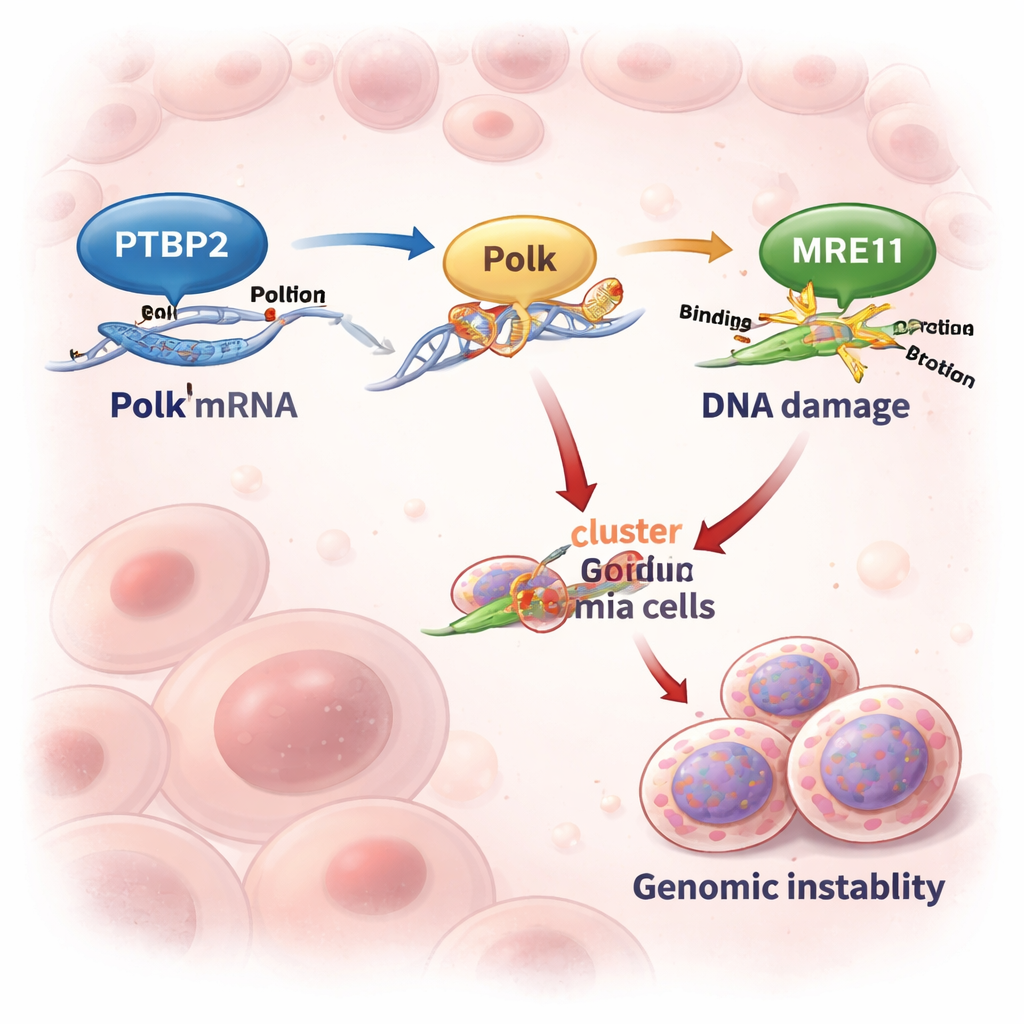
Een foutgevoelige DNA-kopieermachine inschakelen
Polk is een "backup" DNA-polymerase dat beschadigd DNA kan overbruggen wanneer de gebruikelijke replicatiemachinerie hapert. Deze eigenschap kan gestreste cellen redden — maar heeft een prijs, omdat Polk foutgevoelig is en mutaties kan introduceren. In cellijnen en patiëntmonsters uit gevorderde CML stegen en daalden Ptbp2- en Polk-niveaus gelijktijdig. Wanneer wetenschappers Ptbp2 in leukemiecellen uitschakelden, daalden Polk-niveaus scherp en degradeerde Polk-RNA bijna twee keer zo snel. Het herintroduceren van Polk in Ptbp2-deficiënte cellen herstelde hun gedrag, wat laat zien dat Ptbp2’s belangrijkste rol hier is om Polk overvloedig en actief te houden.
Schade repareren — maar niet perfect
Om te zien hoe dit duo DNA-reparatie beïnvloedt, behandelden de onderzoekers cellen met hydroxyureum, een middel dat DNA-replicatie doet stagneren en vaak bij CML-patiënten wordt gebruikt. Cellen zonder Ptbp2 liepen veel meer DNA-schade op, zichtbaar als lange "kometstaarten" en felle γH2AX-foci — kenmerkend voor gebroken chromosomen. Deze beschadigde cellen waren gevoeliger voor celdood. Daarentegen verdroegen cellen met hoge Ptbp2- en Polk-niveaus het middel beter, repareerden schade efficiënter en overleefden, hoewel hun reparatie slordig was. Overexpressie van Polk in Ptbp2-knockoutcellen herstelde deze gevoeligheid, wat bevestigt dat het Ptbp2–Polk-partnerschap leukemiecellen helpt replicatiestress te doorstaan en apoptose te vermijden.
Een DNA-schadenetwerk dat instabiliteit bevordert
Het verhaal eindigt niet bij Polk. Het team toonde aan dat Polk fysiek interacteert met MRE11, een sleutellid van het MRN-complex dat DNA-breuken detecteert en het ATM–CHK2 schade-responspad activeert. Wanneer Ptbp2 werd verwijderd, daalde Polk, namen MRE11-niveaus en -activiteit af en verzwakte de ATM–CHK2-signalisatie. Het terugplaatsen van Polk herstelde MRE11 en diens activatie. Gedetailleerde DNA-fiberexperimenten lieten zien dat Ptbp2 en Polk helpen verhinderen dat vastgelopen replicatievorken worden afgeknaagd, grotendeels via MRE11. Het blokkeren van MRE11 met een remmer ondermijnde deze vorkbescherming en vergrootte DNA-schade. Paradoxaal genoeg hoopten cellen met actief Ptbp2–Polk–MRE11-signaal meer chromosomale afwijkingen op, zoals zusterchromatide-uitwisselingen, breuken, spleten, multipolaire spilstructuren en multinucleëuze reuzencellen — klassieke tekenen van genomische instabiliteit die agressievere kanker kunnen aanwakkeren.
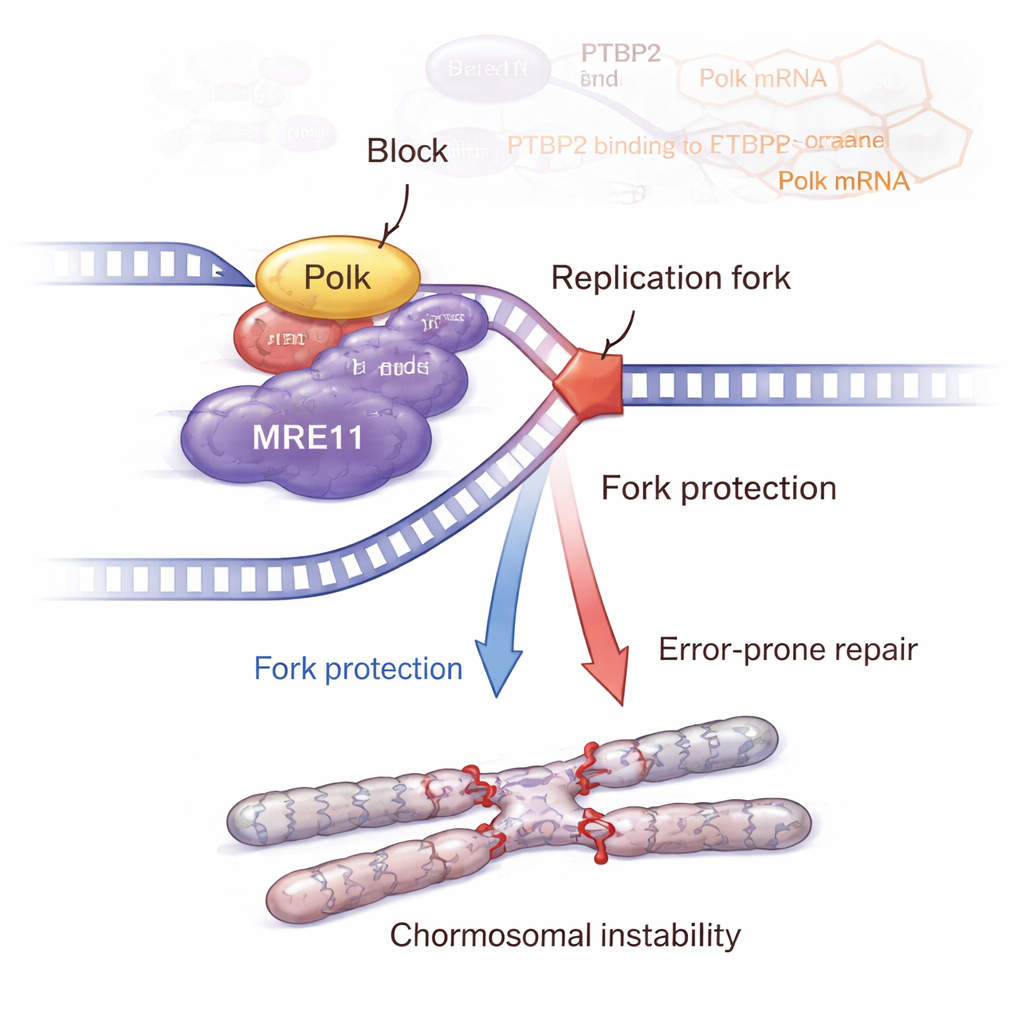
Van muizen naar mogelijke nieuwe therapieën
In muismodellen produceerden leukemiecellen met intact Ptbp2 grotere, meer abnormale tumoren dan cellen zonder Ptbp2. Weefsels van deze muizen toonden hogere niveaus van Ptbp2, Polk, de proliferatiemarker Ki-67 en verstoorde celdelingsstructuren. In een apart CML-achtig muismodel aangedreven door BCR::ABL1 leidde extra Ptbp2 tot verhoogde Polk-expressie en een grotere hoeveelheid atypisch delende cellen en invasieve leukemische clusters in milt en lever, wat wijst op versnelde ziekteprogressie. Samen suggereren deze bevindingen dat de Ptbp2–Polk–MRE11–ATM–CHK2-as leukemiecellen in staat stelt intense DNA-stress te doorstaan terwijl schadelijke mutaties zich geleidelijk ophopen.
Waarom dit belangrijk is voor patiënten
Voor leken is de kernboodschap dat sommige leukemiecellen aan de controle ontsnappen door een koorddanser te zijn: ze herstellen hun DNA net genoeg om te overleven, maar niet zo goed dat ze mutaties vermijden. Ptbp2 stabiliseert Polk, dat vervolgens samenwerkt met MRE11 om gestrest DNA te beschermen en schadensignalen gaande te houden — maar die reparatie is onvolmaakt en bevordert genetische chaos. Omdat gevorderde CML en andere kankers schijnbaar afhankelijk zijn van dit fragiele evenwicht, zou het gericht verstoren van Ptbp2 of diens controle over Polk cellen kunnen doen kantelen van overleving naar zelfvernietiging, wat een veelbelovende nieuwe strategie voor therapieën biedt, vooral in de moeilijk behandelbare blast crisis-fase.
Bronvermelding: Lama, S., Barik, B., IS, S. et al. DNA polymerase kappa stabilized by Ptbp2 interacts with MRE11 and promotes genomic instability in leukemia. Cell Death Discov. 12, 96 (2026). https://doi.org/10.1038/s41420-026-02951-0
Trefwoorden: chronische myeloïde leukemie, genomische instabiliteit, DNA-reparatie, DNA-polymerase kappa, PTBP2