Clear Sky Science · nl
Mitofagie bij alvleesklierkanker: mechanistische inzichten en implicaties voor nieuwe therapeutische strategieën
Waarom de energiecentrales van onze cellen ertoe doen bij alvleesklierkanker
Pancreasductaal adenocarcinoom is een van de dodelijkste vormen van kanker, deels omdat tumoren snel leren resistent te worden tegen vrijwel elke behandeling die artsen inzetten. Dit overzichtsartikel belicht een onverwachte speler in dat resistentie‑verhaal: mitofagie, het ingebouwde systeem van de cel om versleten mitochondriën — de kleine “energiecentrales” die energie produceren — te herkennen en te recyclen. Begrijpen hoe alvleesklierkanker dit opruimproces kaapt, kan nieuwe wegen openen naar effectievere en duurzamere therapieën.
Cellulaire schoonmaakploegen en de overlevingstrucs van kanker
Mitochondriën doen veel meer dan alleen energie produceren; ze helpen bij het regelen van metabolisme, celdood en de verwerking van schadelijke moleculen, de zogeheten reactieve zuurstofsoorten. Wanneer mitochondriën beschadigd zijn of in teveel aantal aanwezig zijn, gebruikt de cel mitofagie om ze te markeren en te verwijderen. Dat kan via twee hoofdroutes verlopen. De ene, bekend als de PINK1/Parkin‑route, vertrouwt op een schade‑sensor (PINK1) en een markeringsenzym (Parkin) om defecte mitochondriën aan te duiden voor afbraak. De andere maakt gebruik van receptorproteïnen zoals BNIP3, NIX en FUNDC1 op de mitochondriale oppervlakte om ze rechtstreeks te koppelen aan de afvalzakjes van de cel, de autophagosomen, zonder die markeringsstap. Deze routes werken vaak samen, waardoor cellen flexibele manieren hebben om hun mitochondriale voorraad aan te passen aan stressoren zoals zuurstoftekort of blootstelling aan geneesmiddelen. 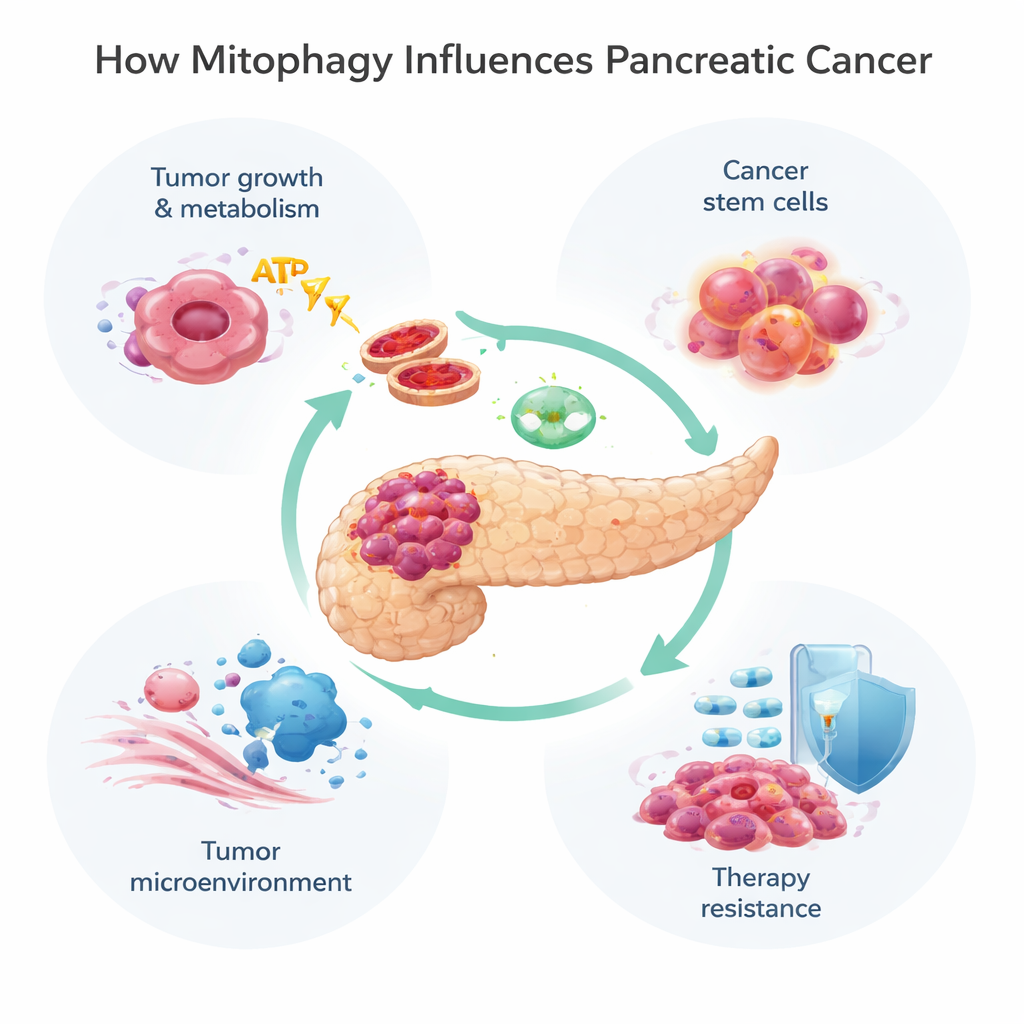
Hoe alvleeskliertumoren hun energiegebruik herschikken
Alvleeskliertumoren leven in een harde omgeving: ze worden slecht doorbloed en bevochtigd en zitten omsloten door dicht, littekenachtig weefsel. Om te overleven herprogrammeren kankercellen hun energiesystemen en schakelen vaak van zuurstofafhankelijke ademhaling in mitochondriën over naar een meer primitief suikerverbrandingsproces, glycolyse genoemd. Mitofagie helpt deze omschakeling fijn af te stemmen. In een vroeg stadium van tumorontwikkeling versnelt verlies van PINK1 of Parkin de kankervorming door ijzerstapeling, verhoogde reactieve zuurstofsoorten en een push richting glycolyse mogelijk te maken. Tegelijkertijd kan een ander mitofagie-eiwit, NIX, helpen nog functionele mitochondriën te verwijderen, waardoor cellen verder naar glycolytisch metabolisme en snellere groei worden geduwd. BNIP3 vertoont daarentegen een complexer patroon: het verschijnt vroeg, wordt later bij veel gevorderde tumoren stilgelegd, en wanneer het hersteld wordt kan het de kankercelgroei vertragen, wat suggereert dat sommige mitofagieroutes kanker remmen terwijl andere haar voeden.
Kanker‑stamcellen en de tumoromgeving
Niet alle kankercellen zijn gelijk. Een kleine subpopulatie, vaak aangeduid als kankerstamcellen, kan zichzelf vernieuwen, nieuwe tumoren zaaien en is bijzonder bestand tegen chemotherapie. Bij alvleesklierkanker vertrouwen deze cellen op mitofagie om metabolisch flexibel te blijven. Een modifier‑eiwit genaamd ISG15 ondersteunt dit proces en helpt hun stam‑achtige eigenschappen te behouden, waarmee mitofagie direct gekoppeld wordt aan terugval en behandelingsfalen. Buiten de kankercellen zelf vormgeeft mitofagie ook de tumor‑micro‑omgeving — de mix van ondersteunende cellen, immuuncellen en bindweefsel rond de tumor. Kanker‑geassocieerde fibroblasten kunnen bijvoorbeeld in een “reverse Warburg‑effect” terechtkomen, waarbij ze hun eigen mitofagie en glycolyse opvoeren en vervolgens de tumor voeden met energierijke bijproducten. Mitofagie beïnvloedt ook hoe immuuncellen kanker herkennen en aanvallen, door de presentatie van immuunvlaggen zoals MHC‑I en remmende signalen zoals PD‑L1 te wijzigen, die tumoren gebruiken om zich te verbergen.
Waarom het blokkeren of stimuleren van opruiming medicijnrespons kan veranderen
Veel standaard- en experimentele behandelingen voor alvleesklierkanker, waaronder chemotherapie met gemcitabine en nieuwe gerichte middelen tegen de veelvoorkomende KRAS‑G12D‑mutatie, beschadigen mitochondriën. Tumorcellen reageren vaak door mitofagie aan te zetten, de schade op te ruimen en aan de dood te ontsnappen. Studies tonen aan dat PINK1‑gedreven mitofagie de dodelijke effecten van chemotherapie en sommige natuurlijke verbindingen kan afzwakken, waardoor kankercellen overleven. Anderzijds kan het, onder bepaalde omstandigheden, te ver doorvoeren van mitofagie — vooral via BNIP3 en NIX — cellen van te veel functionele mitochondriën beroven, wat resulteert in een energiecrisis en celdood bevordert. Deze dualiteit betekent dat mitofagie tumoren ofwel kan beschermen tegen behandeling of, mits op de juiste manier aangestuurd, ze vatbaarder kan maken. 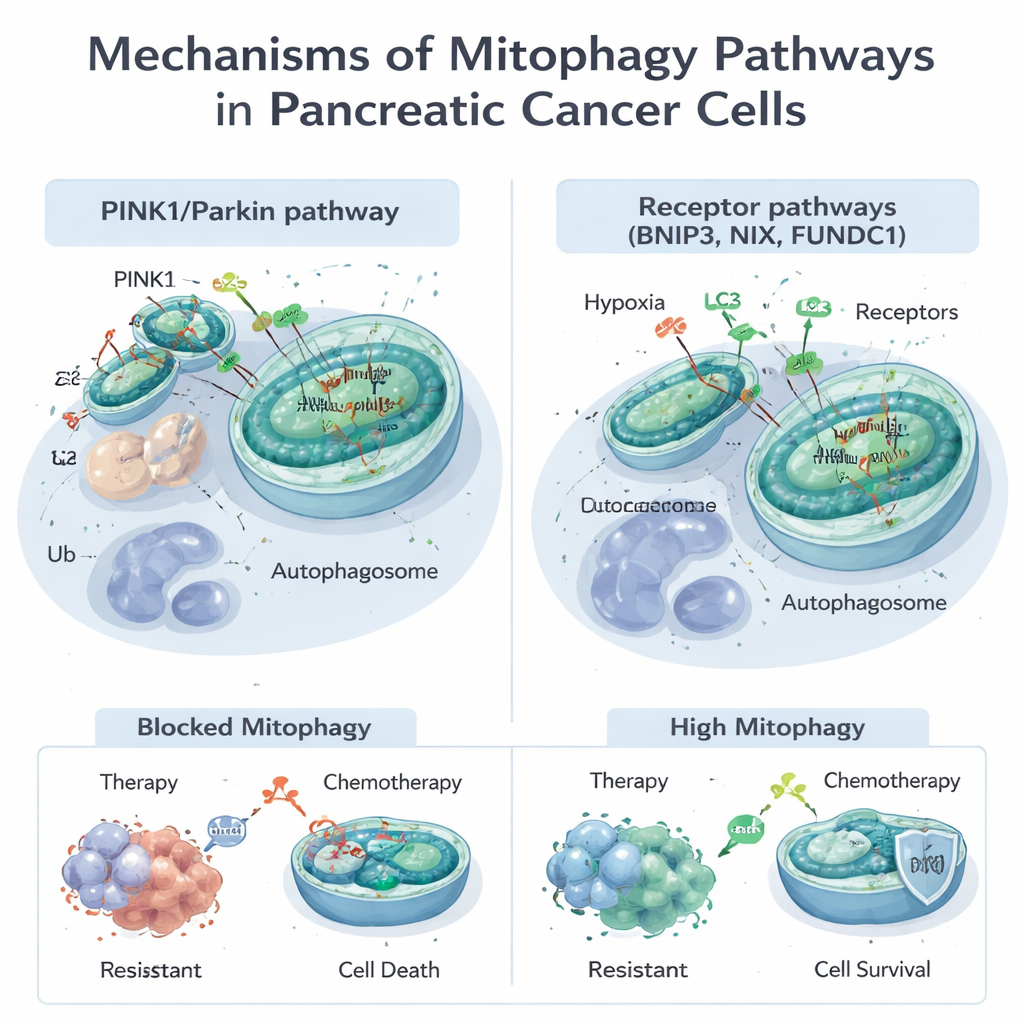
Nieuwe behandelideeën en de noodzaak van slimme patiëntselectie
Aangezien mitofagie op het kruispunt ligt van metabolisme, stressreacties en celdood, is het een aantrekkelijk doelwit voor combinatietherapieën. Huidige medicijnstrategieën werken meestal indirect: sommige verbindingen verstoren mitochondriale splijting en fusie; andere, zoals chloroquine en hydroxychloroquine, blokkeren de laatste fasen van het recycleproces door de fusie van afvalzakjes met zure afbraakcompartimenten uit te schakelen. Meerdere klinische onderzoeken testen deze middelen naast standaardchemotherapie bij alvleesklierkanker. De resultaten zijn tot nu toe wisselend — sommige patiënten profiteren, anderen niet. Een deel van het probleem is dat tumoren sterk verschillen in hun basale mitofagie‑ en metabole profielen: sommige zijn sterk afhankelijk van mitochondriale ademhaling, andere van glycolyse. De auteurs stellen dat toekomstig succes zal afhangen van betere biomarkers en genhandtekeningen om patiënten te clusteren op mitofagie‑activiteit en energiegebruik, en van de ontwikkeling van preciezere geneesmiddelen die specifieke mitofagiepaden selectief bijsturen in plaats van autophagie grofweg aan of uit te zetten. Voor niet‑specialisten is de kernboodschap dat het leren lezen en voorzichtig bijsturen van dit mitochondriale opruimsysteem kan helpen van alvleesklierkanker een beter beheersbare ziekte te maken.
Bronvermelding: Wang, Z., Lyu, Z., Palmen, R. et al. Mitophagy in pancreatic cancer: mechanistic insights and implications for novel therapeutic strategies. Cell Death Discov. 12, 93 (2026). https://doi.org/10.1038/s41420-026-02948-9
Trefwoorden: alvleesklierkanker, mitofagie, mitochondriën, chemotherapie‑resistentie, tumormetabolisme