Clear Sky Science · nl
Geactiveerde mesenchymale stamcellen verminderen schistosomiasis‑fibrose door omschakeling van macrofaagsubtypen en efferocytose te bevorderen via de Itgb2‑Rac1‑as
Het verminderen van levernarben door een veelvoorkomende parasiet
Schistosomiasis, een parasitaire ziekte die meer dan 200 miljoen mensen wereldwijd treft, laat vaak hardnekkige littekens in de lever achter, zelfs nadat de wormen zijn gedood. Deze littekens, bekend als fibrose, kunnen voortschrijden naar cirrose en levensbedreigende leverfalen. Deze studie onderzoekt een nieuwe celgebaseerde behandeling die de eigen immuuncellen van het lichaam leert beschadigd weefsel efficiënter op te ruimen, en biedt een nieuw perspectief op het omkeren van door parasieten veroorzaakte leverschade.
Waarom levernarben moeilijk genezen
Wanneer Schistosoma‑wormen eieren in de lever leggen, bouwt het immuunsysteem dichte celclusters — granulomen — rondom die eieren. Na verloop van tijd legt deze beschermende reactie te veel bindweefsel neer, waardoor de lever geleidelijk verstevigt. Een sleutelrol in dit proces is weggelegd voor macrofagen, het opruimteam van het lichaam. Eén subtype, aangeduid als ‘inflammatoire’ macrofagen, voedt de schade door het afgeven van agressieve signaalstoffen; een ander, meer ‘herstellend’ type helpt littekenweefsel af te breken en ontsteking te dempen. De centrale vraag in dit werk is of we macrofagen veilig kunnen aansporen van de schadelijke naar de helende toestand.
Stamcellen trainen om het immuunsysteem te sturen
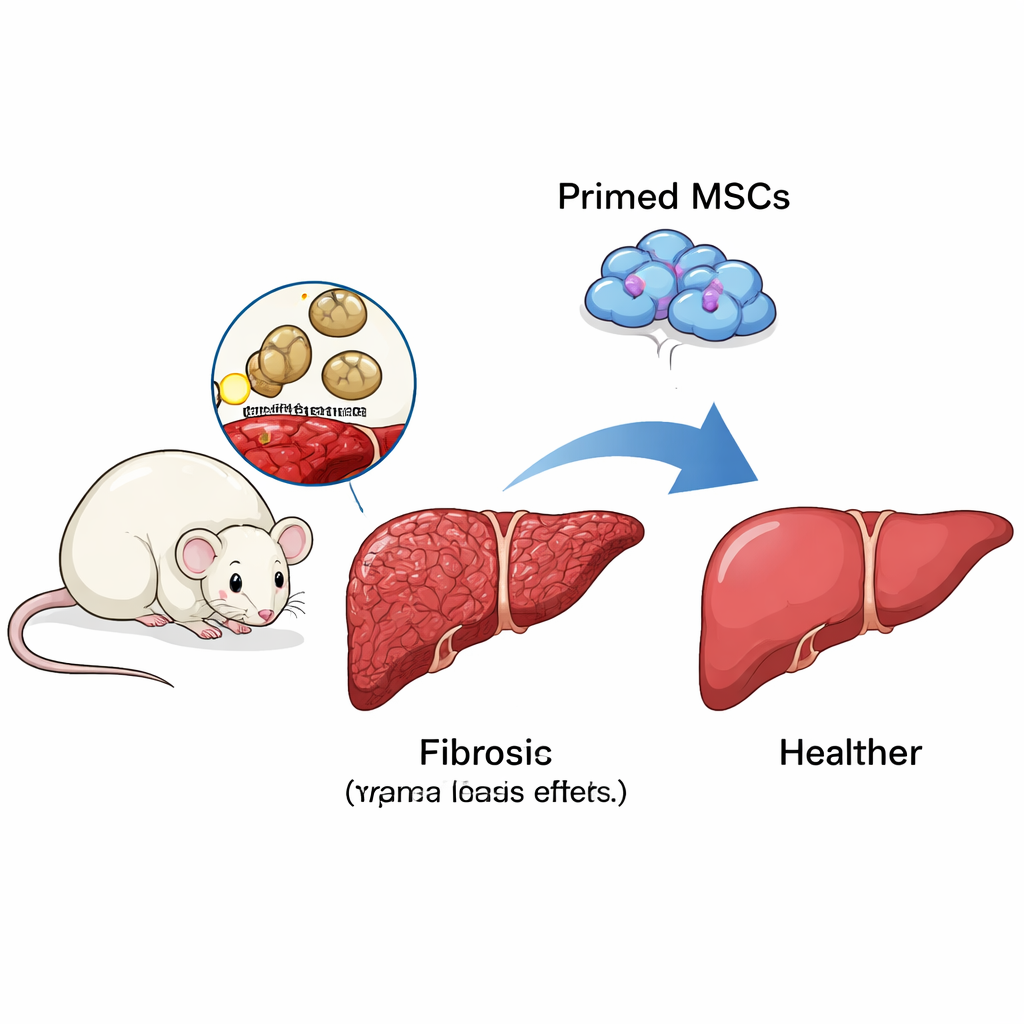
Mesenchymale stamcellen (MSC’s) — veelzijdige cellen die in beenmerg en andere weefsels voorkomen — trekken aandacht als mogelijke behandeling voor leverfibrose. Op zichzelf werken ze echter niet altijd goed. De onderzoekers ontdekten dat het ‘primen’ van MSC’s in het laboratorium met twee immuunsignalen, IFN‑γ en LPS, hun effectiviteit bij muizen geïnfecteerd met Schistosoma japonicum sterk verbeterde. Vergeleken met onbehandelde dieren of dieren die onvoorbereide MSC’s kregen, hadden muizen die geprimede MSC’s ontvingen levers die er gezonder uitzagen, namen meer in gewicht toe en toonden veel kleinere granulomen en minder collageenophoping onder de microscoop. Merkers van geactiveerde, littekenvormende cellen daalden eveneens, wat wijst op een daadwerkelijke afname van fibrose en niet alleen cosmetische veranderingen.
Het opruimteam van het lichaam herprogrammeren
Dieper gravend, maten de onderzoekers hoe geprimede MSC’s het gedrag van macrofagen beïnvloedden. In behandelde levers waren er minder inflammatoire macrofagen en meer van het pro‑resolving subtype dat beter is in het ontmantelen van littekenweefsel. Tegelijkertijd daalden de niveaus van klassieke ontstekingsmoleculen, terwijl nuttige, wondherstellende factoren binnen een gebalanceerd bereik bleven in plaats van extreem te stijgen. Toen de onderzoekers de instroom van nieuwe inflammatoire macrofagen naar de lever blokkeerden, daalden zowel het aantal herstellende cellen als de voordelen voor fibrose. Dit suggereerde dat geprimede MSC’s niet simpelweg nieuwe cellen toevoegen, maar binnenkomende inflammatoire macrofagen omzetten in een meer vredige, reparatiegerichte vorm.
Macrofagen helpen zover te eten naar herstel
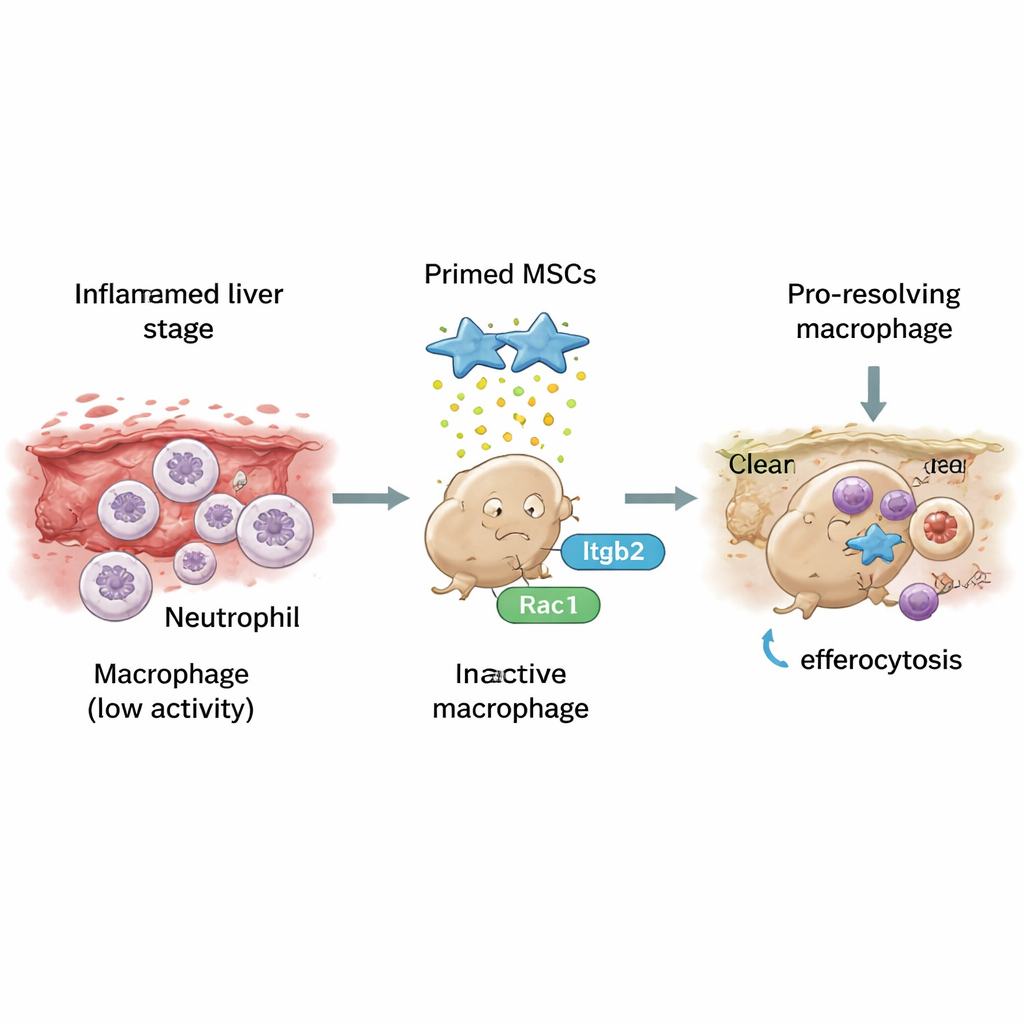
De studie richtte zich vervolgens op een proces dat efferocytose heet — het ordelijke ‘opeten’ van stervende cellen, met name uitgewerkte neutrofielen, een ander type immuuncel. Bij geïnfecteerde muizen die geprimede MSC’s kregen, werden levermacrofagen veel vaker aangetroffen met ingeslokte neutrofielen, een teken van actieve opruiming. In kweekvaten werden macrofagen die werden blootgesteld aan geprimede MSC’s beter in het inslikken van gelabelde apoptotische (stervende) neutrofielen en verschoof gelijktijdig hun genactiviteit naar een pro‑resolving profiel. De onderzoekers identificeerden een belangrijke moleculaire handgreep voor deze verandering: een receptor genaamd Itgb2 op macrofagen, die communiceert met een interne schakelaar, Rac1, die het cytoskelet en het inslikkenregime van de cel aanstuurt. Geprimede MSC’s verhoogden zowel Itgb2‑ als Rac1‑activiteit; het blokkeren van een van beide verminderde efferocytose scherp en keerde de verschuiving naar helende macrofagen om.
Wat dit kan betekenen voor toekomstige behandelingen
Simpel gezegd laat het werk zien dat speciaal geprimede stamcellen als ‘coaches’ voor immuuncellen na schistosomiasis kunnen fungeren, en hen aansporen om te stoppen met het aanwakkeren van ontsteking en in plaats daarvan afval en littekenweefsel efficiënter op te ruimen. Door de Itgb2–Rac1‑route te activeren, helpen deze geprimede MSC’s macrofagen soepel dode cellen af te voeren en vervolgens een littekenoplossende aard aan te nemen. Hoewel er nog veel moet gebeuren voordat deze aanpak bij mensen kan worden getest, biedt de studie een duidelijk mechanistisch stappenplan voor het ontwerpen van MSC‑gebaseerde therapieën die niet alleen schade onderdrukken, maar de lever ook actief helpen te herstellen na parasitaire infectie.
Bronvermelding: Lei, J., Ren, Y., Chen, Z. et al. Primed mesenchymal stem cells attenuate schistosomiasis fibrosis by enhancing macrophage subset switching and efferocytosis via Itgb2-Rac1 axis. Cell Death Discov. 12, 97 (2026). https://doi.org/10.1038/s41420-026-02947-w
Trefwoorden: schistosomiasis, leverfibrose, mesenchymale stamcellen, macrofagen, efferocytose