Clear Sky Science · nl
Dikke darmkanker-afgeleide osteopontine herprogrammeert macrofagen naar een pro-metastatische M2-toestand via de PI3K/AKT/CSF1-CSF1R-as
Waarom dit belangrijk is voor mensen met darmkanker
De meeste sterfgevallen door colorectale (dikke darm en endeldarm) kanker worden niet veroorzaakt door de oorspronkelijke tumor zelf, maar door uitzaaiingen naar andere organen. Deze studie onderzoekt hoe kankercellen "praten" met nabije immuuncellen om de verspreiding van tumoren te bevorderen. Door een sleutelboodschap te onthullen die kankercellen uitzenden om immuuncellen te herprogrammeren tot helpers in plaats van strijders, wijst het werk op nieuwe behandelingsstrategieën die de metastase bij gevorderde colorectale kanker mogelijk kunnen vertragen of stoppen.
Een kleverig eiwit met een donkere kant
De onderzoekers richtten zich op een eiwit dat osteopontine of OPN heet, dat zowel door kankercellen als door bepaalde immuuncellen in tumoren wordt geproduceerd. OPN wordt al langer in verband gebracht met slechtere uitkomsten bij veel kankersoorten, maar precies hoe het de verspreiding bij colorectale kanker bevordert, was onduidelijk. Door grote patiëntendatabases en tumorweefsels te analyseren, vonden de onderzoekers dat OPN-niveaus veel hoger waren in colorectale kankergezwellen dan in normaal darmweefsel, vooral bij patiënten met gevorderde ziekte en afstandsmetastasen. Patiënten met tumoren die meer OPN hadden, hadden over het algemeen een slechtere overleving, wat suggereert dat OPN nauwer verbonden is met agressieve, moeilijk te behandelen kanker.
Het zijn niet alleen de kankercellen zelf
Verrassend genoeg werden kankercellen uit colorectale tumoren in het laboratorium, die gedwongen werden meer of minder OPN te maken, niet op zichzelf veel invasiever of mobieler. Hun groei, migratie en vermogen om door kunstmatige membranen te dringen veranderden weinig. Dit tartte het gangbare idee dat OPN vooral werkt door de eigen kracht van kankercellen direct te versterken. In plaats daarvan keek het team naar de buurt van de tumor—de zogenoemde tumor-micro-omgeving—met name naar een groep immuuncellen die macrofagen worden genoemd en die óf tumoren aanvallen (een “M1”-toestand) óf hen ondersteunen (een “M2”-toestand).
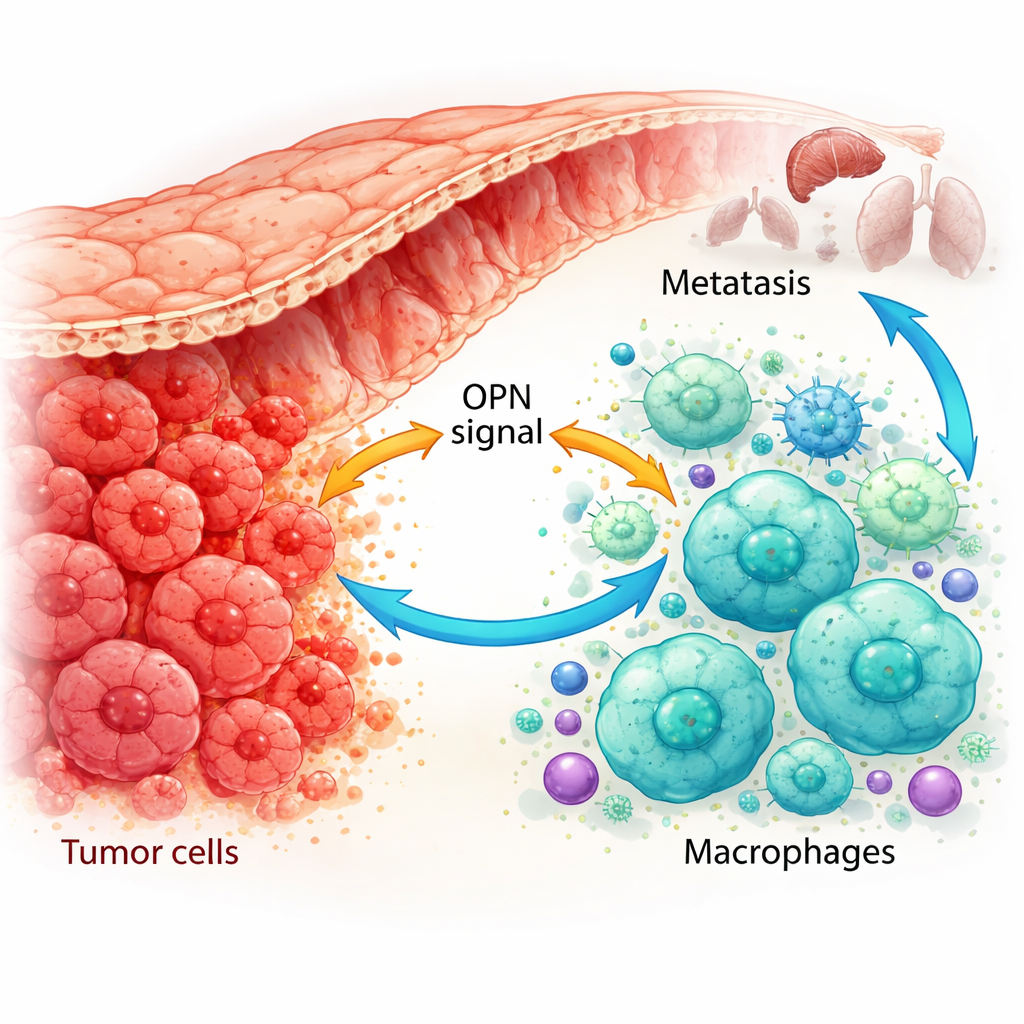
Hoe immuuncellen worden herbedraad tot tumorhulpjes
Met behulp van enkelcel-genetische kaarten en geavanceerde kleuring van patiëntweefsels toonden de onderzoekers aan dat OPN niet alleen door kankercellen wordt geproduceerd, maar ook door tumor-geassocieerde macrofagen. In tumoren die zich al hadden verspreid, waren zowel de kankercellen als een specifiek subtype van macrofagen rijk aan OPN. Deze macrofagen neigden naar de M2-achtige, tumorondersteunende toestand en kwamen meer voor wanneer de tumor OPN-niveaus hoog waren. In muismodellen trokken tumoren die zo werden aangepast dat ze meer OPN produceerden meer van deze M2-achtige macrofagen aan en groeiden ze sneller, terwijl tumoren met verlaagd OPN minder M2-macrofagen hadden en langzamer groeiden. Dit suggereert dat OPN een krachtige rekruteerder en herprogrammeerder van macrofagen in de tumoromgeving is.
De verborgen signaleringsketen: van OPN naar metastase
Om de moleculaire keten van gebeurtenissen te achterhalen, kweekte het team humane macrofagen samen met colorectale kankercellen die verschillende hoeveelheden OPN produceerden. Ze vonden dat kankercellen met hoge OPN hun macrofagen naar de M2-toestand duwden en een tweerichtingsbeweging aanmoedigden: macrofagen migreerden naar de tumor toe, en tumorcellen werden als reactie op signalen van deze macrofagen invasiever. Bij nadere bestudering ontdekten de wetenschappers dat OPN een signaalweg in macrofagen activeert die PI3K/AKT wordt genoemd. Deze activatie zorgt er op haar beurt voor dat macrofagen grote hoeveelheden van een andere molecule, CSF1, uitscheiden en het receptor-niveau voor die molecule, CSF1R, op hun oppervlak verhogen. CSF1 werkt dan in een lus om de M2, pro-metastatische toestand verder te versterken en blijft macrofagen naar de tumor trekken.
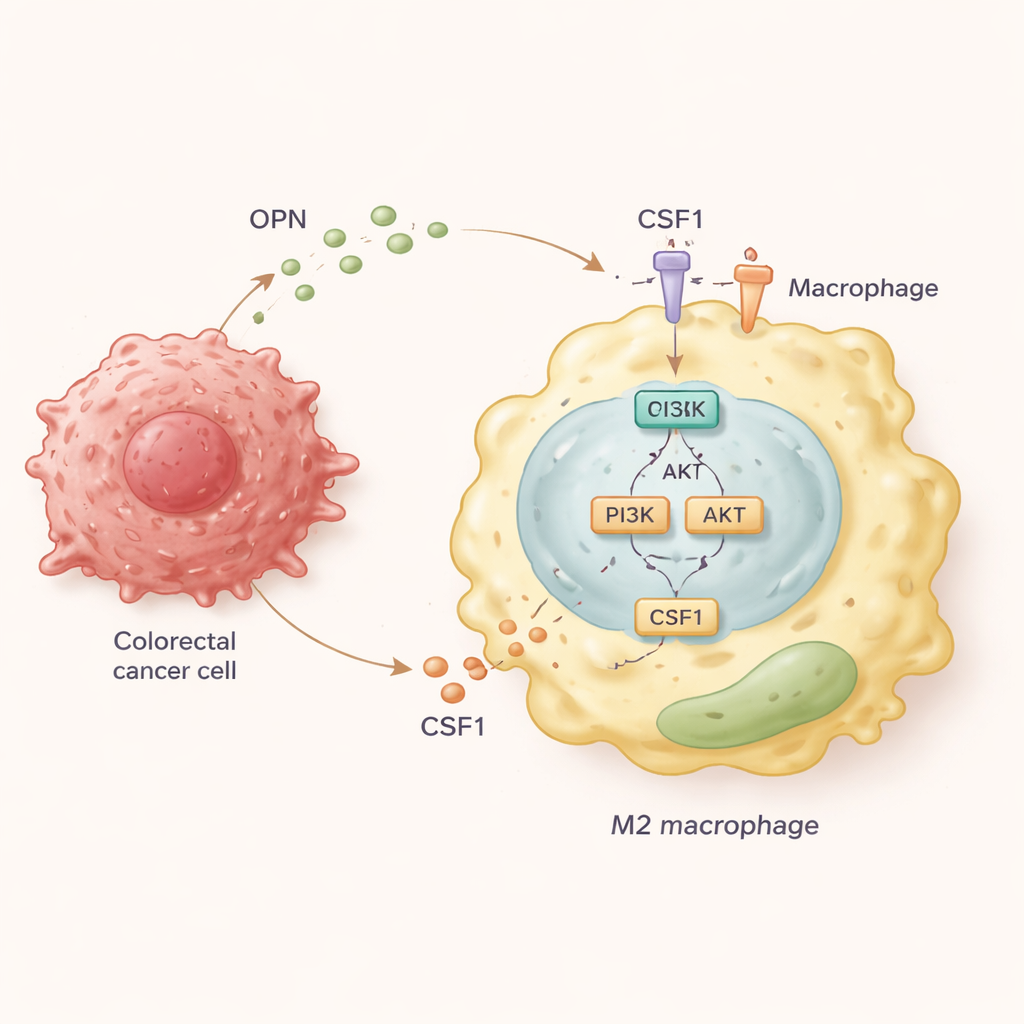
De lus blokkeren om verspreiding te vertragen
In muismodellen van colorectale kanker die zich in de buikholte hadden verspreid, testten de onderzoekers een CSF1R-blokkerend middel genaamd PLX3397. Muizen met OPN-rijke tumoren ontwikkelden veel metastatische knobbeltjes, maar behandeling met de CSF1R-remmer verminderde zowel het aantal uitzaaiingen als de aanwezigheid van M2-achtige macrofagen in de tumoren significant. Tumorcellen vertoonden minder groei en meer tekenen van geprogrammeerde celdood. Belangrijk is dat het middel voornamelijk de tumorbevorderende macrofagen uitputte zonder de meer ontstekingsgerichte typen sterk te beïnvloeden, wat wijst op een relatief gerichte manier om het steunnetwerk van de tumor te verzwakken.
Wat dit betekent voor toekomstige behandelingen
De kernboodschap voor leken is dat sommige colorectale kankers succesvol uitzaaien niet alleen omdat de kankercellen agressief zijn, maar omdat ze nabije immuuncellen kapen en ze veranderen in medeplichtigen. In deze studie fungeert door kankercellen geproduceerde OPN als een meesterchakelaar die macrofagen herprogrammeert via de PI3K/AKT- en CSF1/CSF1R-signaleringsketen, waardoor een vruchtbare bodem voor metastase ontstaat. Door deze keten te onderbreken—in het bijzonder bij de CSF1R-stap—wisten de onderzoekers de tumorsprеiding bij muizen te verminderen. Dit suggereert dat het meten van OPN-niveaus kan helpen patiënten te identificeren die baat kunnen hebben bij geneesmiddelen die macrofagen richten, en dat het combineren van zulke middelen met bestaande behandelingen of immuuntherapieën nieuwe hoop kan bieden voor mensen met gevorderde colorectale kanker.
Bronvermelding: Liang, X., Qin, F., Yuan, Z. et al. Colorectal cancer-derived osteopontin rewires macrophages into a pro-metastatic M2 state via the PI3K/AKT/CSF1-CSF1R axis. Cell Death Discov. 12, 92 (2026). https://doi.org/10.1038/s41420-026-02945-y
Trefwoorden: dikke darmkanker, osteopontine, tumor-geassocieerde macrofagen, metastase, CSF1R-remming