Clear Sky Science · nl
Het gericht aanpakken van NXPH4/ALDH1L2‑signalering onderdrukt enzalutamide‑resistentie bij prostaatkanker
Waarom dit belangrijk is voor prostaatkankerpatiënten
Veel mannen met gevorderde prostaatkanker zijn afhankelijk van een krachtig hormoonblokkerend middel genaamd enzalutamide. In het begin werkt het vaak goed: tumoren krimpen en de ziekte vertraagt. Maar bij de meeste patiënten vindt de kanker uiteindelijk een manier om het middel te omzeilen en begint weer te groeien. Deze studie onderzoekt hoe die ontsnapping plaatsvindt en wijst op een nieuwe kwetsbaarheid in geneesmiddel‑resistente tumoren—wat een mogelijke route biedt om bestaande behandelingen langer en effectiever te laten werken.
Een veelgebruikte behandeling versus een hardnekkige ziekte
De groei van prostaatkanker is sterk verbonden met mannelijke hormonen, of androgenen, die werken via een eiwit dat de androgeenreceptor wordt genoemd. Enzalutamide is bedoeld om deze receptor uit te schakelen en is een standaardtherapie wanneer tumoren niet meer reageren op traditionele hormoonverlagende behandelingen. Helaas passen veel tumoren zich aan en worden wat artsen castratie‑resistente prostaatkanker noemen. De auteurs van dit artikel wilden ontdekken welke genen kankercellen helpen te overleven onder enzalutamide, in de hoop dat het blokkeren van deze helpers het effect van het middel zou kunnen herstellen.
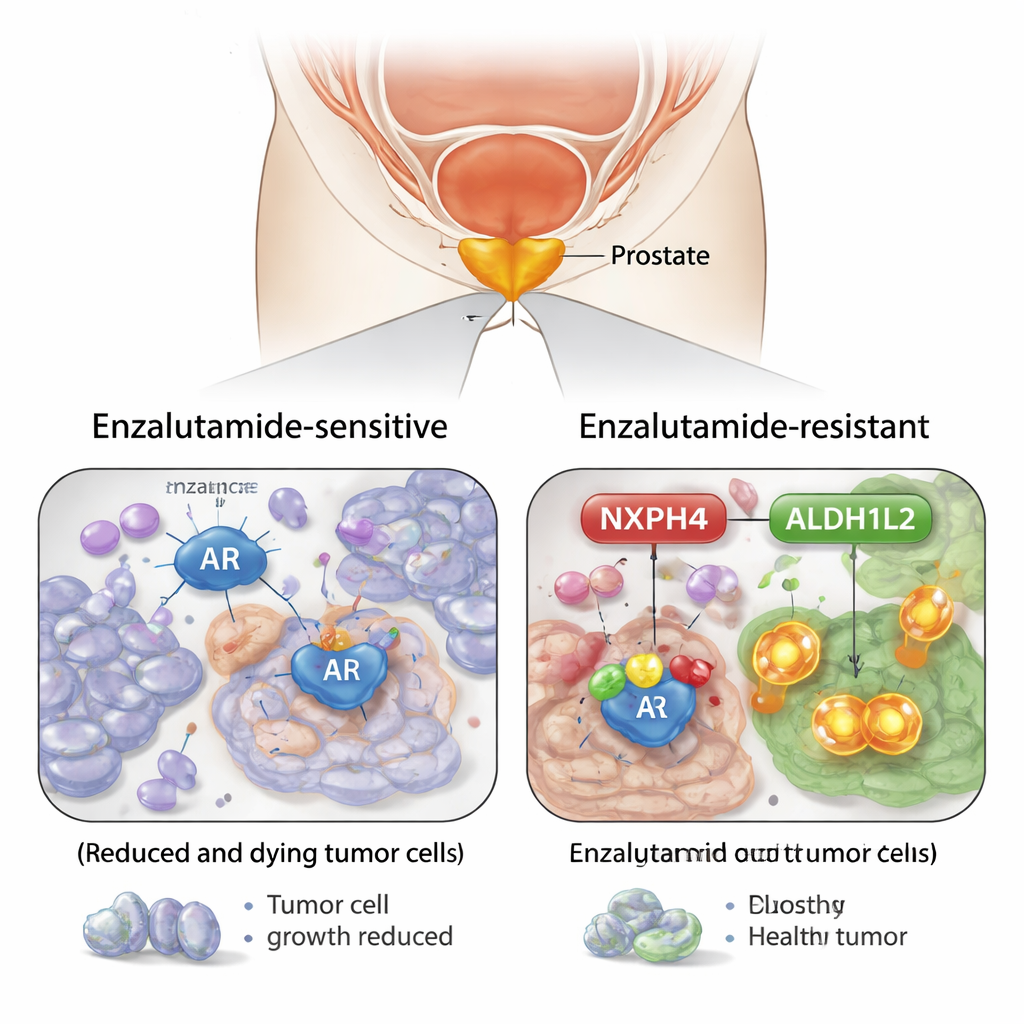
Een verrassend hulpstofje in de schijnwerper
Door prostaatkankercellen die gevoelig waren voor enzalutamide te vergelijken met cellen die resistent waren geworden, identificeerde het team een eiwit genaamd NXPH4 als een belangrijke speler. Resistente cellen maakten veel meer NXPH4 aan, en de niveaus van NXPH4 namen gestaag toe wanneer cellen na verloop van tijd aan enzalutamide werden blootgesteld. Weefselmonsters van patiënten lieten hetzelfde patroon zien: hogere NXPH4 in agressievere tumoren en in kankers die niet langer op het middel reageerden. Wanneer de onderzoekers NXPH4‑niveaus verlaagden in resistente cellen, werden die cellen gemakkelijker te doden met enzalutamide en vormden ze minder kolonies, zowel in kweek als in muismodellen. Omgekeerd maakte het geforceerd extra produceren van NXPH4 cellen moeilijker behandelbaar.
Hoe hormonen NXPH4 activeren
De studie vroeg ook waarom NXPH4 zo overvloedig is in deze tumoren. Het antwoord wees opnieuw naar de androgeenreceptor. De onderzoekers toonden aan dat wanneer cellen werden behandeld met het hormoon dihydrotestosteron, de NXPH4‑niveaus stegen. Bij toevoeging van extra androgeenreceptor nam NXPH4 toe; bij blokkade van de receptor daalde NXPH4. Gedetailleerde DNA‑experimenten bevestigden dat de androgeenreceptor fysiek bindt aan de regelregio van het NXPH4‑gen en het activeert. Dit betekent dat hetzelfde hormoongestuurde systeem dat de groei van prostaatkanker voedt ook cellen voorbereidt met NXPH4, waardoor de basis wordt gelegd voor latere medicijnresistentie.
De energiecentrales van de cel versterken
Dieper gravend, ontdekte het team dat NXPH4 verandert hoe kankercellen energie en stress in hun mitochondriën beheren, de kleine krachtcentrales van de cel. Onder hormoonblokkerende omstandigheden verplaatst een deel van NXPH4 zich naar de mitochondriën en bindt daar aan een ander eiwit, ALDH1L2, dat cruciaal is voor de productie van NADPH, een sleutelmolecuul dat helpt schadelijke reactieve zuurstofsoorten (ROS) te beheersen. In resistente cellen vormen NXPH4 en ALDH1L2 een complex dat de mitochondriale ademhaling stimuleert, het membraanpotentiaal behoudt, NADPH verhoogt en ROS‑niveaus verlaagt. Deze combinatie houdt de mitochondriën gezond en stelt kankercellen in staat de stress door enzalutamide te doorstaan in plaats van te sterven zoals ze normaal zouden doen.
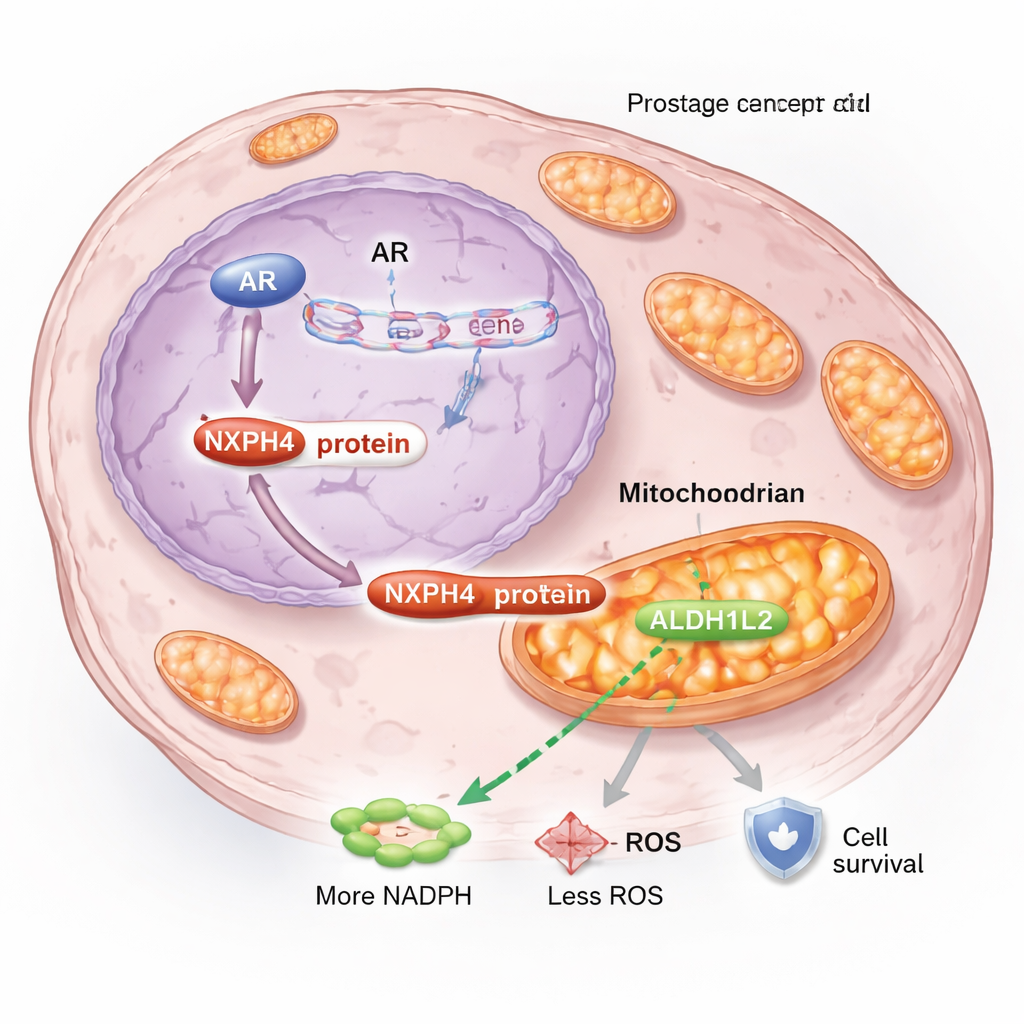
De circuit van resistentie doorbreken
Toen de onderzoekers dit mitochondriale ondersteuningssysteem verstoorden, waren de resultaten opvallend. Het verminderen van NXPH4 in resistente cellen verlaagde de mitochondriale activiteit, verhoogde oxidatieve stress, vertraagde de groei en maakte cellen veel gevoeliger voor enzalutamide. Het uitschakelen van ALDH1L2 had een vergelijkbaar effect en wist de beschermende voordelen van extra NXPH4 uit, wat bevestigt dat deze twee eiwitten samenwerken. In muismodellen groeiden tumoren zonder NXPH4 langzamer, en het combineren van verlies van NXPH4 met enzalutamide deed tumoren nog sterker krimpen dan een van beide benaderingen afzonderlijk. Deze bevindingen suggereren dat het NXPH4–ALDH1L2‑partnerschap niet slechts een bijverschijnsel van resistentie is, maar een drijvende kracht achter die resistentie.
Wat dit kan betekenen voor toekomstige behandeling
Kort gezegd laat dit werk zien dat sommige prostaatkankers enzalutamide overleven door hun energievoorziening te herbedraden. NXPH4, aangezet door de androgeenreceptor, werkt samen met ALDH1L2 in de mitochondriën om ze draaiende te houden, te beschermen tegen oxidatieve schade en tumorcellen te helpen de hormoonblokkerende therapie te doorstaan. Het richten op NXPH4, of op zijn interactie met ALDH1L2, zou dit overlevingscircuit kunnen verzwakken. Hoewel er nog geen medicijnen tegen NXPH4 bestaan, benadrukt de studie dit molecuulpaar als een veelbelovend nieuw doelwit. In de toekomst kan het combineren van enzalutamide met middelen die NXPH4‑ALDH1L2‑signalering verstoren patiënten mogelijk langer voorblijven op resistentie tegen prostaatkanker.
Bronvermelding: Sun, X., Zhang, Y., Zhang, W. et al. Targeting NXPH4/ALDH1L2 signaling suppresses enzalutamide resistance in prostate cancer. Cell Death Discov. 12, 91 (2026). https://doi.org/10.1038/s41420-026-02944-z
Trefwoorden: prostaatkanker, enzalutamide‑resistentie, mitochondriale stofwisseling, NXPH4, ALDH1L2