Clear Sky Science · nl
Trim15 stabiliseert VDAC3 via ubiquitinering om autophagie te onderdrukken en chemosensitiviteit te verhogen bij hypopharyngeaal plaveiselcelcarcinoom
Waarom deze kankerstudie ertoe doet
Hypopharyngeaal plaveiselcelcarcinoom is een moeilijk te behandelen keel‑kanker met lage overlevingskansen en weinig effectieve opties wanneer de ziekte uitzaait of niet meer op medicijnen reageert. Deze studie onthult een verborgen cellair traject dat mede bepaalt of deze kankercellen onder behandeling afsterven of zich stilletjes aanpassen en overleven. Door uit te leggen hoe twee eiwitten, Trim15 en VDAC3, de cellulaire zelfreiniging en stressreacties regelen, wijst het werk op nieuwe manieren om bestaande chemotherapeutica effectiever te maken.
Een dodelijke keelkanker die in het zicht verborgen zit
De hypopharynx ligt diep in de keel, waardoor tumoren daar vaak onopgemerkt groeien tot ze al in een vergevorderd stadium zijn. Op dat moment moeten artsen kiezen tussen agressieve chirurgie die spraak en slikken sterk kan aantasten, of orgaanbehoudende benaderingen zoals chemotherapie en bestraling die niet altijd genezen. Omdat de overleving in de afgelopen decennia weinig is verbeterd, richten onderzoekers zich op de onderliggende biologie die deze tumoren in staat stelt te groeien, uit te zaaien en medicijnresistent te worden. De huidige studie concentreert zich op hoe kankercellen beschadigde mitochondriën—hun energiecentrales—behandelen en hoe dat hun reactie op stress en therapie vormt.
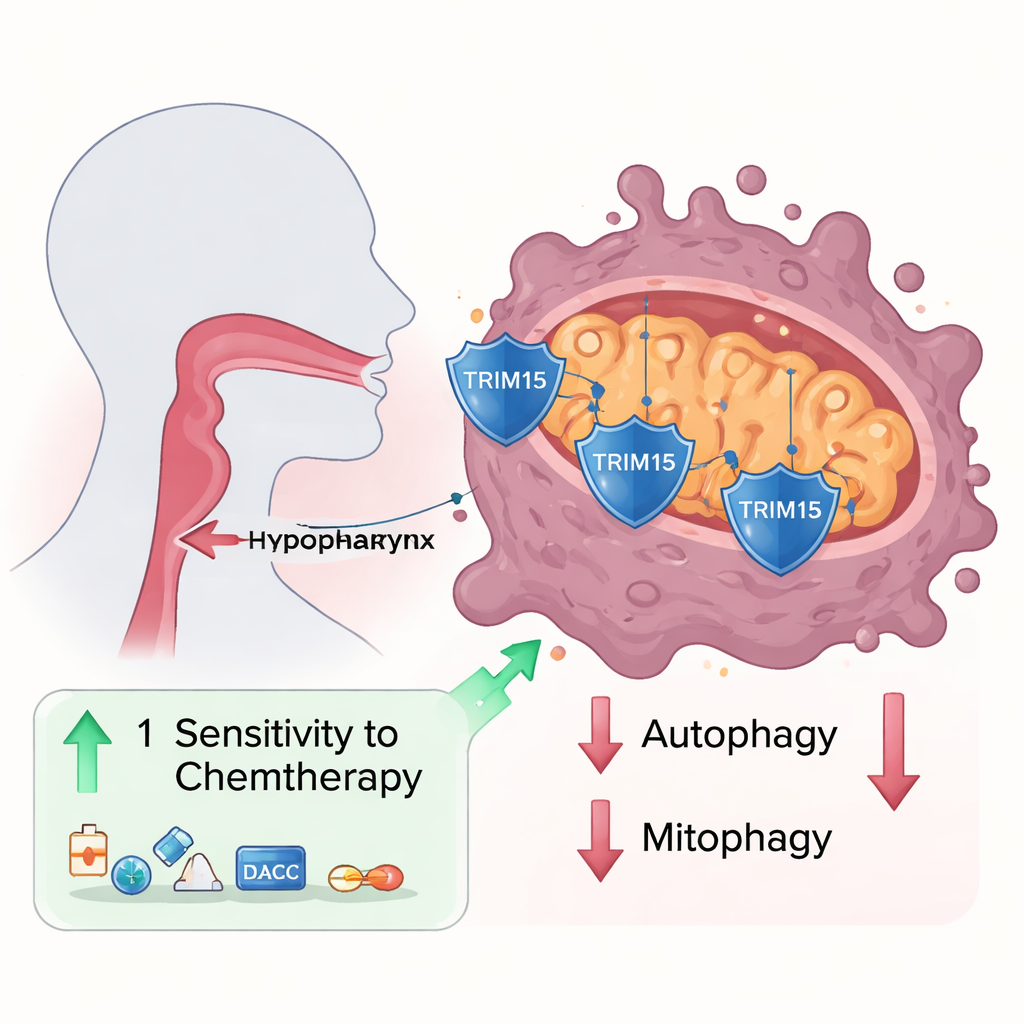
Een beschermend eiwit dat ontbreekt
De onderzoekers bestudeerden tumormonsters en cellijnen van hypopharyngeale kanker en vonden dat een eiwit genaamd Trim15 consequent gereduceerd was vergeleken met het aangrenzende normale weefsel. Wanneer ze kankercellen dwongen meer Trim15 te produceren, groeiden en migreerden de cellen langzamer; bij verwijdering werden de cellen agressiever. Met biochemische pull‑downexperimenten ontdekten ze dat Trim15 fysiek interageert met een ander eiwit, VDAC3, dat in het buitenmembraan van mitochondriën zit en fungeert als poort voor moleculen die in‑ en uitgaan. In plaats van VDAC3 voor afbraak te markeren, voegt Trim15 een specifiek type moleculair label toe dat VDAC3 juist stabiliseert en de niveaus hoog houdt.
Hoe kankercellen hun energiecentrales recyclen
Mitochondriën worden continu gecontroleerd en kunnen, wanneer ze beschadigd zijn, verwijderd worden via een gespecialiseerde recyclingroute genaamd mitofagie. Het team toonde aan dat VDAC3 normaal gesproken als een rem op deze recycling fungeert. Wanneer VDAC3 overvloedig aanwezig was, daalden markers van algemene zelfvertering (autofagie) en mitofagie; wanneer VDAC3 verminderd was, versnelden deze processen en werden meer mitochondriën ingesloten en afgebroken. Deze verandering beïnvloedde ook de balans van reactieve zuurstofsoorten (ROS)—chemisch reactieve moleculen die vaak als cellaire uitlaat worden beschreven. Hoge VDAC3 verhoogde ROS‑niveaus, waardoor de cellen meer gestrest raakten, terwijl lage VDAC3 de cellen in staat stelde beschadigde mitochondriën te verwijderen, ROS te verlagen en beter te overleven onder zware omstandigheden.
Alcohol, oxidatieve stress en medicijnresistentie
Chronische alcoholblootstelling is een belangrijke risicofactor voor hypopharyngeale kanker, deels omdat geconcentreerde ethanol herhaaldelijk het keelslijmvlies ontspoort. Wanneer de onderzoekers kankercellen in het laboratorium aan alcohol blootstelden, daalden zowel Trim15‑ als VDAC3‑niveaus. Deze daling bleek een adaptieve zet van de kankercellen te zijn: door de Trim15–VDAC3‑as te verzwakken, versterkten ze mitofagie, hielden ze ROS op veiligere niveaus en konden ze alcoholgeïnduceerde schade beter verdragen. Een vergelijkbare reactie trad op bij de standaard chemotherapie‑stof 5‑fluorouracil (5‑FU): de behandeling verlaagde Trim15 en VDAC3, wat waarschijnlijk tumorcellen helpt dodelijke oxidatieve stress te vermijden en bijdraagt aan chemoresistentie.
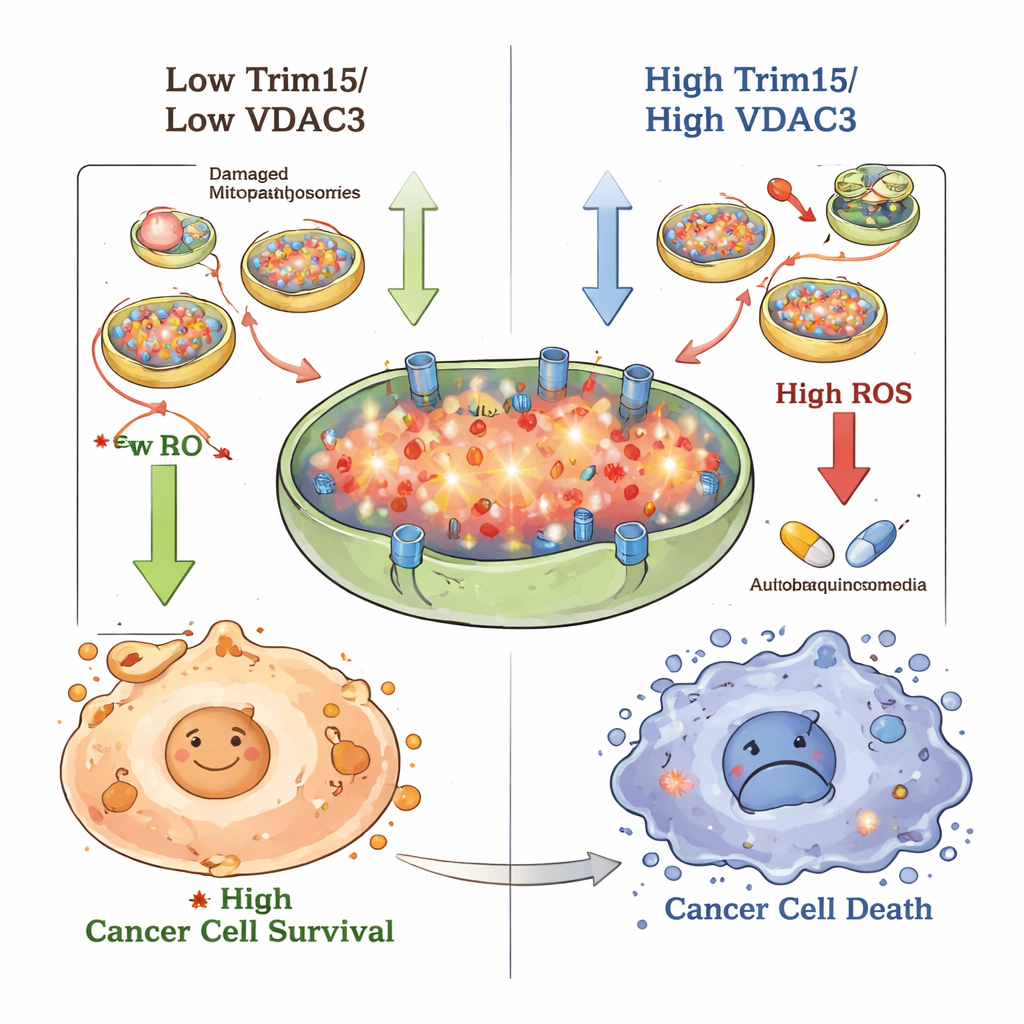
Zelf‑bescherming uitschakelen om chemotherapie te versterken
Het team vroeg zich vervolgens af of het blokkeren van autofagie deze bescherming zou wegnemen. Ze gebruikten chloroquine, een al lang bekend antimalariamiddel dat de laatste stappen van cellulaire zelfvertering verstoort. In kweek remde chloroquine op zichzelf de groei en beweging van hypopharyngeale kankercellen en veegde het het groeivoordeel weg dat ontstond door verlies van VDAC3. Bij muizen met humane tumorgrafts verkleinden chloroquine en 5‑FU elk afzonderlijk tumoren, maar de combinatie werkte het beste en verminderde zowel tumorvolume als gewicht meer dan elk middel afzonderlijk zonder duidelijke extra toxiciteit. Belangrijk: het forceren van cellen om te veel Trim15 of VDAC3 aan te maken maakte ze gevoeliger voor 5‑FU, deels doordat ROS‑niveaus stegen tot waarden die de cellen niet meer konden hanteren.
Wat dit betekent voor toekomstige behandelingen
Voor een leek toont de studie aan dat sommige hypopharyngeale kankercellen chemotherapie overleven door betere recyclers te worden: ze ruimen beschadigde mitochondriën snel op en houden oxidatieve stress net laag genoeg om sterfte te vermijden. Trim15 en VDAC3 werken samen als tegenwicht tegen dit gedrag—wanneer ze aanwezig zijn, beperken ze recycling en verhogen ze stress, waardoor kankercellen makkelijker te doden zijn. Door op deze Trim15–VDAC3–mitofagie‑as te mikken, bijvoorbeeld met middelen zoals chloroquine toegevoegd aan standaardchemotherapie, zouden artsen mogelijk hardnekkige keeltumoren beter behandelbaar kunnen maken en de uitkomsten voor patiënten kunnen verbeteren.
Bronvermelding: Wang, G., Shen, Y., Wang, L. et al. Trim15 stabilizes VDAC3 via ubiquitination to suppress autophagy and enhance chemosensitivity in hypopharyngeal squamous cell carcinoma. Cell Death Discov. 12, 88 (2026). https://doi.org/10.1038/s41420-026-02943-0
Trefwoorden: hypopharyngeale kanker, autofagie, mitochondriën, chemotherapie‑resistentie, chloroquine